EU will saRNA Kostaive zulassen Teil 6
Post-marketing Daten der zweimonatigen Nachbeobachtung und japanische Herstellerinformationen
Teil 1 der Erklärungen zum japanischen Zulassungsdokument
Teil 2 der Erklärungen zum japanischen Zulassungsdokument
Teil 3 der Erklärungen zum japanischen Zulassungsdokument
Teil 4 der Erklärungen zum japanischen Zulassungsdokument
Teil 5 der Erklärungen zum japanischen Zulassungsdokument
Roger Bittel hat mir über einen seiner Kontakte den Link geschickt, wo man die japanischen Informationen findet, was mit den saRNA Gespritzten passierte.
Übersetzt mit deepl.com, weil ich kein Japanisch kann. Ich kann die Übersetzung also auch nicht kontrollieren. Ich bin komplett auf die KI angewiesen. Die (übersetzten) Dokumente sind in diesem Artikel zum Download oder als Link hinterlegt.
Fachportal
Auf dem Fachportal sind Zwischenberichte transparent direkt zugänglich, man muss nicht erst klagen, wie im wilden Westen der EU.
Erster Zwischenbericht
Leider fehlt der erste Zwischenbericht und ist (noch) nicht als pdf verlinkt.
Die meisten Dokumente kann ich aber nicht übersetzen, weil man den Text nicht in Deepl kopieren kann und Deepl das pdf auch nicht übersetzen kann. Die Rechte der pdfs sind eingeschränkt und ich weiß nicht, wie ich das entfernen kann.
Zweiter Zwischenbericht
Verschreibungspflichtige Arzneimittel | Meiji Seika Pharma Co., Ltd.
Dieses Dokument hat nur 4 Seiten (im japanischen Original 3 Seiten).
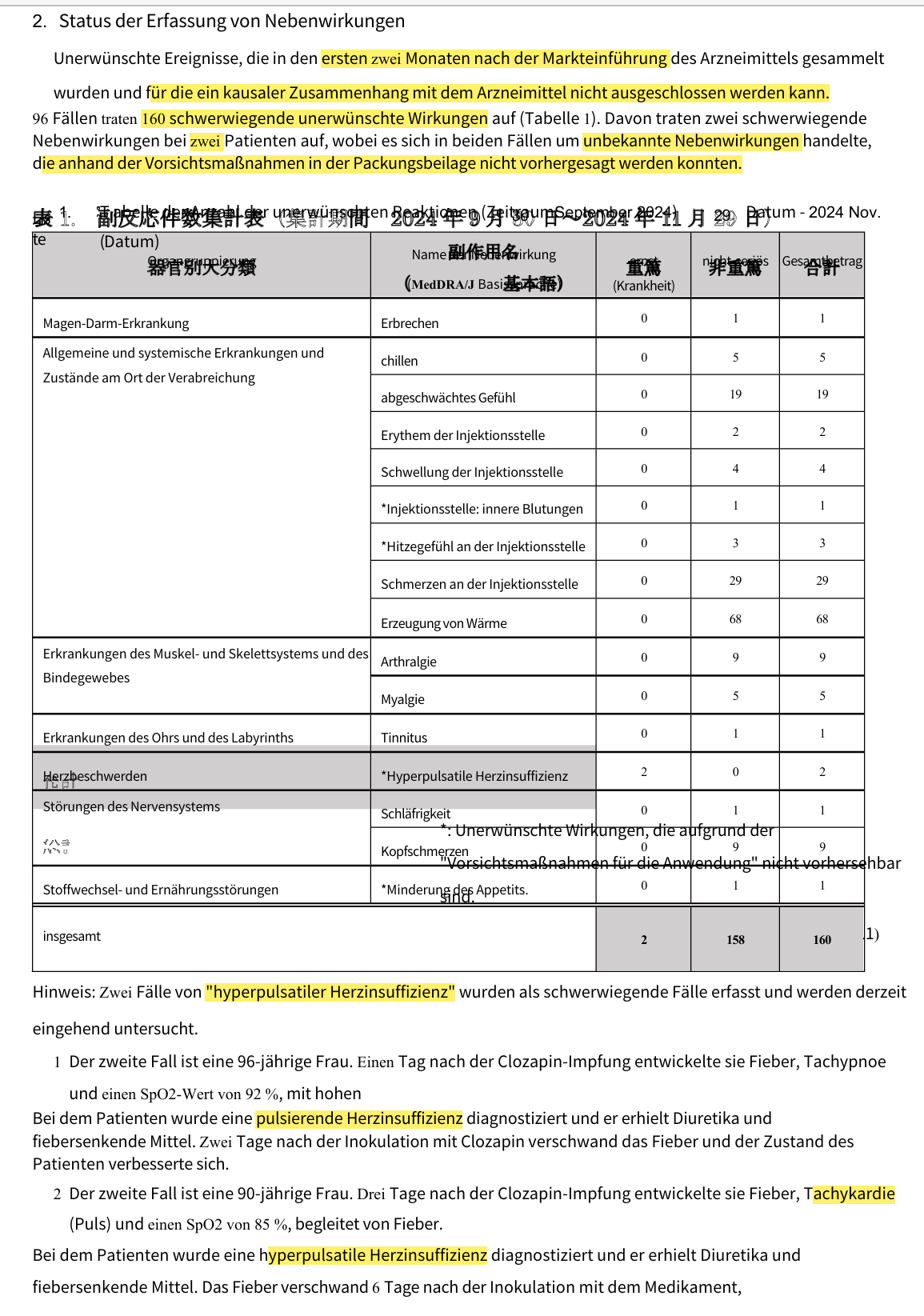
Die post-marketing Studie dauerte nur zwei Monate. Bereits in den ersten zwei Monaten nach Markteinführung wurden folgende unerwünschte Nebenwirkungen gemeldet.
Zwei Menschen entwickelten eine Herzinsuffizienz, die als hyperpulsatil bzw. pulsierend beschrieben wird. Keine Ahnung, ob das an der Übersetzung liegt. Ich schätze, das ist eine Herzinsuffizient mit erhöhter Schlagfrequenz. Im englischen Dokument steht “pulsatile heart failure” und “hyperpulsatile heart failure”.
Herzinsuffizient endet IMMER TÖDLICH.
NYHA ist ein Maß für die Schädigung des Herzens. Es gibt vier Stufen:
Stadium I: Trotz nachweisbarer Herzerkrankung keine Beschwerden; im Alltag uneingeschränkte körperliche Leistungsfähigkeit
Stadium II: Leistungseinschränkung und Beschwerden bei starker körperlicher Belastung (Treppensteigen über zwei Etagen, Wandern in unebenem Gelände); in Ruhe oder bei leichter Tätigkeit fühlen sich die Kranken aber wohl
Stadium III: Beschwerden schon bei alltäglicher leichter körperlicher Belastung wie Gehen auf ebener Strecke; Beschwerdefreiheit in Ruhe
Stadium IV: Beschwerden bereits in Ruhe; körperliche Tätigkeiten sind nicht möglich, ohne dass Beschwerden auftreten
Tritt Atemnot bereits bei alltäglicher leichter Belastung auf (NYHA III), so sterben 25 % der Betroffenen innerhalb eines Jahres, bei Atemnot bereits in Ruhe (NYHA IV) sind es über 50 %.1
Beipackzettel
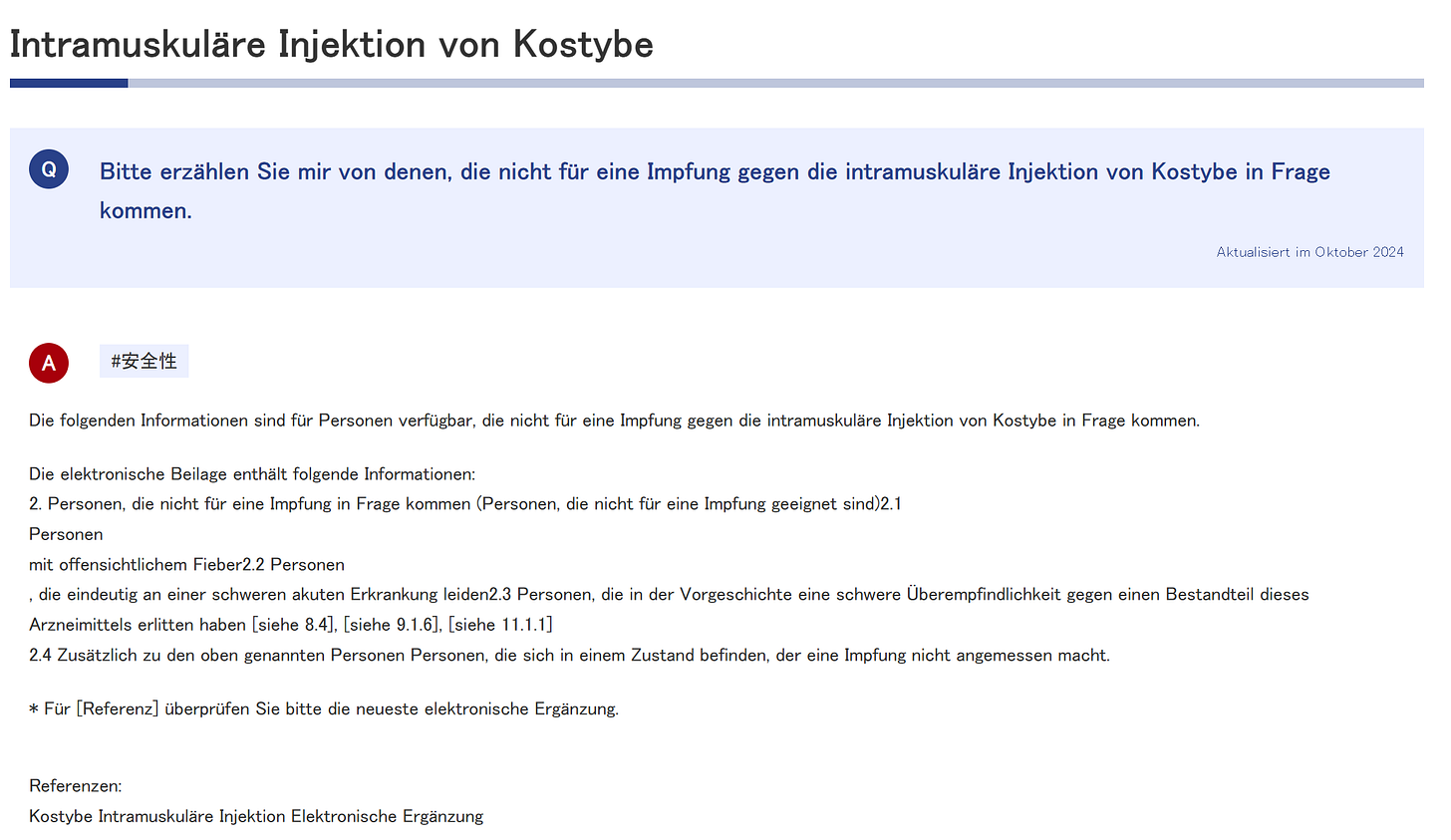
Wer nicht geimpft werden darf
Selbsterklärend. Keine Ahnung, wie lange es wirkt, das ist zumindest ehrlich. Ob das so direkt auch in den deutschen Beipackzetteln stehen wird?
Was ist mir CAPRA-Reaktionen auf LNPs?
CARPA Reaktionen sind Komplement aktivierte Pseudoallergien, die nicht vorhersagbar, nicht testbar, schnell oder langsam eintreten können und mitunter tödlich enden. 5% bis 45% der Menschen reagieren mit einer CARPA Reaktion auf Nanolipide im Gegensatz zu weniger als 2% auf Penicillin.2
Scheint bei saRNA möglichwerweise direkt in die Herzinsuffizienz zu gehen, wenn man sich das post-marketing Dokument anschaut.
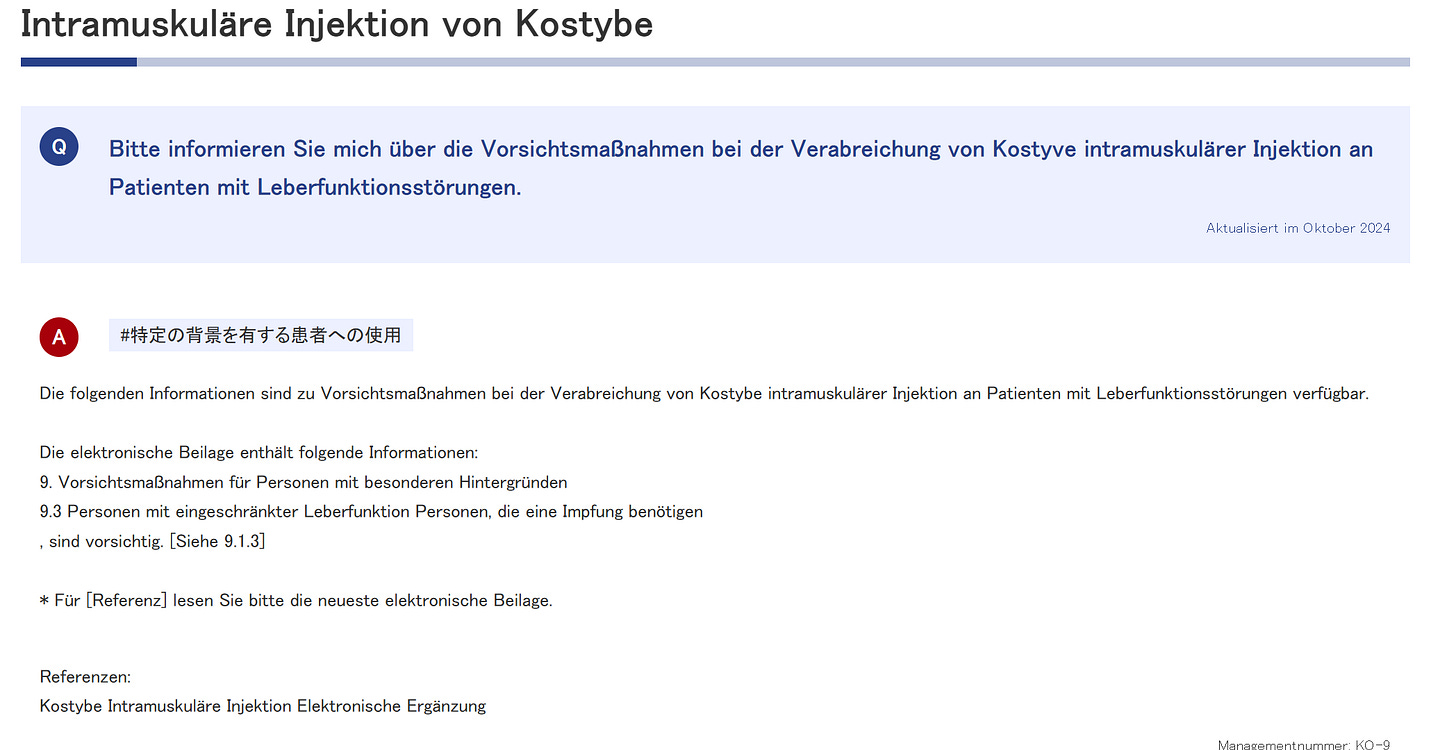
Das Lustige an Abschnitt 9 des Beipackzettels ist, dass die Schwurbler exakt das 2021 auch gesagt haben: Erst einmal einen Allergietest mit dem Lipid machen (das ein Allergologe gar nicht so einfach bekommt). Und solange das das nicht ausgeschlossen ist, keine Impfung. Dafür wurden wird diffamiert und ausgelacht. Hier steht es im Beipackzettel.
Man hat vor allem Menschen mit Vorerkrankungen gespritzt, die hier ausgenommen sind. Wer nimmt Blutverdünner? Meist Herzkranke. Die hat man mit modRNA besonders bevorzugt. So gesehen, ein recht ehrlicher Beipackzettel. Nur geeignet für ganz gesunde Menschen (die das Produkt nicht benötigen).
Da zwei vollkommen neue Substanzen verwendet werden (ATX-126 und Kaliumsorbat wurden vorher noch nie für intramuskuläre Injektionen verwendet3), die vorher nicht im Menschen getestet wurden und zudem CARPA Reaktionen auftreten können, hat auch der Allergologe ein Problem bei der Bescheinigung.
Aber in der Plandemie war jeder impffähig, der hier explizit ausgeschlossen wird.
Ansonsten steht auch das drinnen, was man aus dem Zulassungsdokument schon kennt.
Wehe die EU lässt es für unter 18 zu.
Bei Myokarditis ist man direkt und hat sogar die Darmalfiller erwähnt:
Was die Nutzlosigkeit angeht, ist man auch sehr transparent: 56,6%, damit eigentlich unter der Hürde, die die EU für eine Zulassung gesetzt hatte.
modRNA mit Fremdkörpern und Verfärbungen wurde in der Plandemie routinemäßig trotzdem verwendet, wurde mir aus Impfzentren zugetragen. Einfach um die Trübung herum aufziehen, hieß es da.
Formular zur Meldung unerwünschter Ereignisse
FAQ Seite:
Hier wird der Beipackzettel in Fragen aufgeteilt, die letzendlich nur den Inhalt des Beipackzettels nach Sektionen wiedergeben.
Fazit
Die Hersteller gehen mit den Problemen in den Dokumenten, die google oder deepl übersetzen kann, sehr offen und direkt um. Man versucht nicht vorzutäuschen, dass dieses Produkt besonders effizient wäre mit 56,6%. Man ist transparent, dass das Produkt für jene, die es bräuchten, wenn es funktionieren würde, nicht geeignet ist und dass man eigentlich kaum Daten hat und nicht weiß, wie lange das Produkt überhaupt wirkt.
Wer sich den Scheiß trotzdem spritzen lässt ist somit selbst Schuld.
Es ist wieder einmal die Politik, die ein unnützes, schädliches Produkt vermarktet, nicht der Hersteller.
Update
Sieht nicht gut aus in Japan.
EU will saRNA Kostaive zulassen Teil 1
Nachdem ich nun von diversen Seiten wegen der saRNA Sache genervt werde, habe ich mich notgedrungen mit den japanischen Unterlagen beschäftigt.









































Pfizer-Sprecherin Small war damals auch offen vorm EU-Parlament, “with the speed of science”. Gleichzeitig hat ihr Chef Bourla öffentlich gelogen, dass sich die Balken biegen.
Die Hersteller sprechen auch diesmal nicht mit einer Stimme: da, wo sie wissen, dass es nur Fachleute zur Kenntnis nehmen, sind sie recht offen. DIe Werbeabteilung strickt derweil mit Politik und Medien weiter an der nächsten Lügengeschichte – und jeder, der öffentlich widerspricht, ist wieder ein Coronaleugner.
So läuft die Nummer.
Hallo Dr. Stebel, Sie haben in Ihrem letzten Beitrag im Corona-Ausschuss über diese japanischen sa-"Impfstoffe" gesprochen und dabei im Nebensatz erwähnt, das der pH-Wert in der Zelle einen Einfluss auf die Knochenzusammensetzung haben könnte. Sie erwähnten, dass Ihnen dieses Phänomen zugetragen wurde. Mein Vater 88, 3 mal gespritzt (letzte im Herbst 2022) und danach subsituiert von mir mit Vit D hochdosiert und K sowie anderen auch von Ihnen und von Florian Schilling empfohlenen Nahrungsergänzungsstoffen hat im Anschluss eines Beckenanbruches einen Knochenschwund im Becken, Rücken, Steissbereich gehabt, der dann in einer OP mit drei Metallstangen fixiert werden musste. Die Chrirugen sprachen von Knochenschwäche, die das ausgelöst hat. Zwischen beiden Vorfällen lagen 8 Wochen, auf dem ersten Röntgen war der Knochenschwund nicht zu sehen, nur der kleine Bruch an der Beckenseite. Im 2. Röntgen nach 8 Wochen war das dann plötzlich vorhanden. Ich glaube das überhaupt nicht, und habe dann versucht Studien zu finden, die diesen Knochenschwund als Nebenwirkung der C-"Impfung" beschreiben, aber bisher nichts gefunden. Können Sie mir da weiterhelfen? LG und danke für Ihre Arbeit. Lisa Peters