Die Plörre ist wohl innen flüssig
ALC-0315 liegt flüssig im Kern des LNP vor und kann die modRNA mutieren
Man sollte ja meinen, dass wenn man ein Produkt auf dem Markt wirft, der Hersteller zumindest wissen sollte, wie dieses Produkt aussieht.
Wie es ausschaut, wussten BioNTech/Pfizer nicht einmal das.
DAS muss nun von Wissenschaftlern an Universitäten aus reinem Forschergeist heraus bestimmt werden. Der Pharma war das zu aufwändig solche Untersuchungen durchzuführen. Wozu auch, hat ja keiner verlangt, dass sie beschreiben, wie ihr Produkt tatsächlich aussieht oder funktioniert.
Schauen wir mal, was mittlerweile zur Struktur des BioNTech/Pfizer Gebräus erforscht wurde. Dass heißt nicht, dass das der Weisheit letzter Schluss ist. Es ist aber zumindest eine Näherung, die zeigt, dass die Realität den eingereichten und kursierenden Modellen so gar nicht entspricht.
Ich befinde mich hier mal wieder thematisch auf dünnem Eis. Keine der Methoden, mit denen in den Publikationen, die ich hier vorstellen werde, habe ich selbst eingesetzt. Ich bin auf diesen Gebieten Laie und versuche selbst zu verstehen, was die Autoren mit damit sagen wollen. Ich bevorzuge eigentlich Reviews, die sind fachfremd einfacher zu lesen.
Die Artikel, um die es in diesem Substack geht, sind aber Forschungsartikel und zwar diese drei:
Szebeni J, Kiss B, Bozó T, Turjeman K, Levi-Kalisman Y, Barenholz Y, Kellermayer M. Insights into the Structure of Comirnaty Covid-19 Vaccine: A Theory on Soft, Partially Bilayer-Covered Nanoparticles with Hydrogen Bond-Stabilized mRNA-Lipid Complexes. ACS Nano. 2023 Jul 25;17(14):13147-13157. doi: 10.1021/acsnano.2c11904. Epub 2023 Jul 7. PMID: 37417667; PMCID: PMC10373524. https://pubmed.ncbi.nlm.nih.gov/37417667/
Unruh T, Götz K, Vogel C, Fröhlich E, Scheurer A. SAXS/PCS study on the mesoscopic structure of lipid nanoparticle (LNP) formulations for mRNA drug delivery: Comirnaty and drug-free LNP dispersions. ChemRxiv. Cambridge: Cambridge Open Engage; 2023; This content is a preprint and has not been peer-reviewed. https://chemrxiv.org/engage/chemrxiv/article-details/64dff30d01042bc1cc4b9ce3
ACS Nano 2024 18 (13), 9746-9764
DOI: 10.1021/acsnano.4c02610
Packer M, Gyawali D, Yerabolu R, Schariter J, White P. A novel mechanism for the loss of mRNA activity in lipid nanoparticle delivery systems. Nat Commun. 2021 Nov 22;12(1):6777. doi: 10.1038/s41467-021-26926-0. PMID: 34811367; PMCID: PMC8608879. https://pubmed.ncbi.nlm.nih.gov/34811367/
Dieses dritte Paper ist spannend, weil es auch dem Hause Moderna stammt, also von einer wirklich ernst zu nehmenden Quelle.
Hermosilla J, Alonso-García A, Salmerón-García A, Cabeza-Barrera J, Medina-Castillo AL, Pérez-Robles R, Navas N. Analysing the In-Use Stability of mRNA-LNP COVID-19 Vaccines Comirnaty™ (Pfizer) and Spikevax™ (Moderna): A Comparative Study of the Particulate. Vaccines (Basel). 2023 Oct 25;11(11):1635. doi: 10.3390/vaccines11111635. PMID: 38005967; PMCID: PMC10675537. https://pubmed.ncbi.nlm.nih.gov/38005967/
Bei den Autoren sind zwei dabei, über die ich bereits in anderem Zusammenhang schon einige Male gestolpert bin.
Szebeni J. aus dem zweiten Artikel ist derjenige, der Schweinen Comirnaty gespritzt hat und wo dann eines der 14 Schweine wiederbelebt werden musste, nachdem 6 eine CARPA Reaktion gezeugt hatten. Das hatte ich in diesem Substack abgearbeitet: https://drbine.substack.com/p/kationische-nanolipide-was-die-hersteller
Tobias Unruh kennt man von der Aktion
https://wissenschaft4allesdichtmachen.de/
und auch von der Aktion Wissenschaftler gegen Impfpflicht (https://tkp.at/2021/12/10/offener-brief-von-wissenschaftlern-gegen-impfpflicht/)
Hier sind Szebeni und Unruh nicht Gruppenleiter und Letztautor, in den hier besprochenen Papern sind sie die Erstautoren und somit Experimentatoren. Das ist auffällig, sehr auffällig. Professoren/Gruppenleiter gibt es eher selten als Experimentator und Erstautor, die stehen für gewöhnlich immer ganz hinten als Gruppenleiter. (Es sei denn sie geben ihrer Frau den Letztautor und trösten sich mit dem Erstautor, während sie den Doktoranden auf die Position der technischen Assistentin verbannen, wie es mir bei meinem Paper passiert ist.) Dass beide in diesem Fall selbst zur Pipette gegriffen haben, ist mehr als auffällig und extrem ungewöhnlich. Einerseits erfahrene Wissenschaftler als Experimentatoren, andererseits sind diese möglicherweise handwerklich in etwa so eingerostet wie ich und haben die Experimente heimlich, am Wochenende, in ihrer Freizeit durchgeführt, wie ich das gemacht hätte. Schwer zu sagen.
Die Autoren des dritten Papers sind mir bisher noch in keinem Corona-Zusammenhang aufgefallen.
Ich erwähne das, weil… ja, die ersten beiden Paper haben natürlich einen BIAS, wenn man sich anschaut, auf welcher Seite die Autoren stehen. Genau wie die Paper der Gegenseite ebenfalls einen BIAS zu Gunsten der modRNA-Technologie haben. Das sollte man sich bewusst manchen, wenn man wissenschaftliche Literatur liest. Ganz besonders, wenn Professoren selbst zur Pipette greifen.
Es gibt keine ideologiefreie Forschung, es gibt überhaupt keine ideologiefreie Meinung. Jeder hat eine Ideologie, man muss sich dessen bewusst sein. Louis Althusser hat dazu Einiges veröffentlicht (https://www.marxists.org/reference/archive/althusser/1970/ideology.htm). Das lernt man im ersten Semester „Einführung in die Kulturstudien“, wenn man eine Geisteswissenschaft studiert, das gehört zu den Grundlagen (die den Naturwissenschaftlern leider meist fehlen).
Ich bin in meinen Artikeln auch nicht frei von Ideologien. Ich bin mir dessen bewusst. Ich weise daher in diesem Artikel einmal auf das Problem hin, weil es bei den besprochenen Papern definitiv zu einem Bias führen kann und ich so fair bin, die Leser darauf hinzuweisen. Ich könnte diese auffälligen Tatsachen auch verschweigen und damit den möglichen Bias verschleiern, habe mich aber dazu entschieden, das Problem direkt an den Anfang zu stellen, damit das nicht zu einem Problem wird, sollte das bei Nutzung dieser Artikel vor Gericht als Problem hochblubbern.
Diese Paper sind aufgrund der Auffälligkeiten bei der Erstautorenschaft vor Gericht sehr vorsichtig einzusetzen zumal eines der Paper auch noch ein Preprint in der ersten Fassung ist.
=== 1. Einblicke in die Struktur des Impfstoffs Comirnaty Covid-19: Eine Theorie über weiche, teilweise mit einer Doppelschicht überzogene Nanopartikel mit wasserstoffbrückenstabilisierten mRNA-Lipid-Komplexen ===
Im Juli erschien ein Paper von Szebeni, welches sich die Lipide von außen mit diversen mikroskopischen Methoden anschaut.
Verwendet wurden folgende Methoden:
AFM = atomic force microscopy = Rasterkraftmikroskopie
Wikipedia beschreibt diese Technik wie folgt (ich schätze, bei rein technischen Beschreibungen wird Wikipedia noch nicht manipulieren, ist ja recht unpolitisch. Daher begehe ich die wissenschaftliche Sünde, in diesem Artikel ein wenig aus Wikipedia zu zitieren.):
„Das Rasterkraftmikroskop, auch atomares Kraftmikroskop oder Atomkraftmikroskop (englisch atomic/scanning force microscope; Abkürzungen AFM bzw. SFM, seltener RKM) genannt, ist ein spezielles Rastersondenmikroskop (Rastersondenmikroskopie (englisch scanning probe microscopy, SPM) ist der Überbegriff für alle Arten der Mikroskopie, bei welchen das Bild nicht mit einer optischen oder elektronenoptischen Abbildung (Linsen) erzeugt wird wie beim Lichtmikroskop (LM) oder dem Rasterelektronenmikroskop (REM), sondern über die Wechselwirkung einer sogenannten Sonde mit der Probe. https://de.wikipedia.org/wiki/Rastersondenmikroskopie). Es ist ein wichtiges Werkzeug in der Oberflächenchemie und dient zur mechanischen Abtastung von Oberflächen und der Messung atomarer Kräfte im Nanometerbereich. Eine nanoskopisch feine Nadel wird mittels einer Blattfeder gegen die zu messende Probe gedrückt, und die atomaren Kräfte biegen die Blattfeder. Diese Auslenkung kann mit Licht gemessen werden, und damit kann die Kraft berechnet werden, die zwischen den Atomen der Oberfläche und der Spitze wirkt. Da zwischen der Probe und der Spitze kein Strom fließt, können auch nichtleitende Proben untersucht werden“ (https://de.wikipedia.org/wiki/Rasterkraftmikroskop)
TEM = transmission electron microscopy = Transmissionselektronenmikroskopie
„Die Transmissionselektronenmikroskopie (TEM, steht auch für Transmissionselektronenmikroskop) ist eine Betriebsart für Elektronenmikroskope, die eine direkte Abbildung von Objekten mithilfe von Elektronenstrahlen ermöglicht. […] Die Elektronen durchstrahlen das Objekt, das ausreichend dünn sein muss. Je nach Ordnungszahl der Atome, aus denen das Objekt besteht, der Höhe der Beschleunigungsspannung und der gewünschten Auflösung kann die sinnvolle Objektdicke von wenigen Nanometern bis zu einigen Mikrometern reichen.“ (https://de.wikipedia.org/wiki/Transmissionselektronenmikroskop)
Cryo-TEM = cryogenic transmission electron microscopy = Kryoelektronenmikroskopie
Die Kryoelektronenmikroskopie (Kryo-EM) ist eine Form der Transmissionselektronenmikroskopie (TEM), bei welcher biologische Proben bei kryogenen Temperaturen (≲ −150 °C) untersucht werden. (https://de.wikipedia.org/wiki/Kryoelektronenmikroskopie)
DLS = dynamic light scattering = Dynamische Lichtstreuung
Bei der dynamischen Lichtstreuung (DLS) […] handelt es sich um eine Analyse-Methode, bei der das Streulicht eines Lasers an einer gelösten bzw. suspendierten Probe ermittelt wird. Sie wird am häufigsten bei Polymeren und Biopolymeren wie zum Beispiel Proteinen angewandt, um den hydrodynamischen Radius (Der hydrodynamische Radius ist der Radius einer hypothetischen festen Kugel, die in einem Lösungsmittel dieselben Diffusionseigenschaften besitzt wie das durch den hydrodynamischen Radius beschriebene Teilchen (zum Beispiel Ion, Protein, Micelle, Virus oder Staubpartikel (https://de.wikipedia.org/wiki/Hydrodynamischer_Radius). Der hydrodynamische Durchmesser beträgt das Doppelte des hydrodynamischen Radius.) der Moleküle zu bestimmen.
Die Bilder, die man mit einem Rasterkraftmikroskop (AFM) erzeugen kann sehen dann so aus:
A/E frisch verdünnte Comirnaty Probe von einer Größe von ca. 120-150nm Durchmesser und 40-60nm topographischer Höhe. Durch das Aufliegen auf die Glasplatte werden die LNPs natürlich platter und verändern ihre Form im Vergleich zum freien schwimmen in Lösung.
B/F 1 Tag bei 4°C, sieht deutlich anders und verklumpter aus
C/G aufgetautes Produkt noch mal eingefroren und dann wieder aufgetaut. Double frozen wie man das manchmal von der Fischtheke von einigen Fischen kennt. Sieht ziemlich zerlegt aus.
D/H Frische Probe Doxil, zum visuellen Vergleich.
Doxil ist ein Chemotherapeutikum und war der erste von der FDA 1995 zugelassene Nanowirkstoff (https://www.sciencedirect.com/science/article/abs/pii/S0168365912002301).
Man sieht, dass wenn man die Plörre bei 4°C im Kühlschrank hält, wie man das einige Tage darf,verändert sich die Struktur der der Lipidpartikel. Sie werden größer und verklumpen. Nach einem Tag sieht es schon nicht mehr so gut aus. Wie das nach 10 Wochen aussehen mag… Ob BioNTech dazu AFM Bilder hätte?
Die Haltbarkeitsinfos beziehen sich auf den neuen XBB.1.5 Schlonz und kommen direkt von BioNTech (infoservice@biontech.de). Vielleicht mag da jemand mal nach AFM Bildern nach jeweils 1,2,3,4,5,6,7,8,9 und 10 Tagen/Wochen fragen.
Ergebnisse der dynamischen Lichtstreuung = Größenbestimmung der LNP
Da die LNPs auf der Glasplatte für die Vermessung mit AFM abgeplattet werden, hat man sie noch mal freischwebend in Lösung vermessen.
Comirnatiy war in Lösung von der LNP Größe somit deutlich kleiner und im Bereich von 80-85 und ähnlich klein wie Doxil.
Die beiden Substanzen unterscheiden sich aber in ihrer Oberflächenladung. Comirnaty hatte eine eher positive Ladung von 8.6 während Doxil deutlich negativer war mit -31, was auch immer die Einheit dieser Ladungen war.
Veränderung des Streulichtverhaltens über die Zeit hat man leider nicht gemessen. Damit hätte man Aggregierung und Haltbarkeit abschätzen und mit den AFM Bildern in Bezug setzen können. Diese Messung fehlt mir hier.
Ergebnisse der Rasterkraftmikroskopie
EN: “Lack of sawtooth-like transitions indicates no hairpin openings in RNAs being pulled from the supporting surface- […] The present study suggests that Comirnaty NPs are soft, deformable, and highly compliant structures.”
DE: „Das Fehlen sägezahnartiger Übergänge deutet darauf hin, dass keine Haarnadelöffnungen in den RNAs vorhanden sind, die von der Trägeroberfläche gezogen werden - [...] Die vorliegende Studie legt nahe, dass Comirnaty NPs weiche, verformbare und hochgradig nachgiebige Strukturen sind.“
Ergebnisse der Kryoelektronenmikroskopie
Wenn man die Lipide schock- und tieffriert, behalten sie ihre Form auch auf dem Objektträger des Elektronenmikroskops. Man kann sie also noch einmal vermessen, ohne, dass sie auf dem Objektträger wegen Elektrostatik oder Erdanziehung plattgedrückt werden.
Ich kann mich aus dem Elektronenmikroskopischen Kurs noch grob erinnern, dass man die gefrorenen Blöcke in einer großen Maschine geschnitten und/oder gebrochen hat. Diese Gefrierschnitte hat man dann mikroskopiert. Ich schätze, hier war es ähnlich.
Erneut hat man Comirnaty mit Doxil verglichen und sieht direkt, dass diese zwei Produkte in ihrem Inneren sehr unterschiedlich aussehen.
EN: “Consistent with the AFM images of fresh Comirnaty (Figure 1A) cryo-TEM images of the freshly diluted vaccine (Figure 3A−C) showed spherical NPs. These NPs exhibit a relatively broad size distribution having about 50 to 200 nm diameter. However, mostly, NPs having 50−80 nm diameters were observed, which may suggest a bimodal distribution. Many of the NPs have a solid core with an electron-dense interior, distinct from the diffused aqueous background.”
DE: "In Übereinstimmung mit den AFM-Bildern von frischer Comirnaty (Abbildung 1A) zeigten Kryo-TEM-Bilder des frisch verdünnten Impfstoffs (Abbildung 3A-C) kugelförmige NPs. Diese NPs weisen eine relativ breite Größenverteilung mit einem Durchmesser von etwa 50 bis 200 nm auf. Meistens wurden jedoch NPs mit Durchmessern von 50-80 nm beobachtet, was auf eine bimodale Verteilung schließen lässt. (*Anmerkung: „Eine bimodale Verteilung ist eine Wahrscheinlichkeitsverteilung oder Häufigkeitsverteilung, bei der die Dichte bzw. deren Schätzung zwei besonders ausgeprägte lokale Maxima aufweist. (https://de.wikipedia.org/wiki/Bimodale_Verteilung)“*) Viele der NPs haben einen festen Kern mit einem elektronendichten Inneren, das sich von dem diffusen wässrigen Hintergrund unterscheidet."
EN: “The cryo-TEM images of Comirnaty NPs highlight another phenomenon: the presence of electron-dense surface “caps” covering parts of the NPs (orange arrows), which resemble a bilayer coating, as in Doxil (Figure 3D). Thus, we hypothesize that these thick semicircle lines are phospholipid bilayers and that Comirnaty NPs are intermittently coated with phospholipid bilayers. In bilayer-free surface areas the IPC lipids and cholesterol should, of necessity, form monolayers. PEG lipids may also be present in these regions, as with lack of proper PEG surface coverage LNPs would quickly fuse. These observations are in keeping with the lack of clear signs of the lipid bilayer envelope by AFM force spectroscopy.”
DE: "Die Kryo-TEM-Bilder von Comirnaty NPs heben ein weiteres Phänomen hervor: das Vorhandensein von elektronendichten Oberflächen-"Kappen", die Teile der NPs bedecken (orangefarbene Pfeile), die einer Doppelschichtbeschichtung ähneln, wie bei Doxil (Abbildung 3D). Wir stellen daher die Hypothese auf, dass es sich bei diesen dicken halbkreisförmigen Linien um Phospholipid-Doppelschichten handelt und dass die Comirnaty NPs zeitweise mit Phospholipid-Doppelschichten überzogen sind. In bilayerfreien Oberflächenbereichen sollten die IPC-Lipide und das Cholesterin zwangsläufig Monoschichten bilden. Auch PEG-Lipide könnten in diesen Bereichen vorhanden sein, da die LNPs bei fehlender PEG-Oberflächenbedeckung schnell verschmelzen würden. Diese Beobachtungen stehen im Einklang mit dem Fehlen eindeutiger Anzeichen für die Lipid-Doppelschicht-Hülle durch AFM-Kraftspektroskopie."
Und nun kommt ein SEHR WICHTIGER wichtiger Satz, den wir für die nächsten beiden Paper brauchen werden:
EN: “The AFM force spectroscopy data suggested that mRNA is associated with lipids within the LNP core. This led us to hypothesize that the electron-dense gritty texture of LNP cores in cryoTEM images (Figures 3A, B) reflects lipid-bound, condensed state mRNA mingled with the excess of ionizable lipids.”
DE: "Die Daten der AFM-Kraftspektroskopie deuten darauf hin, dass die mRNA mit Lipiden innerhalb des LNP-Kerns verbunden ist. Dies veranlasste uns zu der Hypothese, dass die elektronendichte, körnige Textur der LNP-Kerne in den Kryo-TEM-Bildern (Abbildungen 3A und B) lipidgebundene, kondensierte mRNA widerspiegelt, die mit einem Überschuss an ionisierbaren Lipiden vermischt ist."
Das heißt, das ALC-0315 ist NICHT in der äußeren Schicht des Lipidnanopartikels sondern im weichen inneren Kern, direkt an die modRNA gebunden. So in etwa wie die Nutella um den Nusskern in einem Ferrero Rocher. Flüssiger, innerer Kern und feste? modRNA?
Ergebnisse der Transmissionselektronenmikroskopie:
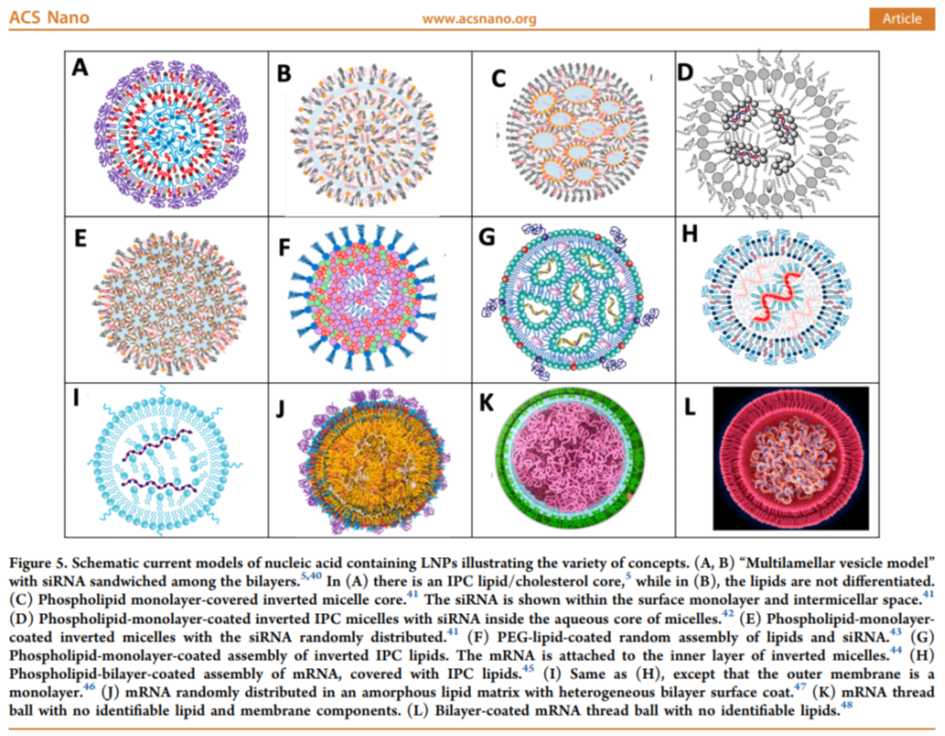
Man kommt insgesamt zu dem Schluss, dass die aktuellen LNP Modelle NICHT auf Comirnaty anwendbar sind.
In dieser Abbildung werde aktuelle Modellvorstellungen gelistet und J scheint mir persönlich der Realität von Comirnaty am nächsten zu kommen. H ist das für gewöhnlich verwendete und bekannteste Bild, aber die doppelschicht hat sich so ziemlich erledigt, wie es aussieht, außer an den Polkappen.
Die Autoren entwerfen folgende Modelle für die Plörre, die so gar nicht so hübsch übersichtlich und strukturiert aussehen, wie die mittlerweile gewohnte Modellzeichnung H. Die Realität ist deutlich unordentlicher.
Moderna hat interessanterweise eine ähnliche Hypothese zur Struktur der LNPs.
Science-Day-2022-Master-Slides-FINAL-(05.17_7am).pdf (q4cdn.com)
Sie wirklich glücklich sind die Autoren mit ihrem Modell aber selbst auch nicht:
EN: „These facts highlight the need to better understand the molecular structure of mRNA-LNPs and accordingly better visualize them in schematic models.”
DE: "Diese Fakten unterstreichen die Notwendigkeit, die molekulare Struktur von mRNA-LNPs besser zu verstehen und sie dementsprechend besser in schematischen Modellen zu visualisieren."
(*Anmerkung: IPC-Lipid = ALC-0315, das saure, kationische Lipd*)
EN: “The analytic and visual data in the present study, taken together with the mentioned size information, suggest a hypothetical model wherein a single or multiple copies of mRNA-IPC complexes densely fill up part or the whole internal space of LNPs. The IPC lipids, or self-associated IPC clusters, stabilize the tertiary structure of mRNA via intra- and interloop cross-links and bridges (Figure 6A). Cross-links may be provided by hydrogen bonds between the free =O and −OH groups of IPC lipids and the nitrogenous bases in the mRNA, while bridges may be formed from IPC clusters.”
DE: "Die analytischen und visuellen Daten in der vorliegenden Studie legen zusammen mit den erwähnten Größeninformationen ein hypothetisches Modell nahe, bei dem eine einzelne oder mehrere Kopien von mRNA-IPC-Komplexen einen Teil oder den gesamten Innenraum der LNPs dicht ausfüllen. Die IPC-Lipide oder selbst-assoziierte IPC-Cluster stabilisieren die Tertiärstruktur der mRNA über Intra- und Interloop-Querverbindungen und Brücken (Abbildung 6A). Querverbindungen können durch Wasserstoffbrücken zwischen den freien =O- und -OH-Gruppen der IPC-Lipide und den stickstoffhaltigen Basen in der mRNA entstehen, während Brücken von IPC-Clustern gebildet werden können.“
Was er damit meint, ist, dass sich das ALC-0315 wie ein Krake um die modRNA windet:
Das wird dann auch im nächsten Paper bestätigt, daher ziehe ich das Video an diese Stelle vor. Es gehört aber eigentlich zum folgenden zweiten Paper, wird aber schon in diesem Paper als Hypothese formuliert.
Man kommt in diesem Paper zu folgender Schlussfolgerung:
EN: “One insight into the nanostructure of the Comirnaty Covid-19 vaccine concerns the tertiary structure of mRNA within the LNPs and its interaction with IPC lipids. Our experimental data and theoretical considerations suggest that the highly convoluted mRNA strains are condensed in the core of NPs primarily by temperature-dependent weak inter- and intramolecular interactions, involving hydrogen bonds and, depending on the actual pH, ionic bonds with IPC lipids. However, ionic interactions between the nucleic acid and IPC lipids may be insignificant or absent at neutral pH in the vaccine’s saline diluted formulation for human use. The predominance of hydrogen bonds and lack of a continuous bilayer around the mRNA−lipid matrix offer an explanation for the soft and compliant structure of Comirnaty LNPs, as well as the vaccine’s limited stability in ambient temperature.”
DE: "Ein Einblick in die Nanostruktur des Comirnaty-Covid-19-Impfstoffs betrifft die Tertiärstruktur der mRNA innerhalb der LNPs und ihre Wechselwirkung mit IPC-Lipiden. Unsere experimentellen Daten und theoretischen Überlegungen deuten darauf hin, dass die stark gefalteten mRNA-Stämme im Kern der LNPs in erster Linie durch temperaturabhängige schwache inter- und intramolekulare Wechselwirkungen kondensiert werden, die Wasserstoffbrückenbindungen und, je nach aktuellem pH-Wert, ionische Bindungen mit den IPC-Lipiden umfassen. Die ionischen Wechselwirkungen zwischen der Nukleinsäure und den IPC-Lipiden können jedoch bei neutralem pH-Wert in der mit Kochsalzlösung verdünnten Formulierung des Impfstoffs für den menschlichen Gebrauch unbedeutend oder nicht vorhanden sein. Das Vorherrschen von Wasserstoffbrückenbindungen und das Fehlen einer kontinuierlichen Doppelschicht um die mRNA-Lipid-Matrix bieten eine Erklärung für die weiche und nachgiebige Struktur der Comirnaty-LNPs sowie für die begrenzte Stabilität des Impfstoffs bei Umgebungstemperatur."
=== 2. SAXS/PCS-Studie über die mesoskopische Struktur von Lipid-Nanopartikel (LNP)-Formulierungen für mRNA Wirkstoffabgabe: Comirnaty® und wirkstofffreie LNP Dispersionen ===
Unruh holt historisch ein wenig mehr aus als das erste Paper und gibt ein paar interessante Hintergründe zu den LNP Formulierungen allgemein, die einen gewissen Bias erkennen lassen, wenn man ehrlich ist.
(*Anmerkung: SLN=solid lipid nanoparticles, NLC= nanostructured lipid carriers)
EN: “Nevertheless, until the year 2020 SLN and NLC based formulations have, besides cosmetic and dermatological applications, not been approved for drug delivery in humans except for Onpattro® and some liposomal preparations which, however, do not obey a solid core.”
DE: "Dennoch sind bis zum Jahr 2020 SLN- und NLC-basierte Formulierungen, abgesehen von kosmetischen und dermatologischen Anwendungen, nicht für die Verabreichung von Arzneimitteln an den Menschen zugelassen, mit Ausnahme von Onpattro® und einigen liposomalen Präparaten, die jedoch nicht einem festen Kern haben."
EN: “All LNP formulations approved in the United States and the European Union before 2020 are indicated for cancer treatment, high unmet medical need, or rare, life-threatening diseases, and thus are intended for only a relatively small group of seriously ill patients.”
DE: "Alle vor 2020 in den Vereinigten Staaten und der Europäischen Union zugelassenen LNP-Formulierungen sind für die Krebsbehandlung, für einen hohen ungedeckten medizinischen Bedarf oder für seltene, lebensbedrohliche Krankheiten indiziert und daher nur für eine relativ kleine Gruppe schwer kranker Patienten bestimmt."
Im Gegensatz zum ersten Paper geben diese Autoren die verwendeten Chargen an:
Da es sich um deutsche Forscher handelt, gehe ich davon aus, dass es sich um Vials aus der deutschen Lieferkette von BioNTech handelt, während Szebeni wahrscheinlich mit Pfizer Chargen gearbeitet hat.
Beide verwendeten Batches sind unauffällig und weder bei den Tweets der Kanzlei Ulbrich gelistet noch bei Howbadismybatch. Es sind also keine der death batches/hot lots, wie man die Chargen mit hohen Nebenwirkungen gerne nennt.
Der pH schwankt insgesamt zwischen 6,7 bis 7,3. und wäre teils knapp außerhalb des zugelassenen pH-Rahmens von 6,9-7,9, der an und für sich schon sehr großzügig ist und scheints MEHRFACH unterschritten wurde. Schon das… ein Qualitätsmangel, den man beim PEI einfach hätte messen können mit pH- Teststreifen.
So schwierig ist pH einstellen nun wirklich nicht. Ich habe die Autoren des Preprints mal darauf hingewiesen in einem Kommentar.
Der pH des menschlichen Blutes liegt bei 7,4. Abweichungen in den sauren Bereich würde ich als ungesund ansehen, daher ja Basenbäder, basische Ernährung…
(https://view.officeapps.live.com/op/view.aspx?src=https%3A%2F%2Fwww.covidtruths.co.uk%2Fwp-content%2Fuploads%2F2021%2F04%2FPriority-OCs-in-quality-LoQ-COVID-19-mRNA-Vaccine-BioNTech.docx&wdOrigin=BROWSELINK)
Die Autoren des Papers haben nun auch selbst leere LNPs ohne modRNA gemischt als Vergleich. Laut Malone braucht es aber die negativ geladene modRNA, damit sich so ein Partikel überhaupt spontan zusammensetzt, wegen der negativen Ladung. An dieser Stelle bin ich ein wenig verwirrt, wie man dann überhaupt einen leeren LNP bauen kann. Bei allen Tierversuchen wurden daher bisher RNA-Dummys verwendet, genau aus diesem Grund.
Interessant auch dieser Satz:
EN: “Two different BNT-sample batches have been studied differing in lipid concentration by a factor of 5 and in the composition of the aqueous phase (salts and pH buffer).”
DE: “Es wurden zwei verschiedene Chargen von BNT-Proben untersucht, die sich in der Lipidkonzentration um den Faktor 5 und in der Zusammensetzung der wässrigen Phase (Salze und pH-Puffer) unterschieden.“
An dieser Stelle musste ich recherchieren, was es mit dem unterschiedlich farbigen Deckeln der Plörre auch sich hatte, das fehlt mir in diesem Preprint. Die Beschriftung war bei Comirnaty ja bekanntlich ein einziges Chaos und hat zu diversen Anwendungsfehlern geführt.
https://labeling.pfizer.com/ShowLabeling.aspx?id=16072
Purple cap musste verdünnt werden: https://www.hse.ie/eng/health/immunisation/hcpinfo/covid19vaccineinfo4hps/preparecomirnaty.pdf
1,8 ml NaCl zusätzlich ergab ca. 6 Dosen à 0.3 ml, also ca. 1,8 ml bis 2,1 ml + x<0,3ml…
Wieviel war in einer Vial enthalten? Wie war die Verdünnung letztendlich? Wurde um den Faktor 5 verdünnt?
An dieser Stelle bekomme ich mathematisch einen Knoten im Hirn und kann nicht wirklich nachvollziehen, wie das mit dem LNP Unterschied zwischen purple und grey cap ist, wenn ich nicht weiß, wieviel in der Vial vorgelegt war.
Das Endvolumen kann max. 2,2 ml gewesen sein, sonst hätte man auch 8 Portionen ziehen können.
2,2ml-1,8ml= 0,4ml
2,2ml/0,4ml=Faktor 5,5
Damit scheint mir der Unterschied zwischen den gray und purple cap Vials nun nicht so wirklich groß zu sein und die Verdünnung den angesprochenen Faktor 5 in den LNPs zu entsprechen. Teilt man die Werte des purple cap durch 5 kommt man ziemlich exakt auf die Werte des grey cap. Ich bin beeindruckt, BioNTech hat das perfekt hinbekommen. Das muss man ihnen zugestehen.
EN: “The deviation of the observed mass fraction of sample BNT412 by about 34 % from the expected value is, however, most probably linked to the significantly less stable dispersive state of the LNPs in the ready to use gray cap in comparison to the very stable LNPs in the concentrated violet cap Comirnaty formulations. For these gray cap Comirnaty dispersions, the particle density is by a factor 5 smaller compared to the violet cap Comirnaty formulations.
In contrast to the violet cap BNT-samples which can be studied by SAXS continuously for 12 h and even after a 1 month of storage without notable changes of the collected pattern, the SAXS data collected from gray cap BNT-samples exhibit continuous temporal changes of their SAXS patterns within 8 h and beyond independent of X-ray irradiation.”
DE: "Die Abweichung des beobachteten Massenanteils der Probe BNT412 um etwa 34 % vom erwarteten Wert hängt jedoch höchstwahrscheinlich mit dem deutlich weniger stabilen Dispersionszustand der LNPs in der gebrauchsfertigen grauen Kappe im Vergleich zu den sehr stabilen LNPs in den konzentrierten violetten Kappen-Comirnaty-Formulierungen zusammen. Die Partikeldichte dieser Gray-Cap-Comirnaty-Dispersionen ist um den Faktor 5 geringer als die der Violet-Cap-Comirnaty-Formulierungen.
Im Gegensatz zu den BNT-Proben mit violetter Kappe, die mittels SAXS kontinuierlich für 12 Stunden und sogar nach einem Monat Lagerung ohne nennenswerte Veränderungen des gesammelten Musters untersucht werden können, zeigen die SAXS-Daten, die von BNT-Proben mit grauer Kappe gesammelt wurden, kontinuierliche zeitliche Veränderungen ihrer SAXS-Muster innerhalb von 8 Stunden und darüber hinaus, unabhängig von der Röntgenbestrahlung."
Natürlich ist die Partikeldichte dünner, in der grauen Formulierung, die ist ja schon verdünnt!
Die Experimentatoren hätten somit, um wirklich vergleichen zu können, die purple cap suspension entsprechend der Anweisungen verdünnen müssen!
Interessant wäre es, die purple cap Inhalte einmal mit NaCl und einmal mit Tris zu verdünnen, und den Unterschied zu dokumentieren. Zusätzlich sollte man eine Steulichtmessung der unverdünnten und verdünnten purple cap Inhalte und grey cap Lösungen über mehrere Tage durchführen, um die Stabilität zu messen, das hatte Szebeni vergessen zu überprüfen. Streulichtmessung müsste man auch mit den aktuellen Produkten machen, um zu prüfen, ob sie wirklich 10 Wochen im Kühlschrank haltbar sind, wie behauptet wird.
Andererseits war das ja nicht ihr Ziel, sie wollten nur die Struktur klären und nicht die Stabilität untersuchen. Sie haben letztendlich gezeigt, dass die ready to use Mischung in den gray cap vials trotz Tris Puffer immer noch instabiler war, als die konzentrierte Plörre in den purple caps vor Verdünnung.
Damit sind die beiden Produkte nicht wirklich vergleichbar und das sieht nicht wirklich nach GMP aus. Würde ich mal vorsichtig sagen.
Bei den anschließenden experimentellen Ausführungen und Messungen steige ich aus. Ich habe damit nie gearbeitet, kenne die Messwerte nicht, die erhoben werden, und kann daher nur vertrauen, dass da sauber gearbeitet wurde.
So stellen sich die Autoren dieses Papers jedoch die BioNTech-Plörre-LNPs vor:
EN: “ALC-0315 forms the main component of the LNP cores and was found (by SAXS and 1HNMR spec troscopy) to be in an amorphous viscous but essentially liquid aggregate state. However, cholesterol seems to be located in immobilized local environments within the LNP core and the stabilizing shell, respectively. Highly mobile ALC-0159 PEG-chains were detected indicating their lo cation in the outermost, dispersion medium rich, ∼4 nm thick stabilizing shell of the LNPs. […] The LNP cores were found to consist of […] 74 w% ALC-0315, 22 w% cholesterol, and 4 w% mRNA for Comirnaty® formulations. […] the observed number of LNPs in Comirnaty® formulations is very close to the total number of mRNA molecules of 2.19 · 1014 per ml dispersion as specified by BioNTech […] The observed internal structure of the LNP cores implies an average core diameter of ∼42 nm (55 nm total particle diameter).”
DE: "ALC-0315 bildet den Hauptbestandteil der LNP-Kerne und befindet sich (mittels SAXS und 1HNMR-Spektroskopie) in einem amorphen, zähflüssigen, aber im Wesentlichen flüssigen Aggregatzustand. Das Cholesterin scheint sich jedoch in immobilisierten lokalen Umgebungen innerhalb des LNP-Kerns bzw. der stabilisierenden Hülle zu befinden. Es wurden hochmobile ALC-0159 PEG-Ketten nachgewiesen, was darauf hindeutet, dass sich das Cholesterin in der äußersten, an Dispersionsmittel reichen, ∼4 nm dicken stabilisierenden Schale der LNPs befindet. [...] Es wurde festgestellt, dass die LNP-Kerne aus [...] 74 w% ALC-0315, 22 w% Cholesterin und 4 w% mRNA für die Comirnaty®-Formulierungen bestehen. [...] die beobachtete Anzahl der LNPs in den Comirnaty®-Formulierungen liegt sehr nahe an der von BioNTech angegebenen Gesamtzahl der mRNA-Moleküle von 2,19 - 1014 pro ml Dispersion [...] Die beobachtete innere Struktur der LNP-Kerne impliziert einen durchschnittlichen Kerndurchmesser von ∼42 nm (55 nm Gesamtpartikeldurchmesser)."
Also in etwa so wie Szebeni, nur mit anderen Methoden bestätigt.
===3. Ein neuer Mechanismus für den Verlust der mRNA-Aktivität in Lipid-Nanopartikelsystemen ===
Wie haben aus den ersten beiden Papern gelernt, dass das kationische Lipid ALC-0315 flüssig im Kern der Plörre vorliegt und sich wohl kuschelig wie ein Krake um die modRNA windet.
Warum auch immer das Moderna LNP nicht parallel behandelt und vermessen wurde, verstehe ich an dieser Stelle nicht.
Nun gibt es leider ein kleines, weiteres Problem, das BioNTech nicht überprüft und kontrolliert hat (neben der Stabilität der LNPs in den Vials mit der grauen Kappe und dem pH (siehe Paper 2)).
EN: “Herein we report the discovery, characterization, and identification of another class of mRNA reactivity that leads to loss in activity: the formation of lipid-mRNA adducts through the covalent addition of reactive lipid species to the nucleobase. Importantly, as many lipid-based nucleic acid formulations share common chemical functionalities, particularly those that use an ionizable amino-lipid, mechanisms identified in this study are broadly applicable. These data can inform manufacturing protocols to limit the formation of lipid-mRNA adducts and ensure the high quality of nucleic acid-based products.”
DE: "Hierin berichten wir über die Entdeckung, Charakterisierung und Identifizierung einer anderen Klasse von mRNA-Reaktivität, die zu einem Aktivitätsverlust führt: die Bildung von Lipid-mRNA-Addukten durch die kovalente Addition reaktiver Lipidspezies an die Nukleobase. Da viele Nukleinsäureformulierungen auf Lipidbasis gemeinsame chemische Funktionalitäten aufweisen, insbesondere solche, die ein ionisierbares Aminolipid verwenden, sind die in dieser Studie identifizierten Mechanismen allgemein anwendbar. Diese Daten können als Grundlage für Herstellungsprotokolle dienen, um die Bildung von Lipid-mRNA-Addukten zu begrenzen und die hohe Qualität von Produkten auf Nukleinsäurebasis zu gewährleisten."
Im Klartext: Die kationischen-Lipide, die sich laut den beiden zuerst behandelten Publikationen, in flüssiger Form, im Inneren der Plörre befinden und sich um die modRNA winden, mutieren diese, so dass diese ihre Aktivität verlieren kann bzw. halt mutiert. Noch eine Möglichkeit für fehlgefaltetes Protein, als wenn wir davon nicht schon genug hätten. Etwas, das man bei der Produktion beachten und prüfen hätte müssen.
Das Paper exerziert anschließend im experimentellen Detail, wie man das überprüfen kann mittels HPLC!!! Und zwar um genau zu sein: reversed phase-ion pair high performance liquid chromatography (RP-IP HPLC).
Die Sache hat jedoch einen Haken, wie Irena Vlatkovic in ihrem Review so schön geschrieben hat:
Vlatkovic I. Non-Immunotherapy Application of LNP-mRNA: Maximizing Efficacy and Safety. Biomedicines. 2021 May 10;9(5):530. doi: 10.3390/biomedicines9050530. PMID: 34068715; PMCID: PMC8151051. https://pubmed.ncbi.nlm.nih.gov/34068715/
EN: “For example, ion pair reversed-phase high-performance liquid chromatography (HPLC) is still considered as a gold standard method for the depletion of unwanted byproducts/contaminants from mRNA of interest. Unfortunately, HPLC is difficult to scale up for the manufacture of large amounts of mRNA and would lead to the production of high amounts of hazardous waste [17]. Therefore, cellulose chromatography was recently developed [17]. This method showed a great efficiency in the depletion of dsRNA contaminants and the production of mRNAs with high purity and low immune activation potential.”
DE: "So gilt beispielsweise die Ionenpaar-Umkehrphasen-Hochleistungsflüssigkeitschromatographie (HPLC) nach wie vor als Goldstandard-Methode für die Entfernung unerwünschter Nebenprodukte/Verunreinigungen aus der mRNA von Interesse. Leider lässt sich die HPLC für die Herstellung großer Mengen mRNA nur schwer skalieren und würde zu großen Mengen an gefährlichem Abfall führen [17]. Daher wurde kürzlich die Cellulose-Chromatographie entwickelt [17]. Diese Methode zeigte eine große Effizienz bei der Abreicherung von dsRNA-Verunreinigungen und der Herstellung von mRNAs mit hoher Reinheit und geringem Immunaktivierungspotenzial."
Referenz 17:
Baiersdörfer M, Boros G, Muramatsu H, Mahiny A, Vlatkovic I, Sahin U, Karikó K. A Facile Method for the Removal of dsRNA Contaminant from In Vitro-Transcribed mRNA. Mol Ther Nucleic Acids. 2019 Apr 15;15:26-35. doi: 10.1016/j.omtn.2019.02.018. Epub 2019 Feb 27. PMID: 30933724; PMCID: PMC6444222. https://pubmed.ncbi.nlm.nih.gov/30933724/
Vergleichen wir doch noch einmal, was Packer als essentiell ansieht, um zu kontrollieren, ob das ALC-0315 oder das SM-102 einem die modRNA zu sehr mutiert hat:
reversed phase-ion pair high performance liquid chromatography (RP-IP HPLC)
Was wäre gold Standard gewesen laut Irena V., um modRNA zu reinigen:
ion pair reversed-phase high-performance liquid chromatography
Was hat man aus Kosten- und Umweltschutzgründen gemacht?
Cellulose-Chromatographie
NATÜRLICH hat man diese umweltschädliche Chromatographie nicht zur Qualitätskontrolle eingesetzt! Man hat sie ja nicht einmal in der Produktion eingesetzt wo es essentiell gewesen wäre. Warum sollte man sie dann im QS/QM-Bereich einsetzen? Das hätte zu unnötigem toxischem Abfall geführt und so ein wenig kaputte modRNA, wenn kümmert das, wo doch ohnehin deutlich überdosiert wurde, da bleibt schon noch genug übrig!
Was wurde denn alles mutiert vom kationischen Lipid?
EN: “[…] similar characteristic neutral mass losses of 132.03 were observed for lipid modifications across all 4 nucleobases.”
DE: “[...] ähnliche charakteristische neutrale Massenverluste von 132,03 wurden für Lipidmodifikationen über alle 4 Nukleobasen hinweg beobachtet."
Alle 4 Nucleotide sind von dieser Art chemischer Mutagenese betroffen! Bei den chemischen Details, die im Paper erklärt werden, bin ich aber definitiv raus mit meinen Einführungsvorlesungen Anorganische Chemie und Organische Chemie für Naturwissenschaftler in den späten 1990er Jahren.
Man kommt in Paper 3 zu dem vernichtenden Schluss:
EN: “Herein we report identification of a lipid-modified class of mRNA impurities generated by electrophilic degradants and impurities originating in the ionizable lipid; these impurities disrupt mRNA translation and negatively impact the activity of LNP-formulated mRNA products. […] This represents a gap in quality control of mRNA-LNPs during manufacturing, particularly as it pertains to consistency and activity of the resultant drug product.[…] The pathway reported herein identifies an important class of impurities that may be present in all lipid-based mRNA systems.”
DE: "Hierin berichten wir über die Identifizierung einer Lipid-modifizierten Klasse von mRNA-Verunreinigungen, die durch elektrophile Abbauprodukte und Verunreinigungen aus dem ionisierbaren Lipid entstehen; diese Verunreinigungen stören die mRNA-Translation und wirken sich negativ auf die Aktivität von LNP-formulierten mRNA-Produkten aus. [...] Dies stellt eine Lücke in der Qualitätskontrolle von mRNA-LNPs während der Herstellung dar, insbesondere in Bezug auf die Konsistenz und Aktivität des resultierenden Arzneimittels. [...] Der hier beschriebene Weg identifiziert eine wichtige Klasse von Verunreinigungen, die in allen lipidbasierten mRNA-Systemen vorhanden sein können."
Lustiger Weise könnten wir es im Falle von durch kationischen Nanolipiden mutierten modRNAs bzw. mmodRNAs oder mmmRNAs zu tun haben: mutierte, modifierte, mRNA.
An dieser Stelle frage ich mich auch, wenn das kationische Lipid mRNA chemisch mutiert, wie sieht es dann in der Zelle aus?
Das kationische Lipid ist, so wie es aussieht, an die modRNA gebunden und wird somit ins Zytosol der Zelle gelangen. Wird es auch dort (m)RNAs mutieren? Kann es auch DNAs chemisch mutieren? Ist das kationische Lipid somit ein chemisches Mutagen? DAS wäre echt unschön, weil wir uns damit NOCH EIN PROBLEM eingehandelt hätten, das Krebs verursachen kann. Wenn das kationische Lipid DNA im Zellkern mutieren könnte oder RNA im Zytosol, klingt das nicht sonderlich gesundheitsförderlich.
Könnte mir BionTech/Pfizer oder Moderna bitte diese Frage beantworten? Haben sie das geprüft? Wenn ja, was kam dabei raus und wenn nein, warum haben sie das nicht untersucht?
Dieses dritte Paper ist sehr chemisch. Ich habe nur die Grundvorlesungen Anorganische und Organische Chemie im Grundstudium irgendwie bestanden. Maria Guchi geht in ihrem Substack deutlich tiefer in die chemischen Details und die daraus resultierenden Probleme.
Christie erklärt das Paper einfacher als Maria Gutschi:
Maria Gutschi hat aber auch einen schönen Substack zur LNP Struktur, bei dem sie etwas andere Schwerpunkte setzt als ich.
=== 4. Analyse der In-Use-Stabilität der mRNA-LNP-COVID-19-Impfstoffe Comirnaty™ (Pfizer) und Spikevax™ (Moderna): Eine vergleichende Studie des Partikels ===
Am 25 Oktober 2023 erschien noch ein Paper, welches die Stabilität und Größe der LNP Partikel untersuchte.
Hermosilla J, Alonso-García A, Salmerón-García A, Cabeza-Barrera J, Medina-Castillo AL, Pérez-Robles R, Navas N. Analysing the In-Use Stability of mRNA-LNP COVID-19 Vaccines Comirnaty™ (Pfizer) and Spikevax™ (Moderna): A Comparative Study of the Particulate. Vaccines (Basel). 2023 Oct 25;11(11):1635. doi: 10.3390/vaccines11111635. PMID: 38005967; PMCID: PMC10675537. https://pubmed.ncbi.nlm.nih.gov/38005967/
Für die Untersuchung verwendet wurden die folgenden Chargen:
Die experimentelle Vorgehensweise der Untersuchungen war wie folgt (direkt übersetzt).
Die abgelaufenen klinischen Comirnaty™- und Spikevax™-Proben wurden verschiedenen Stressbedingungen unterworfen:
(i) in transparente 2-mL-Glasfläschchen gefüllt und 24 Stunden lang in einer Alterungskammer (Solarbox 3000e RH, Cofomegra, Mailand, Italien) einer beschleunigten künstlichen Lichtbestrahlung (250 W/m2) ausgesetzt,
(ii) in klare 2-mL-Glasfläschchen gefüllt und 24 Stunden lang bei Raumtemperatur (RT) natürlichem Licht ausgesetzt,
(iii) mechanischer Belastung ausgesetzt, indem mehrere wiederholte Injektionen (1 und 3) bei 300 l/s unter Verwendung der Spritzen und der 18-G-Nadeln wie oben angegeben durchgeführt wurden,
(iv) mechanischer Belastung ausgesetzt, indem die Proben 10 s lang manuell kräftig geschüttelt wurden, und
(v) mechanischer Belastung ausgesetzt, indem die Proben 10 s lang durch Vortex bei 2400 U/min vibriert wurden.
Die noch nicht abgelaufenen Comirnaty™- und Spikevax™-Proben wurden den folgenden Bedingungen ausgesetzt folgenden Stressbedingungen ausgesetzt:
(i) mechanischer Stress, indem die Proben manuell Schütteln der Proben für 10 s und
(ii) mechanische Beanspruchung durch Vibration der Proben Vibration durch Vortex bei 2400 U/min für 10 s.
Diese Studie wurde in dreifacher Ausführung durchgeführt, wobei sowohl mit den nicht abgelaufenen als auch mit den abgelaufenen Comirnaty™- und Spikevax™-Proben.
Aufgrund der Entscheidung des Krankenhauses, die Verwendung von Spikevax™ einzustellen, wurde die Stabilität für 24 h nur mit Comirnaty™-Proben durchgeführt. Anschließend wurden Einzeldosen von 300 l nicht abgelaufener Comirnaty™-Dispersionen wie folgt gelagert:
(i) in 1-mL-Spritzen und gekühlt bei 2-8 °C, geschützt vor Tageslicht,
(ii) in 1-mL-Spritzen und bei Raumtemperatur (RT) mit Klimaanlage (20 °C), nicht geschützt vor Tageslicht,
(iii) in in 1-mL-Spritzen und Lagerung bei RT ohne Klimatisierung (thermische Exkursion 18-35 C), nicht geschützt vor Tageslicht,
(iv) in 1-mL-Spritzen und Lagerung bei 20 C, geschützt vor und
(v) in den Original-Impfstoff-Glasfläschchen, gekühlt bei 2-8 °C und vor Tageslicht geschützt gelagert. Diese Studie wurde in doppelter Ausführung durchgeführt.
Für die Analyse wurden die gleichen Methoden verwendet, die oben bereits beschrieben wurden, als DLS = dynamic light scattering und TEM = Transmissionselektronenmikroskopie. Die Daten sind somit mit den anderen Publikationen vergleichbar aufgrund der gleichen Methodik.
Abbildung 1. Größenverteilungsdiagramme nach Volumen von mehreren repräsentativen Comirnaty™-Proben aus (A) nicht abgelaufenen und (B) abgelaufenen Fläschchen.
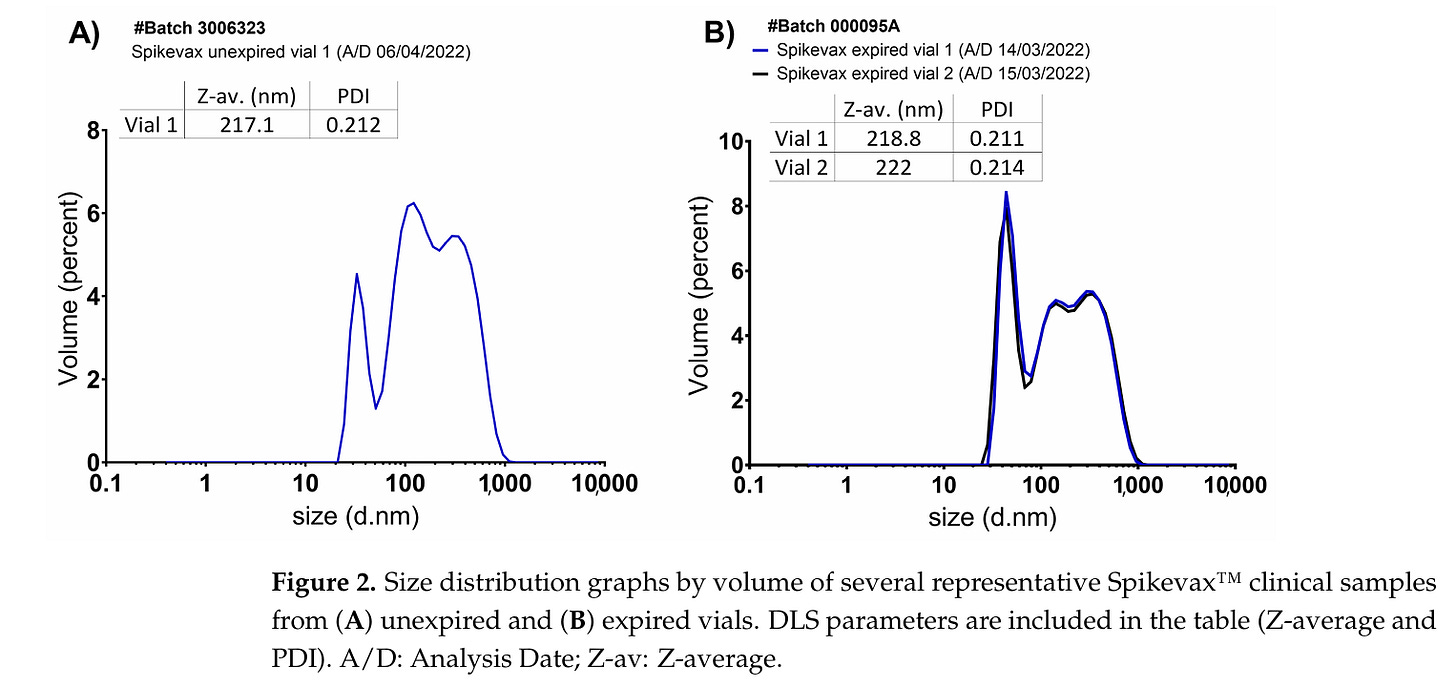
Abbildung 2. Größenverteilungsdiagramme nach Volumen von mehreren repräsentativen klinischen Spikevax™-Proben aus (A) nicht abgelaufenen und (B) abgelaufenen Fläschchen
Man sieht im direkten Vergleich, dass die Größen der LNP-Partikel von BioNTech/Pfizer und Moderna sich DEUTLICH utnescheiden. Die LNPs von Moderna haben eine deutlich variablere Größenverteilung, das hat BioNTech/Pfizer schon deutlich besser hinbekommen. Dort sieht man aber, dass es nach dem Ablaufdatum zu klumpen beginnt und die LNPs miteinander verschmelzen.
Abbildung 3. Repräsentative Größenverteilungsdiagramme nach Volumen verschiedener Comirnaty™-Proben, die manuell geschüttelt und durch Vortex vibriert wurden (A), und abgelaufener Proben, die künstlichem Lichtstress (B), manuellem Schütteln und Vibrieren durch Vortex (C) sowie 1 und 3 wiederholten Zyklen von Injektionen mit Spritzen (D) ausgesetzt waren. A/D: Datum der Analyse.
Abbildung 4. Repräsentative Größenverteilungsdiagramme nach Volumen von nicht abgelaufenen Spikevax™-Proben, die manuellem Schütteln und Vibration durch Vortex (A) ausgesetzt wurden, und abgelaufenen Proben, die künstlicher Lichtstress (B), manuellem Schütteln und Vibration durch Vortex (C) und 1 und 3 wiederholten Zyklen von Injektionen mit Spritzen (D). A/D: Datum der Analyse.
Man sieht, schütten und Vibration sind dem Produkt nicht zuträglich, aber es wird nicht ausreichend zerstört, dass kein Schaden mehr durch Transfektion auftreten würde. Einiges an LNPs scheint zu flokkulieren, bei Moderna deutlich stärker als bei BioNTech/Pfizer, aber es dürfte noch genug über sein, um Schaden anzurichten. Richtig kaputt ist das Produkt nach Schütteln oder einem French Press Effekt durch das drücken durch Kanülen nicht. Ob das gute oder schlechte Nachrichten sind, lasse ich mal dahingestellt.
Abbildung 5. Repräsentative Größenverteilungsdiagramme nach Volumen von klinischen Comirnaty™-Proben am Tag 0 (ungeöffnete Kontrolle) und nach Lagerung unter verschiedenen klinischen Bedingungen für 24 h. RT: Raumtemperatur; AC: Klimaanlage.
Auch Raumtemperatur scheint dem Produkt (leider) nicht viel anhaben zu können.
Abbildung 6. Repräsentative Comirnaty-LNPs aus einer einzelnen, nicht gealterten Kontrollprobe: mikroskopische Aufnahmen aufgenommen in verschiedenen Amplifikationsstufen und Positionen.
Abbildung 7. Repräsentative TEM-Bilder von (A) einer nicht abgelaufenen Comirnaty™-Probe (Kontrolle) am Tag 0 der Herstellung, (B) abgelaufener Comirnaty™-Probe, (C) nicht abgelaufener Comirnaty™-Probe, die manuellem Schütteln, (D) Probe C, die 30 Tage lang bei 2-8 °C gealtert wurde, und (E) nicht abgelaufene Comirnaty™-Probe die einer Vortex-Vibration unterzogen wurde.
Im Elektronenmikroskop hingegen sieht es so aus, als wenn abgelaufene Chargen BioNTech/Pfizer Plörre tatsächlich nicht mehr so gut gewesen sein können, schütteln dem Produkt nicht gut tun würde (was gute Nachrichten wären). Kaum ein Arzt wird das BioNTech/Pfizer Zeug gevortext haben, was es so gar nicht gut verträgt.
Abbildung 8. Repräsentative TEM-Bilder von (A) abgelaufener Spikevax™-Kontrollprobe, (B) abgelaufener Spikevax™-Probe, die manuell geschüttelt wurde, und (C,D) verfallener Spikevax™-Probe, die einer Vortex-Vibration
Modernas Plörre scheint noch instabiler zu sein als die von BioNTech/Pfizer, dafür ist aber mehr modRNA enthalten.
Das Fazit der Autoren:
“Wir zeigen bemerkenswerte Stabilitätsdaten für Comirnaty™ (Pfizer-BioNTech) und Spikevax™ (Moderna) COVID-19-Impfstoffe nach Zubereitung/Lagerung und Belastungstest. Obwohl beide Produkte auf der gleichen mRNA-LNP-Technologie basieren, zeigen die hier vorgestellten Ergebnisse, dass sie sich durch unterschiedliche Partikelgrößenprofile auszeichnen, ebenso wie durch ihr Verhalten gegenüber den verschiedenen Handhabungs-/Belastungsbedingungen. Comirnaty™ erwies sich als besonders empfindlich gegenüber mechanischen Belastungen und Gefrier-/Auftauzyklen von 20 °C bis Raumtemperatur, weniger empfindlich gegenüber Injektionszyklen und überhaupt nicht empfindlich gegenüber Lichteinwirkung. Andererseits erwiesen sich die Spikevax™-Proben unter den meisten der getesteten Belastungsbedingungen hinsichtlich der DLS-Parameter als stabil, obwohl insbesondere bei den mechanisch belasteten Proben Veränderungen der Größenverteilungsprofile beobachtet wurden. “
Mein Fazit:
Das Dreckzeug ist leider stabiler, als ich gehofft hatte. Ich hatte gehofft, dass die Plörre in heißen Impfzentren im Sommer stark geschädigt würde und die Impflinge somit vielleicht glimpflicher davongekommen sein könnten. Ich schätze, diese Hoffnung muss ich begraben. Das Dreckzeug von BioNTech/Pfizer und Moderna ist zäher als gedacht. Mist aber auch.
Update:
15.05.2024 4. Analyse der In-Use-Stabilität der mRNA-LNP-COVID-19-Impfstoffe Comirnaty™ (Pfizer) und Spikevax™ (Moderna): Eine vergleichende Studie des Partikels































I made a probe of translation for the videos. Please forgive the mistakes, I am not a chemist !Dr Tobias Unruh presents himselfMy name is Tobias and I love numbers. Small numbers, large numbers, short and long numbers. And very precise numbers.I compose Comparisons and Formulas with which you can check Theories and see if they are right. If they do more numbers come out, on which you can rely.Since shortly I have some doubt and that scares me. You should get basic rights back when the doubling time is more than 10 days. Then with a value of 35, not yet.The R-value must then be under 1. then the 7 day incidence under 50 , or under 100, or under 10 ?And these values come from us, from scientists. And that scares me.Dear government, stop the number chaos and fix a number. then I will feel safe again. Close the schools and universities forever and then no one will contradict you. That gives security. And you people, follow the instructions of the government.Thanks.
Part 1 (which is the third video)In this video we will look at the new corona vaccines, and what they have to do with soap. The vaccines are based on the modRNA system, which delivers the message, and this modRNA is packed inside lipid nanoparticles. Recently we have come to know how these molecules are built, through the research of prof Tobias Unruh from the Erlangen University Nuernberg. There is a link underneath the videoSo what did they find? I tried to sketch the rough structure of the molecule - there is a center, nucleus, that we have to imagine not as being hard, solid, but more like an oil drop, with different ingredients that we will see later. The nucleus has a diameter of 40 nanometer. Here it says LNP lipid nanoparticle center. Different methods (small angle X-ray scattering e.a.)make it possible to find a shell of about 2 nanometer and a further shell of about 4 nanometer. The 2 nanometer shell is free of water and is lipophyl - oil loving and water resistant. The reason for this are these hydrocarbon chains which is also typical for soaps. A classic soap is a long chain of hydrocarbon with a carboxylic acid group which acts like an ester here. We hydrolyze this and then the Sodium salt of this, is a classic soap.With the letters DSCP a molecule with a very polar head group and very un-polar rest chain. This reacts very well with water (hydrophyl). As a total the molecule is neutral but we do have 2 ionen and one cation, Ammonium cation and a phosphate anion. The chains like tolayer and like with other soaps we have here head groups that interact with water. Water will stay away from this lower part, but is very receptive of the top part. DSCP and ALC0159 could be used as tenside, wash active bond, they would be too expensive, they are a bit more complex. We can thus imagine, with here the DSCP and here the ALC0159 which want to layer with their long chains ; inbetween there are these (steroid) better known as cholesterol, in fact cholesterine, and these 3 molecules form the 2 nanometer shell. They are in contact with the inside, the oil drop, containing the mRNA, ALC315 and cholesterol. The ALC0159 has here on the side a very long side chain, here is NN=45 (oxygen and 2 CH2 groups) appears about 50 times so, very long, and in contact with water, which means it can make water bridges - this is a polyethylen glycol side chain with a thickness of 4 nanometer. What now with that soap? When you clean oil with soap, you will also have a central oily part, and then the lipophyle side chains, and on the outside the water-loving part, which makes the soap water soluble. How many molecules do we have here?In the center we have the modified RNA at a rate of 30 microgramALC315 430 microgramfrom the amount you can tell that this is the most important molecule190 microgram cholesteroland although only on the outside, ALC0159 50 microgramDSCP phospholipid 90 microgramVery interesting is that the ALC315 is the only agent that really wraps around the modRNA What the interaction is between all these ingredients we will see in part 2 We have water on the outside, then a layer of water-free and also the inside is almost completely water-free. Except for the water molecule in the polar MRNA The interacting in the molecule mix we will see in next video.
Part 2in this second part of the chemistry of medicines we discuss again the new developed anti-covid products based on modRNA technics. In the first part we saw the rough structure of the nano particles which make up the larger part of the vaccines. We know the detail from the work of prof Tobias. so what have we seen in the former hour - we have a nucleus (Kern, center) nano particle from about 40 nanometer, maybe a bit larger. Inside is the modRNA, carrying the genetic information and this modRNA is packed in a molecule ALC315. There is also some cholesterol. We should imagine this center according to prof Unru as being fluid. We have an inside shell, 2 nanometer, lipophile, and an outside shell, 4 nanometer in diameter, hydrophile. Which molecules are responsible for these shells was also discussed in a former video. Now we will look at the molecular interactions with the modRNA. We have an RNA molecule - a very long chain with phosphate groups lined up on the nucleotide. Hier are the 4 classic nucleotide but with the modified RNA comes here another nucleotide namely the nmethyl pseudouridin (for this addition the nobel prize was given) it changes the characteristics. It changes the stability. This will also be caused by the fact that normally we have here a Hydrolyse sensitive No Acetal but here it is a clean ETgroup which is of course more stable.The length of the string is about 4500 nucleotide. This very long string can fold up because of the interaction between the molecules, hydrogen bonds. De molecule also carries always some Hydratwater. How can this now fit into this lipophile center? for this the ALC315 is responsible. This is describes as a cationish lipid (which it is not, but it is very little short of being a cationish lipid and we could easily make it that)The tertiair amine here at this spot should only be protonized. Then we get an Ammoniumsalt and when we get the water out we have Ammonium Hydroxid.We can compare this molecule with an octopus - in the center is the tertiair amin, then the ammonium salt, which will bind electrostatically to the phosphate groupsof the backbone of the molecule, and here a relative strong hydrogene re-bond. Here we have a tentacle with a OH group, which is also polar and can re-bond with H. and will associate with one of the polar groups here. Further we have also Ester functions on the longer pieces of the 'tentacle' ; these are dipole, hydrogen bonds acceptors and they will orientate them along the polar groups.So here is the octopus - the snout bites into the phosphate backbone, the polar groups act like suction cups on the T tentacles, not as strong as the NH bridge,but they still will hook themselves reversible somewhere. Then we still have these lipophile pieces on the tentacles, which should really not be this close to the polar groups. They should go towards the outside. Now imagine how many of these ALC315 molecules are available, 430 microgram of ALC315 and only 30 of the modRNA, so everywhere these molecules associate and cover the modRNA with their lipophile tentacles outwards - so inside hydrophyl and outside lipophyl. This fits with the lipophyle cholesterol which sits in the center of the molecule also.to recap - the modRNA enclosed in the outwards oriented lipophyle ALC315, the inside shell which is outwards hydrophyl and inwards lipophyl and this whole system is then water soluble.thanks for watching
looks like a total mess. Not a chemist, but your summary of the articles does not sound good for all those injected with these unknown products. Thank you for sharing