Das Spike-Protein und LNPs aktivieren das Komplementsystems
Das Komplement als mögliche Ursache von Impfschäden und Sheddingsymptomatik?
Ich glaube, wir müssen dringend über das Komplementsystem reden.
Wie kann es sein, dass bisher fast jeder Arzt und Wissenschaftler das Komplementsystem bei Impfschäden ignoriert hat?
Neu war das nicht. Das war ein bekanntes, ungelöstes Problem der Technologie und da ist das Spike-Protein noch nicht einmal mit dabei:
Fazit und Kurzversion für Eilige:
Sowohl LNPs als auch das Spike-Protein aktivieren den alternativen Weg des Komplementsystems.
10% des Komplementsystems sitzen in den Schleimhäuten und können für die als Sheddingsymptomatik beschriebenen Symptome bei Ungeimpften verantwortlich sein. Es gibt dabei eine genetische Komponente, weswegen nur “wenige” Menschen davon betroffen sind.
Einige der Impfschäden (z. Bsp. Lymphozyten-Amok) könnten durch das Komplementsystem verursacht sein.
Einige der Nebenwirkungen der modRNA könnten durch das Komplementsystem verursacht sein.
Die Ärzte sollten somit bei Impfgeschädigten auch prüfen, ob das Komplementsystem aktiv ist und dieses, wenn notwendig, runterfahren.
Möglicherweise ist Diät/Fasten eine Option.3
1. Was ist das Komplementsystem?
Die Grundlagen dieses Artikels stammen aus dem Janeway Immunologie 9. Auflage. Kapitel 2.2.
Ein wenig stammt auch aus
Schröder-Braunstein, J., & Kirschfink, M. (2020). Das Komplementsystem: von den Grundlagen zur klinischen Bedeutung. Transfusionsmedizin, 10(02), 75–88. https://doi.org/10.1055/a-0997-4456 (https://www.thieme-connect.com/products/ejournals/abstract/10.1055/a-0997-4456)
Ich referenzier nicht jedes einzelne Zitat, das wird zu unübersichtlich. Direkte Zitate aus den oben genannten Texten sind kursiv, was von mir ergänzt oder abgeändert wurde, ist normal geschrieben.
1.1 Das Komplementsystem und die angeborene Immunität
Wenn ein Krankheitserreger die Epithelbarrieren und erste antimikrobielle Abwehrmechanismen des Körpers überwunden hat, trifft er als nächstes auf eine Hauptkomponente der angeborenen Immunität, die man als Komplementsystem bezeichnet. Dabei handelt es sich um eine Reihe löslicher Proteine, die im Blut und in anderen Körperflüssigkeiten vor kommen.
ABER 10 % der Komplementmenge sind auch in den Schleimhäuten zu finden, da kann auch eine Aktivierung stattfinden.4 Das Komplement ist somit nicht nur im Körperinneren zu finden. Es ist auch Teil der angeborenen, passiven Immunantwort in den Schleimhäuten, also Teil der ersten Verteidigungslinie.
Das Komplementsystem ist ein hochkonservierter Teil des angeborenen Immunsystems. Mehr als 50 lösliche und membrangebundene Proteine bilden ein ausgeklügeltes Netzwerk aus löslichen, zelloberflächenassoziierten und intrazellulären Proteinen, die als Mustererkennungsmoleküle, Proteasen, Regulatoren und Signalrezeptoren fungieren und gemeinsam einen wichtigen Beitrag zur Immunüberwachung und Gewebehomöostase des Körpers leisten.
Wenn keine Infektion vorliegt, zirkulieren diese Proteine in einer inaktiven Form. Bei Anwesenheit von Krankheitserregern oder an Krankheitserreger gebundenen Antikörpern wird das Komplement „aktiviert“. Bestimmte Komplementproteine treten miteinander in Wechselwirkung und bilden verschiedene Reaktionswege der Komplementaktivierung aus, wobei alle dasselbe Ziel haben – das Abtöten der Krankheitserreger, entweder direkt durch Erleichtern der Phagocytose oder durch Auslösen von Entzündungsreaktionen, die das Bekämpfen der Infektion unterstützen.
Die wichtigste Aufgabe des Komplements ist, die Aufnahme und Zerstörung von Pathogenen durch phagocytotische Zellen zu erleichtern.
Es gibt drei Wege der Komplementaktivierung:
Der klassische Weg wird von Antikörpern aktiviert.
der alternative Weg ist wahrscheinlich der älteste aller Aktivierungswege des Komplements. Seine wichtigste Eigenschaft besteht darin, dass er spontan aktiviert werden kann. Der alternative Weg kann von von Krankheitserregern direkt aktiviert werden. Der alternative Weg wird sowohl vom Spike-Protein als auch von Lipidnanopartikeln aktiviert.
der Lektinweg wird von Proteinen des Lektintyps aktiviert, die Kohlenhydrate an der Oberfläche von Krankheitserregen erkennen und daran binden.
Das Komplementsystem kann jedoch auch von absterbenden Zellen aktiviert werden, etwa bei Schädigungen aufgrund von Sauerstoffmangel, aber auch durch Zellen, die eine Apoptose (den programmierten Zelltod) durchlaufen. In diesen Fällen unterstützt die Bindung des Komplements die Phagocyten dabei, die toten und absterbenden Zellen vollständig zu beseitigen. So wird das Risiko verringert, dass Zellinhaltsstoffe freigesetzt werden und eine Autoimmunreaktion auslösen.
Man sieht, dass egal auf welchem Weg das Komplement aktiviert wird, diese Signalwege in C3 zusammenlaufen und die schlussendlich die gleichen Reaktionen auslösen. Dabei wirkt der Aufbau dieser Reaktionswege selbstverstärkend, so dass kleinste Mengen eines Pathogens ausreichen.
Die Reaktionswege des Komplements werden von Proteinen in Gang gesetzt, die als Mustererkennungsrezeptoren das Vorhandensein von Krankheitserregern erkennen können. Dadurch wird das erste Zymogen aktiviert, das dann eine Proteolysekaskade anstößt. Dabei werden die Komplementproteine nacheinander aktiviert, wobei jedes zu einer aktiven Protease wird, die viele Moleküle des nächsten Zymogens im Reaktionsweg spaltet und aktiviert. Auf diese Weise wird das Signal verstärkt, während sich die Kaskade fortsetzt. So kann selbst das Auftreten einer geringen Anzahl von Pathogenen eine schnelle Reaktion auslösen, die sich bei jedem Schritt deutlich verstärkt.
2. Was lässt das Lehrbuch über den Einfluss des Komplements auf Schäden durch das Spike-Protein ableiten?
2.1 Es kann zu Gerinnungsstörungen kommen:
Über enzymatische Wechselwirkungen und gemeinsame Regulatoren besteht eine enge Verbindung zum Gerinnungs- und Fibrinolysesystem. Dies erklärt, warum es bei vielen komplementbedingten Erkrankungen zur Entwicklung von Thrombosen kommt.
Das Komplement verbindet die an geborene und adaptive Immunität durch Verstärkung der Antikörperantwort, Modulation der T-Zell-Antwort und Förderung des immunologischen Gedächtnisses.
2.2 Das Komplement lockt Phagozyten in befallene Körpergewebe
Arne Burkhardt prägte den Begriff “Lymphozyten-Amok”5. Möglicherweise bietet das Lehrbuch für diese Beobachtung eine Erklärung. Es könnte an einer Komplementaktivierung liegen.
Die bekannten Rezeptoren für gebundene Komplementkomponenten sind mit ihrer Funktion und Verteilung in 7 Abb. 2.30 aufgeführt.
Der C3b-Rezeptor CR1 ist ein negativer Regulator der Komplementaktivierung. CR1 wird von vielen verschiedenen Arten von Immunzellen exprimiert, beispielweise von Makrophagen oder neutrophilen Zellen. Die Bindung von C3b an CR1 allein kann die Phagocytose nicht an regen, dafür sind weitere Immunmediatoren erforderlich, die Makrophagen aktivieren. So kann das kleine Komplementfragment C5a Makrophagen aktivieren, Bakterien aufzunehmen, die an ihre CR1-Rezeptoren gebunden sind. C5a bindet an den C5a Rezeptor, der ebenfalls von Makrophagen exprimiert wird. Dieser Rezeptor enthält sieben membrandurchspannende Domänen. Rezeptoren dieser Art übertragen ihre Signale durch guaninnucleotidbindende Proteine (G-Proteine) im Zellinneren und man bezeichnet sie deshalb allgemein als GProteingekoppelte Rezeptoren. C5L2 (GPR77) wird von neutrophilen Zellen und von Makrophagen exprimiert. Er ist ein nicht signalisierender Rezeptor, der für C5a als eine Art Köder (decoy receptor) fungiert und wahrscheinlich die Aktivität des C5a-Rezeptors reguliert. Auch Proteine, die mit der extra zellulären Matrix assoziiert sind wie Fibronectin, können zur Aktivierung von Phagocyten beitragen; diese Proteine sind von Bedeutung, wenn Phagocyten in das Bindegewebe gelockt und dort aktiviert werden.
Die Bindung vieler C3b-Moleküle an das Pathogen ist das zentrale Ereignis der Komplementaktivierung. Spezifische Komplementrezeptoren erkennen gebundene Komplementkomponenten, besonders C3b und seine inaktiven Fragmente. Diese Rezeptoren befinden sich auf phagocytotischen Zellen, die Pathogene aufnehmen, welche von C3b und seinen inaktiven Fragmenten opsonisiert wurden. Die kleinen Spaltprodukte von C3 und C5 binden an spezifische Rezeptoren, die an trimere G-Proteine gekoppelt sind, und locken so Phagocyten, beispielsweise neutrophile Zellen, zu Infektionsherden und aktivieren sie.
2.3 Die kleinen Peptidfragmente einiger Komplementproteine können eine lokale Entzündungsreaktion auslösen
Die kleinen Komplementfragmente C3a und C5a wirken auf spezifische Rezeptoren auf Endothelzellen und Mastzellen und rufen dadurch lokale Entzündungsreaktionen hervor. […] Wenn C3a und C5a in großer Menge gebildet oder systemisch injiziert werden, lösen sie einen allgemeinen Kreislaufkollaps aus und verursachen ein schockähnliches Syndrom, ähnlich einer systemischen allergischen Reaktion unter Mitwirkung von IgE-Antikörpern. Solch eine Reaktion bezeichnet man als anaphylaktischen Schock und die kleinen Fragmente des Komplements demzufolge häufig als Anaphylatoxine.
2.4 MCAS - Mastzellaktivierungssyndrom
Darüber hinaus können C3a und C5a Mastzellen aktivieren, die in Geweben unterhalb von Schleimhäuten vorkommen und anschließend Mediatoren wie Histamin und den Tumornekrosefaktor TNF-α freisetzen, die ähnliche Effekte hervorrufen. Die Veränderungen, die C5a und C3a verursachen, rekrutieren Antikörper und das Komplementsystem und locken Phagocyten zu Infektionsherden.
EN: “Cross talk between MCs and complement is facilitated by the production of complement proteins by MCs and their activation by the MC tryptase. The coordinated activity between MCs and the complement system plays a key role, for example, in a number of allergic, cutaneous, and vascular diseases.”6
DE: “Der Austausch zwischen Mastzellen und Komplement wird durch die Produktion von Komplementproteinen durch Mastzellen und deren Aktivierung durch die MC-Tryptase erleichtert. Die koordinierte Aktivität zwischen Mastzellen und dem Komplementsystem spielt beispielsweise bei einer Reihe von allergischen, Haut- und Gefäßerkrankungen eine Schlüsselrolle.”
Wenn der Reiz (das Spike-Protein) nicht verschwindet, könnte es zu einer Daueraktivierung der Mastzellen kommen, was sich als Mastzellaktivierungssyndrom äußern könnte. Die Mastzellen und das Komplement könnten sich dabei in feed-forward und feed-back Schleifen hochschaukeln.
EN: “Additionally, at a cellular level, MCs act as potent effector cells of complement activation by expressing receptors for C3a and C5a through which their chemoattraction and activation are mediated by anaphylatoxins in a paracrine and autocrine fashion.”7
DE “Darüber hinaus fungieren Mastzellen auf zellulärer Ebene als potente Effektorzellen der Komplementaktivierung, indem sie Rezeptoren für C3a und C5a exprimieren, über die ihre Chemoattraktion und Aktivierung durch Anaphylatoxine auf parakrine und autokrine Weise vermittelt wird.”
Dummerweise aktiviert das Spike-Protein die Mastzellen auch direkt.8
2.5 Krankheiten, die mit einer fehlgeleiteten Komplementaktivierung zusammenhängen können
atypisch hämolytisch-urämisches Syndrom
altersbedingte Maculadegeneration
2.6 Sheddingsymptomatik
Wie kann das Komplementsystem die von vielen Menschen beobachtete Sheddingsymptomatik und die hohen IgG Titer bei ungeimpften Menschen erklären?
Die Sekrete der Schleimhäute und die Gewebe enthalten etwa 10 % der gebildeten Komplementmenge.9
Das Spike-Protein aktivieren das Komplement direkt. Möglicherweise reichen dabei von Geimpften ausgeatmete Exosomen mit Spike-Protein10 bereits zur Aktivierung des Komplementsystems.
Das Komplement verbindet die an geborene und adaptive Immunität durch Verstärkung der Antikörperantwort, Modulation der T-Zell-Antwort und Förderung des immunologischen Gedächtnisses.11
2.3 Exosomen
Exosomen sind an vielen biologischen Prozessen im Zusammenhang mit TCR-ausgelösten Immunreaktionen, induziertem Zelltod, Antigenpräsentation und interzellulärem miRNA-Austausch beteiligt. Exosomen spielen eine Schlüsselrolle im Prozess der Zell-zu-Zell-Kommunikation und beeinflussen den Phänotyp der Empfängerzellen. Diese nanoskaligen extrazellulären Vesikel können von allen Zelltypen produziert werden und viele Arten von Signalmolekülen tragen, darunter mRNA, miRNAs, Proteine und Peptide. Neue Erkenntnisse zeigen, dass viele metabolische Proteinkinasen eine Vielzahl von Proteinsubstraten phosphorylieren, um die Genexpression, die Zellzyklusprogression und -proliferation, Apoptose, Autophagie und die Exosomensekretion zu regulieren. Exosomen können die Unterdrückung von Immunzellen bewirken. Auf diese Weise reduzieren Exosomen die Zahl der effektiven antigenpräsentierenden Zellen und hemmen die T-Zell-Reaktionen. Es sind jedoch weitere Studien erforderlich, um die Funktionen von Exosomen im Zusammenhang mit der Pathogenese von Krankheiten und therapeutischen Ansätzen aufzudecken.12
3. Das Spike Protein und das Komplementsystem
Es gab am Anfang die Theorie, dass das Spike Protein alle drei Wege des Komplement Systems aktivieren würde13 14, experimentell scheint sich jedoch der alternative Weg herauszukristallisieren.
DAS, das Spike-Protein das Komplement jedoch aktiviert, war anhand des Immunologie Lehrbuchs bereits ableitbar und wurde mittlerweile auch experimentell bestätigt:
EN: “This S1-induced pro-inflammatory phenotype led to exuberant C3 and C5b-9 deposition on endothelial cells, along with C3a and C5a generation that further amplified S1-induced complement activation. Functional blockade of ACE2 or complement inhibition halted S1-induced platelet aggregates by limiting von Willebrand factor and P-selectin exocytosis and expression on endothelial cells. Overall, we demonstrate that SARS-CoV-2-derived S1 is sufficient in itself to propagate inflammatory and thrombogenic processes in the microvasculature, amplified by the complement system, recapitulating the thromboembolic complications of COVID-19.”15
DE: “Dieser S1-induzierte pro-inflammatorische Phänotyp führte zu einer übermäßigen Ablagerung von C3 und C5b-9 auf Endothelzellen Endothelzellen sowie zur Bildung von C3a und C5a, die die S1-induzierte Komplementaktivierung weiter verstärkten. Aktivierung verstärkte. Die funktionelle Blockade von ACE2 oder die Komplementhemmung stoppte S1-induzierte Thrombozytenaggregate, indem sie die Exozytose und Expression von Willebrand-Faktor und P-Selektin Expression auf Endothelzellen. Insgesamt zeigen wir, dass das von SARS-CoV-2 stammende S1 allein ausreicht, um entzündliche und thrombogene Prozesse in der Mikrovaskulatur zu fördern, die durch das Komplementsystem verstärkt werden und die thromboembolischen Komplikationen von COVID-19.”
Das Komplement ist Bestandteil der Immunantwort gegen Sars-Cov2. Nicht überraschend, aber von der Politik komplett ignoriert. Der Einfluss auf Immunität ist somit auch nicht detailliert untersucht.
EN: “Furthermore, in the presence of the respective antiserum and COVID-19 convalescent serum, these epitopes successfully fixed the complement, implying a possible role in innate im munity.” 16
DE: „Außerdem haben diese Epitope in Gegenwart des entsprechenden Antiserums und des COVID-19-Rekonvaleszentenserums das Komplement erfolgreich gebunden, was auf eine mögliche Rolle in der angeborenen Immunität hindeutet.”
Das Spike-Protein aktiviert den alternativen Weg des Komplementsystems. Das ist der Weg, der von Pathogenen spontan und direkt aktiviert werden kann. Betroffen scheinen Menschen zu sein, die wohl genetisch vorbelastet sind. Das könnte auch erklären, warum bestimmte Menschen Sheddingsymptomatiken aufweisen, andere Menschen trotz hoher Titer nicht.
EN: “Direct activation of the alternative complement pathway by SARS-CoV-2 spike proteins is blocked by factor D inhibition. […]
Our data may explain why only a minority of COVID-19 patients develop life-threatening multiorgan failure. Complement-driven diseases such as aHUS, HELLP, and CAPS often have underlying germline variants that impair the ability of endothelial cells to protect themselves from complement-mediated injury in the setting of a complement-amplifying condition such as preg nancy, cancer, autoimmunity, or other inflammatory states. […]
Thus, it will be important to determine whether patients with the most severe forms of COVID-19 harbor variants in complement-regulatory genes.”17
DE: “Direkte Aktivierung des alternativen Komplementwegs durch SARS-CoV-2-Spike-Proteine wird durch Hemmung von Faktor D blockiert. […]
Unsere Daten könnten erklären, warum nur eine Minderheit der COVID-19-Patienten ein lebensbedrohliches Multiorganversagen entwickelt. Komplement-gesteuerte Krankheiten wie aHUS, HELLP und CAPS haben oft zugrundeliegende Keimbahnvarianten, die die Fähigkeit der Endothelzellen beeinträchtigen, sich vor komplementvermittelten Verletzungen im Rahmen einer komplementverstärkenden Erkrankung wie Schwangerschaft, Krebs, Autoimmunität oder anderen Entzündungszuständen zu schützen. […]
Daher wird es wichtig sein, festzustellen, ob Patienten mit den schwersten Formen von COVID-19 Varianten in Varianten in komplementregulierenden Genen aufweisen. ”
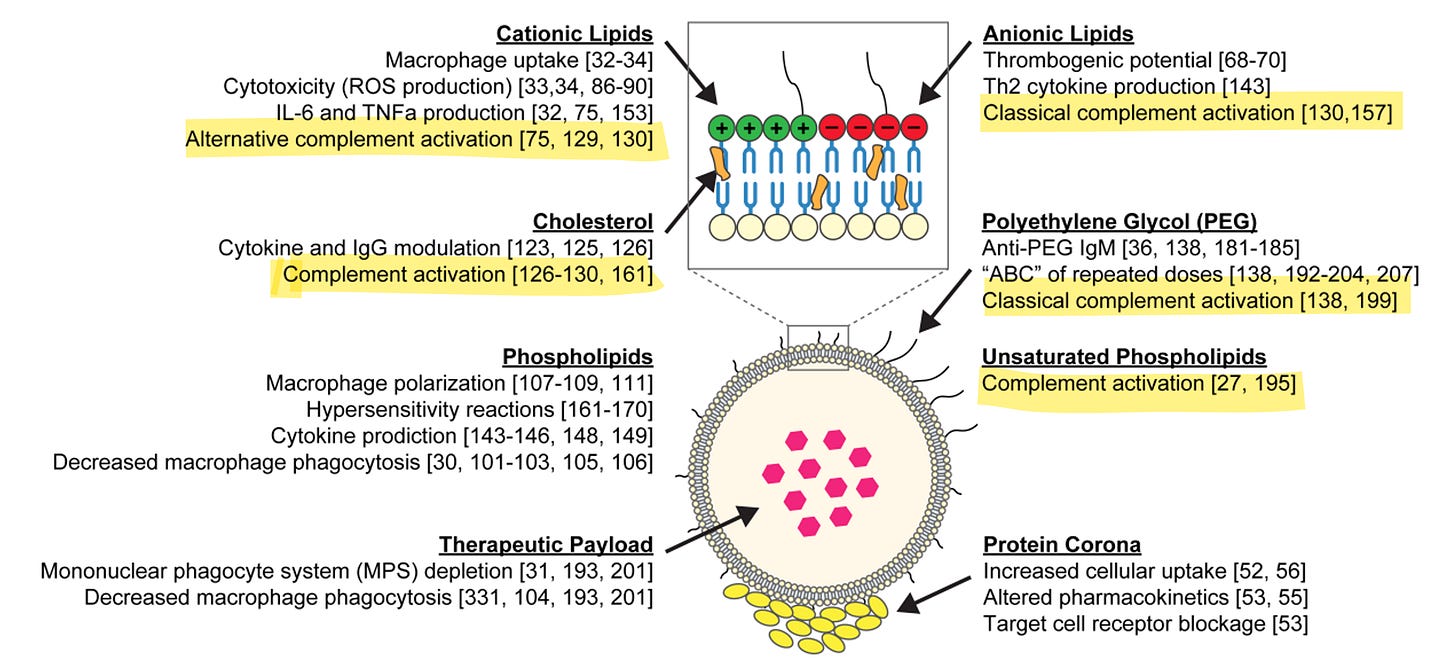
Lipidnanopartikel (LNPs) und das Komplement
Das Phänomen ist nicht neu. Das Problem war schon 2014 bekannt:
EN “Complement activation-related pseudoallergy: a stress reaction in blood triggered by nanomedicines and biologicals”18
DE: „Komplementaktivierungsbedingte Pseudoallergie: eine Stressreaktion im Blut, ausgelöst durch Nanomedikamente und biologische Stoffe“
Es gibt diverse Medikament, die das Komplement aktivieren, das ist nicht neu.
ABER:
EN: “mRNA-LNP COVID-19 Vaccine Lipids Induce Complement Activation and Production of Proinflammatory Cytokines: Mechanisms, Effects of Complement Inhibitors, and Relevance to Adverse Reactions.
Incubation of Pfizer-BioNTech's Comirnaty and Moderna's Spikevax with 75% human serum led to significant increases in C5a, sC5b-9, and Bb but not C4d, indicating C activation mainly via the alternative pathway.”19
DE: “mRNA-LNP COVID-19-Impfstoff-Lipide induzieren Komplementaktivierung und Produktion proinflammatorischer Zytokine: Mechanismen, Auswirkungen von Komplement-Inhibitoren und Bedeutung für unerwünschte Reaktionen.
Die Inkubation von Comirnaty von Pfizer-BioNTech und Spikevax von Moderna mit 75 % Humanserum führte zu einem signifikanten Anstieg von C5a, sC5b-9 und Bb, aber nicht von C4d, was auf eine C-Aktivierung hauptsächlich über den alternativen Weg hinweist.“
EN: “Results showed that recipients of mRNA vaccines exhibited elevated levels of serum acute-phase proteins, such as haptoglobin and C-reactive protein, alongside decreased white blood cell counts compared to those receiving conventional vaccines. Proteomic analysis identified significant changes in nine proteins, including interactions involving complement component C9, haptoglobin, and alpha-1-acid glycoprotein, suggesting implications for complement activation and inflammatory responses. Furthermore, variability in anti-polyethylene glycol antibody levels was noted among mRNA vaccine recipients compared to conventional vaccine recipients.”20
DE: “Die Ergebnisse zeigten, dass Empfänger von mRNA-Impfstoffen im Vergleich zu Empfängern herkömmlicher Impfstoffe erhöhte Werte von Akut-Phase-Proteinen im Serum, wie Haptoglobin und C-reaktives Protein, sowie eine verminderte Anzahl weißer Blutkörperchen aufwiesen. Die Proteomanalyse ergab signifikante Veränderungen bei neun Proteinen, darunter Wechselwirkungen zwischen dem Komplementkomponente C9, Haptoglobin und Alpha-1-Säureglykoprotein, was auf eine Aktivierung des Komplementsystems und Entzündungsreaktionen hindeutet. Darüber hinaus wurde bei Empfängern von mRNA-Impfstoffen im Vergleich zu Empfängern herkömmlicher Impfstoffe eine Variabilität der Anti-Polyethylenglykol-Antikörperkonzentrationen festgestellt.”
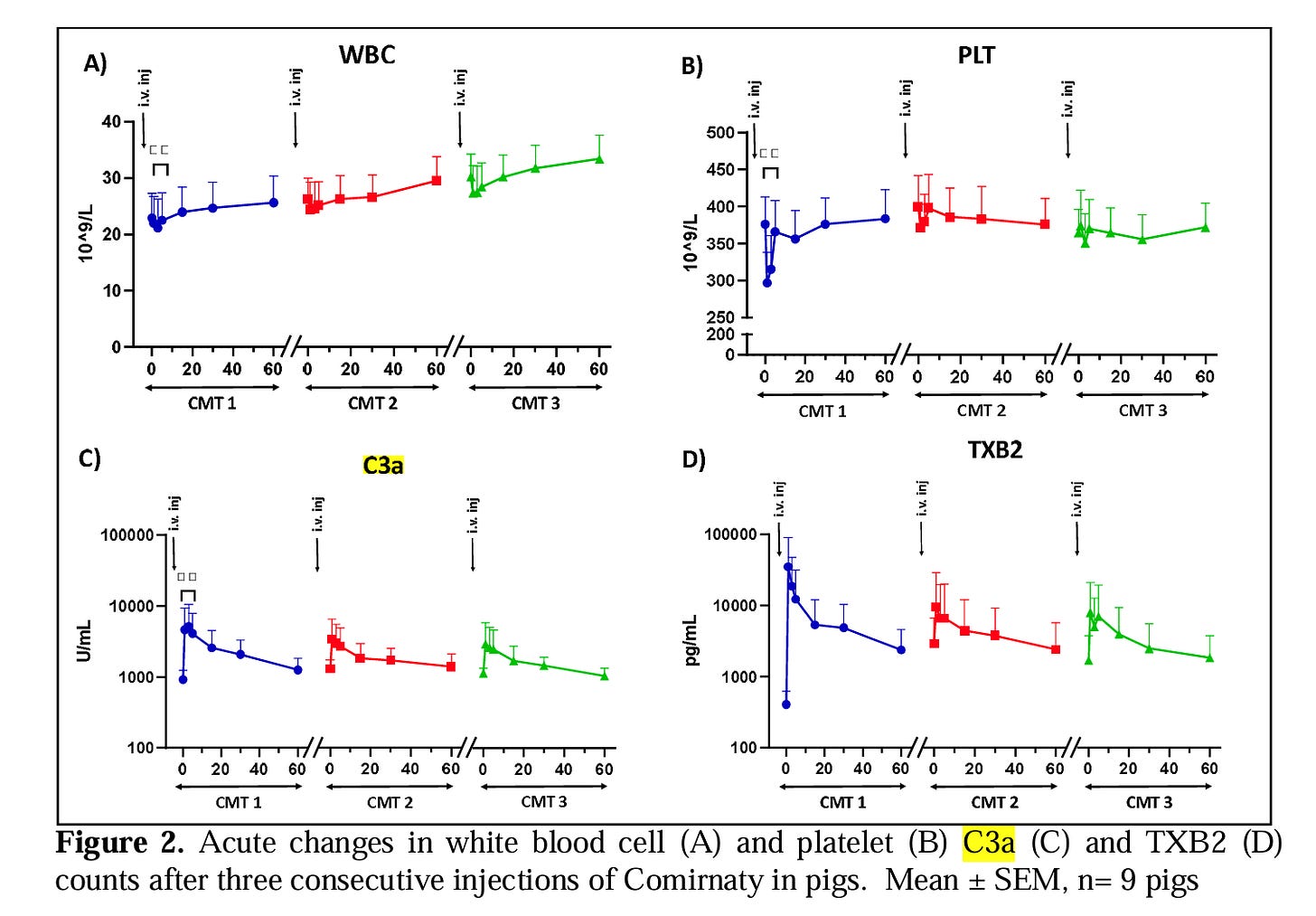
EN: “Figure 2B shows the other characteristic blood cell effect of immune active nanoparticles: transient thrombocytopenia. This change was observed only after the first vaccine injection, and it could not be repeated with further injections. Such thrombocytopenia is a well documented consequence of leukocyte and platelet activation, as well as pulmonary endothelial cell stimulation, mediated by the anaphylatoxins C3a and C5a. This process involves the formation of platelet–leukocyte aggregates and their transient adhesion to pulmonary endothelium, a phenomenon referred to as pulmonary marginalization. These interactions contribute to platelet sequestration and reversible thrombocytopenia during systemic inflammatory reactions (Guo & Ward, 2005; Sims & Wiedmer, 1991). Consistent with the above-delineated role of C activation in leukocytosis and thrombocytopenia, we found laboratory evidence of C activation: sudden rise of C3a anaphylatoxin on the same time course where blood cell changes occur (Figure 2C). “21
DE: “Abbildung 2B zeigt die andere charakteristische Wirkung immunaktiver Nanopartikel auf die Blutzellen: vorübergehende Thrombozytopenie. Diese Veränderung wurde nur nach der ersten Impfung beobachtet und konnte bei weiteren Injektionen nicht wiederholt werden. Eine solche Thrombozytopenie ist eine gut dokumentierte Folge der Aktivierung von Leukozyten und Thrombozyten sowie der Stimulation der Lungenendothelzellen, vermittelt durch die Anaphylatoxine C3a und C5a. Dieser Prozess beinhaltet die Bildung von Thrombozyten-Leukozyten-Aggregaten und deren vorübergehende Adhäsion an das Lungenendothel, ein Phänomen, das als pulmonale Marginalisierung bezeichnet wird. Diese Wechselwirkungen tragen zur Thrombozytensequestrierung und reversiblen Thrombozytopenie während systemischer Entzündungsreaktionen bei (Guo & Ward, 2005; Sims & Wiedmer, 1991). In Übereinstimmung mit der oben beschriebenen Rolle der C-Aktivierung bei Leukozytose und Thrombozytopenie fanden wir Laborbelege für eine C-Aktivierung: einen plötzlichen Anstieg des Anaphylatoxins C3a im gleichen Zeitverlauf wie die Veränderungen der Blutzellen (Abbildung 2C).”
Die Symptome jedoch, decken sich recht gut, mit den häufigsten Nebenwirkungen im Beipackzettel.
Die Symptome decken sich auch mit dem, was Menschen als Sheddingsymptomatik bezeichnen.
Sowohl die Nebenwirkungen als auch die Sheddingsymptome könnten durch eine Komplementaktivierung im Sinne eine Pseudoallergie (CARPA - complement activated pseudoallergy) verursacht zu sein.
“CARPA Reaktionen sind Komplement aktivierte Pseudoallergien, die nicht vorhersagbar, nicht testbar, schnell oder langsam eintreten können und mitunter tödlich enden. 5% bis 45% der Menschen reagieren mit einer CARPA Reaktion auf Nanolipide im Gegensatz zu weniger als 2% auf Penicillin.”22
Welche immunologischen Reaktionen hinter den jeweiligen Symptomen stehen, kann dabei von Mastzellaktivierung über Lymphozyten-Amok… gehen. Das macht die Diagnose herausfordernd.
Updates:
18.06.2025:
Inglut CT, Sorrin AJ, Kuruppu T, Vig S, Cicalo J, Ahmad H, Huang HC. Immunological and Toxicological Considerations for the Design of Liposomes. Nanomaterials (Basel). 2020 Jan 22;10(2):190. doi: 10.3390/nano10020190. PMID: 31978968; PMCID: PMC7074910. https://www.mdpi.com/2079-4991/10/2/190)
Xiao MT, Ellsworth CR, Qin X. Emerging role of complement in COVID-19 and other respiratory virus diseases. Cell Mol Life Sci. 2024 Feb 18;81(1):94. doi: 10.1007/s00018-024-05157-8. PMID: 38368584; PMCID: PMC10874912. https://pmc.ncbi.nlm.nih.gov/articles/PMC10874912/
Schieffer, E., & Schieffer, B. (2022). The rationale for the treatment of long-Covid symptoms – A cardiologist’s view. Frontiers in Cardiovascular Medicine, 9. https://doi.org/10.3389/fcvm.2022.992686
Thomas, L. (2024, June 30). Kapitel 24: Komplementsystem. Labor & Diagnose. https://www.labor-und-diagnose.de/k24.html
“Lymphozyten-Amok” nach Impfung. (n.d.). https://www.achgut.com/artikel/lymphozyten-amok_nach_impfung
Elieh Ali Komi D, Shafaghat F, Kovanen PT, Meri S. Mast cells and complement system: Ancient interactions between components of innate immunity. Allergy. 2020 Nov;75(11):2818-2828. doi: 10.1111/all.14413. Epub 2020 Jun 15. PMID: 32446274. https://pubmed.ncbi.nlm.nih.gov/32446274/
Elieh Ali Komi D, Shafaghat F, Kovanen PT, Meri S. Mast cells and complement system: Ancient interactions between components of innate immunity. Allergy. 2020 Nov;75(11):2818-2828. doi: 10.1111/all.14413. Epub 2020 Jun 15. PMID: 32446274. https://pubmed.ncbi.nlm.nih.gov/32446274/
Zhang S, Xu C-L, Wang J, Xiong X, Wang J-H. Spike proteins of coronaviruses activate mast cells for degranulation via stimulating Src/PI3K/AKT/Ca2+ intracellular signaling cascade. J Virol. 2025 Apr 30:e0007825. doi: 10.1128/jvi.00078-25. Epub ahead of print. PMID: 40304504. https://pubmed.ncbi.nlm.nih.gov/40304504/
Thomas, L. (2024, June 30). Kapitel 24: Komplementsystem. Labor & Diagnose. https://www.labor-und-diagnose.de/k24.html
Vitriol, D. V. (2024f, February 29). Mögliche biochemische Wege zu shedden. DrBine’s Newsletter.
Mögliche biochemische Wege zu shedden
Eigentlich sind die Puzzlestücke schon alle irgendwo in meinen Artikeln, aber ich fasse sieh hier einmal in einem gemeinsamen Artikel zusammen und strukturiere sie um. Text- und Buchstabenrecycling, um die Umwelt zu schonen. Wer weiß, vielleicht werden in Deutschland irgendwann sogar dich Buchstaben knapp. Darf ich das „Z“ mittlerweile wieder verwenden …
Schröder-Braunstein, J., & Kirschfink, M. (2020). Das Komplementsystem: von den Grundlagen zur klinischen Bedeutung. Transfusionsmedizin, 10(02), 75–88. https://doi.org/10.1055/a-0997-4456 (https://www.thieme-connect.com/products/ejournals/abstract/10.1055/a-0997-4456)
Engin A. Dark-Side of Exosomes. Adv Exp Med Biol. 2021;1275:101-131. doi: 10.1007/978-3-030-49844-3_4. PMID: 33539013. https://pubmed.ncbi.nlm.nih.gov/33539013/
Perico L, Benigni A, Remuzzi G. SARS-CoV-2 and the spike protein in endotheliopathy. Trends Microbiol. 2024 Jan;32(1):53-67. doi: 10.1016/j.tim.2023.06.004. Epub 2023 Jun 12. PMID: 37393180; PMCID: PMC10258582. https://pubmed.ncbi.nlm.nih.gov/37393180/
Vitriol, D. V. (2024a, January 22). X Mechanismen der Thrombosenbildung durch die Plörre. DrBine’s Newsletter. https://drbine.substack.com/publish/post/140931721
Perico L, Morigi M, Galbusera M, Pezzotta A, Gastoldi S, Imberti B, Perna A, Ruggenenti P, Donadelli R, Benigni A, Remuzzi G. SARS-CoV-2 Spike Protein 1 Activates Microvascular Endothelial Cells and Complement System Leading to Platelet Aggregation. Front Immunol. 2022 Mar 7;13:827146. doi: 10.3389/fimmu.2022.827146. PMID: 35320941; PMCID: PMC8936079. https://pubmed.ncbi.nlm.nih.gov/35320941/
Rathore D, Chauhan P, Bonagiri A, Gandhi L, Maisnam D, Kumar R, Row AT, Kesavulu MM, Venkataramana M. Non-RBD peptides of SARS-CoV-2 spike protein exhibit immunodominance as they elicit both innate and adaptive immune responses. Heliyon. 2024 Oct 29;10(21):e39941. doi: 10.1016/j.heliyon.2024.e39941. PMID: 39568852; PMCID: PMC11577203. https://pubmed.ncbi.nlm.nih.gov/39568852/
Yu J, Yuan X, Chen H, Chaturvedi S, Braunstein EM, Brodsky RA. Direct activation of the alternative complement pathway by SARS-CoV-2 spike proteins is blocked by factor D inhibition. Blood. 2020 Oct 29;136(18):2080-2089. doi: 10.1182/blood.2020008248. PMID: 32877502; PMCID: PMC7596849. https://pubmed.ncbi.nlm.nih.gov/32877502/
Szebeni J. Complement activation-related pseudoallergy: a stress reaction in blood triggered by nanomedicines and biologicals. Mol Immunol. 2014 Oct;61(2):163-73. doi: 10.1016/j.molimm.2014.06.038. Epub 2014 Aug 12. PMID: 25124145. https://pubmed.ncbi.nlm.nih.gov/25124145/
Bakos T, Mészáros T, Kozma GT, Berényi P, Facskó R, Farkas H, Dézsi L, Heirman C, de Koker S, Schiffelers R, Glatter KA, Radovits T, Szénási G, Szebeni J. mRNA-LNP COVID-19 Vaccine Lipids Induce Complement Activation and Production of Proinflammatory Cytokines: Mechanisms, Effects of Complement Inhibitors, and Relevance to Adverse Reactions. Int J Mol Sci. 2024 Mar 22;25(7):3595. doi: 10.3390/ijms25073595. PMID: 38612407; PMCID: PMC11012056. https://pubmed.ncbi.nlm.nih.gov/38612407/
Roh G, Lee J, Park HM, Kwak W, Park HJ, Oh A, Na Y, Ha D, Lee YS, Bae SH, Lee S, Yoon S, Lee S, Jung J, Lee J, Nam JH. Comparative immunologic profiling of mRNA and protein-conjugated vaccines: acute inflammatory responses and anti-PEG antibody production. Anim Cells Syst (Seoul). 2025 Jun 10;29(1):387-401. doi: 10.1080/19768354.2025.2510984. PMID: 40503431; PMCID: PMC12153003. https://pubmed.ncbi.nlm.nih.gov/40503431/
László Dézsi, Gábor Kökény, Gábor Szénási, Csaba Révész, Tamás Mészáros, Bálint A. Barta, Réka Facsko, Anna Szilasi, Tamás Bakos, Gergely T. Kozma, Attila B. Dobos, Béla Merkely, Tamás Radovits, János Szebeni. Acute anaphylactic and multiorgan inflammatory effects of Comirnaty in pigs: evidence of spike protein mRNA transfection and paralleling inflammatory cytokine upregulation bioRxiv 2025.06.07.658379; doi: https://doi.org/10.1101/2025.06.07.658379 https://www.biorxiv.org/content/10.1101/2025.06.07.658379v1
Szebeni J. Complement activation-related pseudoallergy: a stress reaction in blood triggered by nanomedicines and biologicals. Mol Immunol. 2014 Oct;61(2):163-73. doi: 10.1016/j.molimm.2014.06.038. Epub 2014 Aug 12. PMID: 25124145. https://pubmed.ncbi.nlm.nih.gov/25124145/













Some in the medical freedom movement have argued for the non-existence of viruses, and even if they existed, that we do not know how they make us sick.
This essay clearly demonstrates how the m-rna/lnp platform creates spike protein which in turn causes sickness through the complement system as you demonstrate.
I suppose, we still have not proven the existence of Sars-Cov-2 itself (never been isolated and just a computer model) and how it makes us sick versus knowing how the m-rna/lnp platform makes us sick through the production of spike protein.
But if viruses don't exist what were Baric/Zhengli actually working "with" to make the virus attack the ACE2 receptors in the body? Obviously, they would not get paid if what they were working with was imaginary and just a computer model? Would they not have to actually work with a real virus to enhance its ability to bind to the ACE2 receptors or were they just working with a computer model? But why would they spend so much time hunting in the caves of China for particular bats as real virus building blocks to be GOF?
If too dumb to answer, I understand.
Thank you.