Eigentlich sind die Puzzlestücke schon alle irgendwo in meinen Artikeln, aber ich fasse sieh hier einmal in einem gemeinsamen Artikel zusammen und strukturiere sie um. Text- und Buchstabenrecycling, um die Umwelt zu schonen. Wer weiß, vielleicht werden in Deutschland irgendwann sogar dich Buchstaben knapp. Darf ich das „Z“ mittlerweile wieder verwenden oder ist es noch verboten?
Vorab Sheddingdefinition der FDA, keine Ahnung, ob die EMA auch eine Definition hat:
Im Sinne dieses Leitfadens bedeutet der Begriff "Shedding" die Freisetzung von VBGT oder onkolytischen Produkten aus dem Patienten auf einem oder allen der folgenden Wege: Ausscheidungen (Kot), Sekrete (Urin, Speichel, Nasopharyngealflüssigkeit usw.) oder über die Haut (Pusteln, Wunden). Shedding unterscheidet sich von der Biodistribution, da letztere beschreibt, wie ein Produkt vom Verabreichungsort im Körper des Patienten verteilt wird, während ersteres beschreibt, wie es Ausscheidung oder Freisetzung aus dem Körper des Patienten. Beim Shedding besteht die Möglichkeit der Übertragung von VBGT oder onkolytischer Produkte von behandelten auf unbehandelte Personen (z. B. enge Kontakte und Angehörige der Gesundheitsberufe). https://www.fda.gov/media/89036/download
Schritt 1: Das Produkt muss im Körper umverpackt werden.
ALSO es shedded NICHT das original BNT162B2 oder Moderna-Produkt sondern eine umverpackte Version, eine billige Fälschung. Damit vermeidet die Natur möglicherweise patentrechtliche Probleme, sonst würden die Firmen sicherlich noch Mutter Natur wegen der unrechtmäßigen Verwendung ihrer Technologie verklagen, so wie sich die Firmen gerade gegenseitig verklagen. Zahlen müsste dann wohl der Steuerzahler. Zum einen derjenige, der das patentgeschützte Produkte widerrechtlich in Umlauf gebracht hat (geshedded) hat und derjenige, der es kostenlos in der gefälschten, umverpackten Version verwendet hat, ohne dafür zu zahlen. Kennt man so ähnlich von Monsanto und seinem sich verteilenden Genmais/Gensoja, da werden dann die geschädigten Bauern, die keinen Genmais/Gensojs wollten verklagt, weil er auf ihrem Feld steht und sie nicht dafür gezahlt haben. (https://www.theguardian.com/environment/2013/feb/12/monsanto-sues-farmers-seed-patents)
Im einen Fall wird dabei das Produkt der modRNA, das Spike-Protein, umverpackt und in Umlauf gebracht, das dürfte vom Patenrecht sicherlich unproblematisch sein, denn die Herstellung des Spike-Proteins ist ja an die jeweiligen Konsumenten outgesourced worden. Sie dürften damit die Rechte an den Spike-Protein-Varianten haben, die sie selbst hergestellt haben und die nicht unbedingt dem Original entsprechen müssen. Manche Zellen werden ja kreativ und wandeln das Spike ein wenig ab, durch Frameshifts (https://pubmed.ncbi.nlm.nih.gov/38057663/) und dergleichen. Das fällt dann vielleicht unter Kunstfreiheit?
Die zweite Variante ist grenzwertig. Da wird ein Teil des codonoptimierten Originalprodukts umverackt. Das umschifft zwar die Patentklagen um die Lipide und deren Nutzung, wie das aber mit den jeweiligen optimierten Gensequenzen aussieht und dem P-Lock, das vom NIH patentiert ist (https://patents.google.com/patent/US10960070B2/en), kann ich nicht sagen, ich bin kein Patentanwalt. Die modRNA wurde ja im Prinzip korrekt erworben und darf somit theoretisch gebraucht weitergegeben werden, wie gebrauchte Sachen auf einem Flohmarkt, wäre so meine Vermutung.
Das Spike Protein wird in Exosomen verpackt
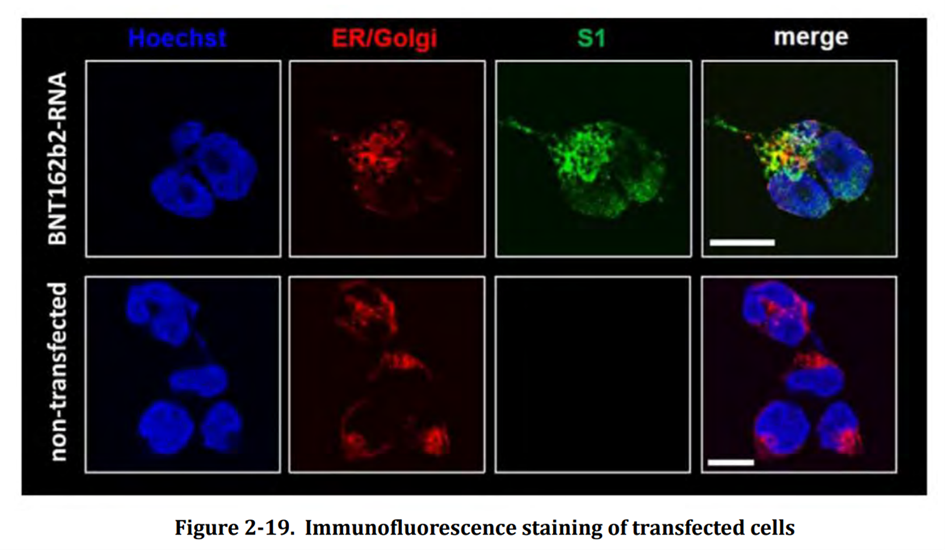
“Diese Ergebnisse zeigen, dass beide Antigene im endoplasmatischen Retikulum verarbeitet werden, zur Sekretion und/oder Oberflächenexpression.” (https://www.tga.gov.au/sites/default/files/foi-2389-03-1.pdf)
Dazu gibt es noch eine Kontrolle aus einem anderen FOIA, ja passt, is tatsächlich so. (https://www.tga.gov.au/sites/default/files/foi-2389-06.pdf)
Wie man sieht, unterscheiden sich die Bilder in der “Investigators Brochure” und im “Nonclinical Evaluation Report”. Diese Versuche wurden also zumindest zweimal gemacht und überprüft und somit können die Daten wohl als gesichert gelten.
Man sieht außerdem, dass das Spike-Protein in den Zellkern geht, nur so nebenbei. Da sollte es sich eigentlich nicht herumtreiben. Bestimmt treibt es da ungehörigen Schabernack, aber das ist aktuell nicht Thema.
Hier noch einmal in ihren eigenen Worten „Das S Protein wird im ER prozessiert.“
Exkurs zum Endoplasmatischen Retikulum:
Ich zitiere hier nun gekürzt aus dem Campbell Biologie 10. Auflage S. 141ff, würde aber auch im alten Campbell 1. Auflage so ähnlich drinnen stehen, denn der Herr Golgi entdeckte diesen Golgi- Apparat 1875. So alt, ist das Wissen, das die modRNA Gläubigen ignorieren.
„Das endoplasmatische Reticulum (ER) ist ein ausgedehntes Netzwerk aus Membranen, das in vielen eukaryotischen Zellen mehr als die Hälfte der Gesamtmembranfläche stellt […].
Man unterscheidet zwei funktionell verschiedene Bereich des ER, die kontinuierlich ineinander übergehen können. Das glatte ER verdankt seinen Namen der Tatsache, dass sich an diesen Membranbereichen keine außen anhaftenden Ribosomen finden. Das raue ER trägt auf seiner Membranaußenseite Ribosomen, die diesen Membranbereichen in elektronenmikroskopischen Bildern ein raues, körniges Aussehen verleihen. […]
Die Funktionen des rauen ER
[…] Schon während der Synthese wird die Polypeptidkette cotranslational durch ein von einem speziellen Porenkomplex in der ER-Membran gebildeten Öffnung in das Lumen des Organells geschleust. […]
Die Proteine des sekretorischen Weges unterscheiden sich bezüglich ihres Transports in das ER-Lumen von den an freien Ribosomen gebildeten cytosolischen Proteinen. Sekretorische Proteine verlassen das ER verpackt in Vesikel, […].
Über die Produktion sekretorischer Proteine hinaus ist das raue ER allgemein der Syntheseort für neue Membranen. […] Künftige Membranproteine werden in den meisten Fällen cotranslational gefaltet, in die Membran insertiert und durch hydrophobe Wechselwirkungen verankert. […]
Exkurs Golgi Apparat aus Wikipedia
Die Funktionen des Golgi-Apparates sind vielfältig und sehr komplex, lassen sich aber nach dem heutigen Wissensstand in drei Gruppen einteilen:
Bildung und Speicherung sekretorischer Vesikel (extrazelluläre Matrix, Transmitter/Hormone),
Synthese und Modifizierung von Elementen der Plasmamembran,
Bildung von primären Lysosomen.
Der Golgi-Apparat funktioniert im Grunde wie die Post: Er empfängt Proteinpäckchen aus dem Endoplasmatischen Retikulum. Innerhalb des Golgi werden diese Proteine modifiziert, indem Zuckermonomere entfernt oder ersetzt werden. Zusätzlich werden die Proteine sortiert, indem Identifikationssymbole wie Phosphatgruppen (ähnlich einer Postleitzahl) angehängt werden. Diese „Postleitzahl“ nennt den Zielort. Schließlich werden die Proteine in Transportvesikeln versendet.
Das ist keine Raketenwissenschaft, das steht sogar (noch) bei Wikipedia.
Für das Spike-Protein selbst ist experimentell nachgewiesen, dass es in und auf Exosomen im Blut kursiert, sowohl nach modRNA-Injektion (https://doi.org/10.4049/jimmunol.2100637) als auch nach Infektion (https://onlinelibrary.wiley.com/doi/10.1002/jmv.28568, https://www.sciencedirect.com/science/article/pii/S1053249822003321). Das kann man für sich selbst auch bei MMD prüfen lassen (https://www.mmd-labor.de/.cm4all/uproc.php/0/Auftrgasformulare/Auftragsformular%20X%20Post%20Covid%20Post%20Vac_1.pdf?cdp=a&_=18cb53d2708)
Die modRNA wird in Exosomen verpackt
BioNTech selbst hat sein Produkt in den Zulassungsunterlagen mit Onpattro (Patisiran) verglichen (https://www.tga.gov.au/sites/default/files/foi-2389-06.pdf). Es kann also davon ausgegangen werden, dass BioNTech sich im Detail mit der Pharmacokinetik von Onpattro (Patisiran) befasst hat und davon ausgeht, dass ihr Produkt eine Onpattro (Patisiran) ähnliche Pharmacokinetik aufweisen wird, sonst hätte man es nicht als Vergleich hinzugezogen, um keine separaten Studien zu den Lipiden durchführen zu müssen und sich die Pharmacokinetik gleich komplett zu sparen (https://cdn.prod.www.manager-magazin.de/media/4cc0d9db-b895-4b7f-ba07-42ef335634d8/BiontechPfizer_Clinical_Protocol.pdf).
Bei Onpattro (Patisiran) und somit auch bei den modRNA-Produkten, ist die Freisetzung der Nutzlast (siRNA im Falle von Onpattro (Patisira) und modRNA im Falle von BNT162B2) aus den Lysosomen in das Zellzytosol bekanntlich der limitierende Schritt.
Vorab: „Die genauen Orte und Mechanismen, durch die LNPs der mRNA helfen, aus dem endosomalen Lumen zu entkommen, sind bis heute rätselhaft.“ (https://pubmed.ncbi.nlm.nih.gov/34882187/)
Ein Großteil der modRNA bleibt in frühen Endosomen stecken, die kaputt sind. Diese Anhäufung kaputter Endosomen kann zu Entzündungsreaktionen führen und cytotoxische Konsequenzen für die Zelle haben. (https://pubmed.ncbi.nlm.nih.gov/34882187/)
Genau wie Onpattro (Patisiran), landet der größte Teil der Therapie auch bei BNT162B2 in der Leber.
Abbildung: Vorgeschlagener Mechanismus der Leberaufnahme von Patisiran LNP und der Freisetzung aus der Leber nach intravenöser Verabreichung. (1) Nach intravenöser Verabreichung von Patisiran dissoziiert PEG2000-C-DMG vom LNP. (2) Die Entfernung der PEG-Beschichtung ermöglicht die Assoziation von endogenem ApoE mit dem LNP, wodurch die Aufnahme in Hepatozyten durch einen ApoE-abhängigen Prozess erleichtert wird. (3) Bei der Internalisierung durch Endozytose wird das ionisierbare DLin-MC3-DMA-Lipid protoniert (positiv geladen), da der pH-Wert im Endosom sinkt. (4) Das positiv geladene DLin-MC3-DMA-Lipid interagiert mit dem negativ geladenen endosomalen Lipid, was zur Desintegration des LNP, zur Destabilisierung der Endosomenmembran und zur Freisetzung von ALN-18328 in das Zytoplasma führt. (5) ALN-18328 bindet an RISC, was zu einem gezielten Abbau der TTR-mRNA und einer anschließenden Verringerung der Zielproteinspiegel führt. (6) Ein Teil der internalisierten LNPs wird durch Exozytose aus den späten Endosomen/Lysosomen wieder in den Blutkreislauf ausgeschieden. ALN-18328, Patisiran-Wirkstoff (kleine interferierende Ribonukleinsäure); ApoE, Apolipoprotein E; IV, intravenös; LDLR, Low-Density-Lipoprotein-Rezeptor; LNP, Lipid-Nanopartikel; mRNA, Boten-RNA; PEG2000-C-DMG, α-(3′-{[1,2 Di(myristyloxy)proponoxy]carbonylamino}propyl)-ω-methoxy, Polyoxyethylen; PEG, PEG2000-C-DMG; DLin-MC3-DMA, (6Z,9Z,28Z,31Z)-Heptatriaconta-6,9,28,31-tetraen-19-yl-4-(dimethylamino)butanoat; RISC, RNA-induzierter Silencing-Komplex; siRNA, small interfering ribonucleic acid; TTR, Transthyretin. (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7187331/)
Den durch Exozytose aus der Leber ausgeschiedene Anteil des Produktes, sei es Onpattro (Patisiran) oder BNT162B2 wird als Extrazelluläre Vesikel, auch Exosomen genannt, in den Blutkreislauf ausgeschieden.
Die Frage ist, wieviel davon könnte als Exosomen ausgeschieden werden?
Die Antwort dazu hat Moderna:
„In vitro führen nur 1-2 % der durch Lipidnanopartikel (LNP) vermittelten Nukleinsäureübertragung zu einer erfolgreichen Zelltransfektion. Das pathogene Potenzial der restlichen 98 % ist jedoch noch nicht ausreichend erforscht.“ (https://pubmed.ncbi.nlm.nih.gov/38263456/).
Ich gehe daher mal von 98% des Produktes aus, das irgendwie, irgendwo vom Körper über Vesikel entsorgt wird.
Wenn das nicht der Fall wäre, würde MMD (siehe oben) das nicht als Labornachweis anbieten. Damit wäre der Beweis im Prinzip erbracht, auch wenn das nicht direkt publiziert ist.
Leider liegen mir keine Laborwerte vor, in welchem Bereich sich das mengenmäßig bewegt.
Basierend auf dem Wissen von Onpattro (Patisiran) ist jedoch bereits davon auszugehen, dass die modRNA selbst ebenfalls in Exosomen im Blutkreislauf kursiert, da Exosomen dafür bekannt sind verschiedenste funktionelle RNA-Spezies zu beinhalten und zu transportieren, die anschließend auch in Proteine übersetzt werden können (https://pubmed.ncbi.nlm.nih.gov/33539013/). Dieser Effekt wurde auch für exogene, also körperfremde RNA gezeigt (https://www.nature.com/articles/s41467-019-12275-6) und von den Autoren des Nature Papers als potentielle Verbreitungsmöglichkeit der exogenen RNA identifiziert. Siguna Müller hat sich diesem Paper detailliert gewidmet:
Die Onpattro (Patisiran) Exosomen haben eine Halbwertszeit von 60-80 Tagen (https://pubmed.ncbi.nlm.nih.gov/31777097/). Halbwertszeit bedeutet, dass diese mit exogenem Erbgut beladenen Exosomen, unter Umständen beladen mit somit optimal vor dem Immunsystem und vor einem Abbau geschützter modRNA, bis zu einem Jahr im Körper kursieren und Zellen nachträglich transfizieren können. Mit modRNA beladene Exosomen können andere Zellen transfizieren und werden daher als deutlich weniger toxische Alternative zu LNPs erforscht (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8435577/ , https://pubmed.ncbi.nlm.nih.gov/33539013/). Das bedeutet, dass sämtliche Organe bis zu einem Jahr nach der letzten Injektion noch nachträglich transfiziert und zur Spike-Protein Produktion gebracht werden können. Die Symptomatik kann sich also exosomenbedingt über ein Jahr lang weiterhin verschlechtern. Somit müssen die Schäden durch das Produkt nicht zeitnah zur Injektion entstehen. Das ist aber köperinternes Shedding.
Schritt 2: Das Produkt muss aus dem Körper entsorgt werden
Nachdem das Spike und die modRNA in Exosomen umverpackt wurden, wobei sich das Spike durchaus auch auf der Oberfläche eines Exosoms befinden kann, müssten diese Informationspakete irgendwie verarbeitet werden. Exosomen haben diverse Funktionen, eigentlich sind sie eher so eine Art interne Email, die an @all geht und die jeder lesen kann. Manchmal aber geht diese Interne Email auch nach draußen, wo sie eigentlich nicht hingehört und auch nicht gelesen werden sollte. Man leakt sozusagen interne Körperinformationen, die für den rein internen Gebrauch vorgesehen waren.
Teilweise könnten Exosomen aber auch als Mülltüten verwendet werden, um Datenmüll aus dem System zu entfernen.
Exosomen/EVs werden z. Bsp. ausgeatmet (https://www.nature.com/articles/s41598-020-73243-5#Sec3, https://www.jacionline.org/article/S0091-6749(13)00524-1/fulltext, https://erj.ersjournals.com/content/58/2/2003024.long) und sind immunogen. So immunogen, dass man sie als Imfpstoffe erforscht (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8317489/), z. Bsp auch gegen Covid (https://pubmed.ncbi.nlm.nih.gov/36232549/ wer hätte das gedacht…).
Diese Paper könnte diese Methode nehmen, um nach der modRNA nach “Impfung” zu suchen und nachzuweisen. Exhaled breath condensate contains extracellular vesicles (EVs) that carry miRNA cargos of lung tissue origin that can be selectively purified and analyzed - PubMed (nih.gov)
Schritt 3: Das Produkt muss von einem anderen Menschen aufgenommen werden.
Und das richtig coole dabei, in diesem Paper (https://pubmed.ncbi.nlm.nih.gov/36232549/) waren sowohl Spike gefüllte als auch RNA-gefüllte Exosomen dabei, die zum inhalieren waren:
Produziert wurden diese „Impfstoffe“ teilweise in LUNGENZELLKULTUR. Gut, das geht jetzt billiger und einfacher, das machen die Geschlumpften ganz kostenlos. Ein sich selbst verteilender Impfstoff auf Exosomenbasis ABER wahrscheinlich ein Gemisch aus Spike-Exosomen und modRNA-Exosomen, also keine definierten Reinprodukte wie im oben zitierten Paper.
Aber auch das ist nicht neu, das ist so alt, dazu gab es schon im Oktober 2020 Review Artikel: Inhaled RNA Therapy: From Promise to Reality - PubMed (nih.gov)
Das Shedding über Exosomen ist kein bug es ist ein feature (https://pubmed.ncbi.nlm.nih.gov/34654691/).
Wie lange Aerosole in der Luft bleiben wurde uns ja in der Plandemie als Argument für Masken vorgebetet (https://www.umweltbundesamt.de/themen/gesundheit/umwelteinfluesse-auf-den-menschen/innenraumluft/infektioese-aerosole-in-innenraeumen#was-sind-aerosole-) da kann man direkt beim Bundesumweltamt mal nachschauen, wie lange infektiöse Aerosole wie EXOSOMEN in der Luft bleiben. Diese kann man nun einfach von der Größe her mit den Viren gleich setzen.
Wir haben aber auch gelernt: Masken bringen nichts, Lüften und Ozonieren aber schon. Filter waren wiederum häufig nutzlos. Vielleicht sollte man auch einfach von den Geschlumpften den „traditionellen“ Plandemieabstand halten, um Sheddingsymptome zu vermeiden (der auf keiner rationalen Basis basierte und komplett erfunden war).
Ein sich selbst herstellender, sich selbst verteilender Impfstoff, der soweit “natürlich” über die Schleimhäute abreagiert, aber dadurch Immunreaktionen natürlich Symptome erzeugen kann.
Aber man wird nicht nur über Inhalation immunisiert.
Und in der freien Wildbahn scheinen Exosomen bei Raumtemperatur 2 Tage stabil zu sein (https://bmccancer.biomedcentral.com/articles/10.1186/s12885-016-2783-2). Ich schätze, das trifft am ehesten auf geschlossene Räume ohne Witterung zu, wo die Exosomen unbehelligt eine Weile herumliegen können, bis die Putzfrau kommt.
Wenn man dann Oberflächen anfasst, auf denen sich derartige Exosomen befinden, hat man den Effekt des Impfens durch Eincremen (https://analyticalscience.wiley.com/content/article-do/impfung-durch-eincremen) über die Haarfolikel.
Andere Formen der externen, unfreiwilligen Aufnahme der ausgeschiedenen Exosomen wären über Körperflüssigkeiten, also über sehr engen menschlichen Kontakt, den man durchaus vermeiden kann, anders als das Atmen. OK, eine Ausnahme des Vermeidens des Körperkontaktes in Sachen Shedding gibt es schon: Das Kind in der Placenta hat halt Pech gehabt beim Vermeiden von engem Körperkontakt.
Muttermilch - Exosomen mit modRNA? da über rt-PCR nachgewiesen (https://pubmed.ncbi.nlm.nih.gov/34228115/, https://pubmed.ncbi.nlm.nih.gov/36156636/, https://www.medrxiv.org/content/10.1101/2021.04.27.21256151v1)
Placental - hier möglicherweise das unverfälschte Originalprodukt (zwei “Immunisierungen” zum Preis von einer)? Vielleicht auch Exosomen der Mutter?(https://doi.org/10.1016/j.ajog.2024.01.022)
Bluttransfusion (da MMD die Exosomen beider Arten im Blut nachweisen kann, sind sie wohl zwangsweise auch im Spenderblut enthalten).
Organstransplantation - Bisher keine Daten. Bei Lebertransplantationen gehe ich von hoher Sheddingrate aus, bei anderen Organen ist das schwer zu sagen.
Hinweis, dass Inhalation, Hautkontakt (und Sperma?) ein Problem sein könnten findet sich in den Pfizer Unterlagen. Da handelt es sich sogar um Shedding zweiten Grades. Der Mann muss nur geshedded worden sein und dann seine schwangere Frau anfassen. Das wäre meldepflichtig gewesen.
Bei Speichel, Schweiß, Vaginalflüssigkeit, Tränenflüssigkeit und Sperma habe ich keine Daten. In Sachen Sperma gibt es aber den sperminenvermittelten Gentransfer, der in der Tierzucht eingesetzt wurde, um transgene Tiere zu erzeugen. Wenn also Exosomen mit modRNA an ein Spermium von außen adsorbieren… (https://en.wikipedia.org/wiki/Sperm-mediated_gene_transfer).
Bei Adenoviren jedoch weiß man, dass diese so shedden können.
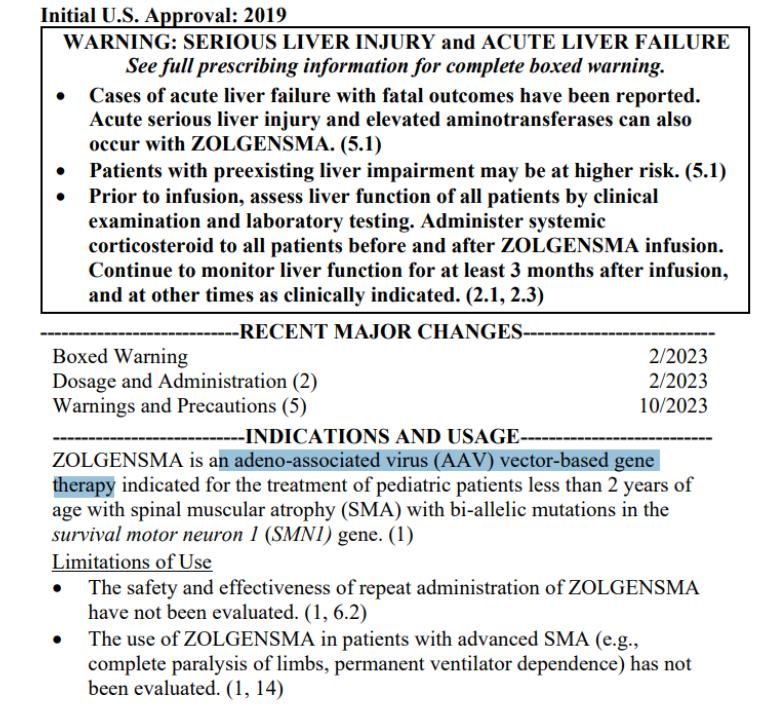
https://www.ema.europa.eu/en/documents/product-information/luxturna-epar-product-information_en.pdf
Das Sheddingproblem ist also nicht nur ein modRNA-Problem, es ist auch ein Adenoviren und somit AstraZeneca bzw. Johnson & Johnson Problem, das besonders interessant sein könnte, wenn das “Impfvirus” sich mit einem wildtypischen Adenovirus bei gleichzeitiger Infektion einer Zelle kreuzt. Das war es dann unter Umständen mit “nicht mehr replikationskompetent”. Kann passiert sein, es liegen dazu aber keine Daten vor.
Im vergleich zu Bluttransfusion, Transplantation oder Fötus einer gespritzten Mutter zu sein, wo das Produkt in die Blutbahn gerät, ist Inhalation und Hautkontakt immer noch weniger schlimm, weil sowohl Einatmen als auch Anfassen oder Küssen nur den Außenbereich des Körpers betrifft, der durch Schleimhäute oder Hautzellen geschützt ist (die erste Abwehrmauer der angeborenen Immunität), aber “informed consent” ist in diesem Zusammenhang sicherlich nicht gegeben worden.
q. e. d.
Direktes Shedden des Spike-Proteins
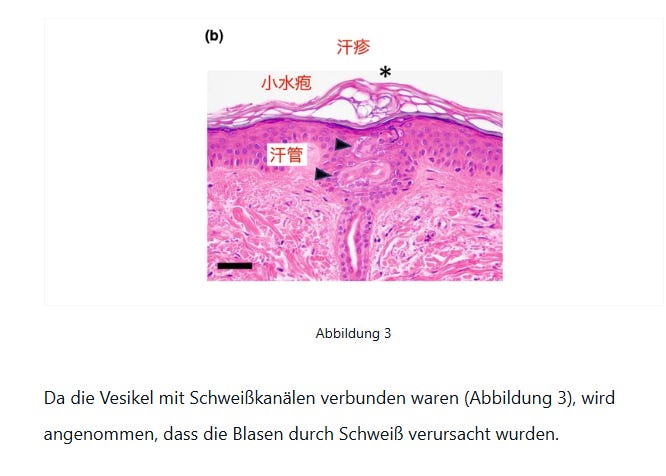
Das Spike-Protein kann direkt in Schweißdrüsen produziert werden und dann direkt über den Schweiß abgegeben werden. Wenn das Protein bei den betroffenen Hautprobleme verursacht, kann es somit wahrscheinlich auch bei Kontaktpersonen Hautprobleme (Kontaktdermatitis) erzeugen. Ein entsprechender Fall, bei der eine injizierte Person Spike-Protein in den Schweißdrüsen produziert(e), wurde in Japan berichtet (https://pubmed.ncbi.nlm.nih.gov/38558035/).
Das Paper ist hinter einer Paywall, der Autor hat aber einen japanischen Blog.(https://note-com.translate.goog/hiroshi_arakawa/n/n01bb10173540?_x_tr_sl=ja&_x_tr_tl=en&_x_tr_hl=de&_x_tr_hist=true)
Updates:
2.03.2024: Andere Arten des Sheddings über Körperflüssigkeiten + Shedding von Adenoviren + FDA Definition von Shedding + Inhaled RNA Therapy: From Promise to Reality - PubMed (nih.gov)
03.03.2024: Sperm-mediated gene transfer - Wikipedia




















Thank you Dr. Bine. If only 2% of LNPs are transfected then do we need to change our view of this from LNP/mRNA "immunisation" to an exosome based pro-drug technology, with all the grave pathophysiological implications and regulatory shortcomings?
I can't read German. Looks like a great informative article..