Woher stammt BioNTechs linearisiertes Plasmid wirklich?
Sind Anandamides Sequenzierergebnisse auf Deutschland übertragbar?
Update 7.05.2023: Per Mail kamen ein paar Infos rein, die ich aktualisiert habe. Danke an Jürgen K. (Ich weiß nicht, ober er seinen vollen Namen hier stehen haben will, daher kürze ich ihn mit „Jürgen K.“ ab, sonst habe ich zweimal „J.“, die mir zugearbeitet haben.)
Dies ist wieder einer dieser Artikel, die nicht auf meinem Mist gewachsen sind. Ich habe mittlerweile Informanten, die mir Informationen und Schreibprompts stecken, die ich dann so gut es geht überprüfe und mit Endnoten versehe. Ja, ich liebe Endnoten, wer hätte das nach meinen bisherigen Texten auch ahnen können.
Und ja, ich bin nicht allwissend und immer froh und dankbar über Informationen, die mir persönlich neu sind.
J. (Danke, wer auch immer Du sein magst), hat mir einige interessante Informationen als Schreibprompts zukommen lassen, die ich hier, so gut es geht, als intellektuelle Schreibübung zusammenfassen werde. Jürgen K. hat am 6.05.2023 einiges per Mail ergänzt.
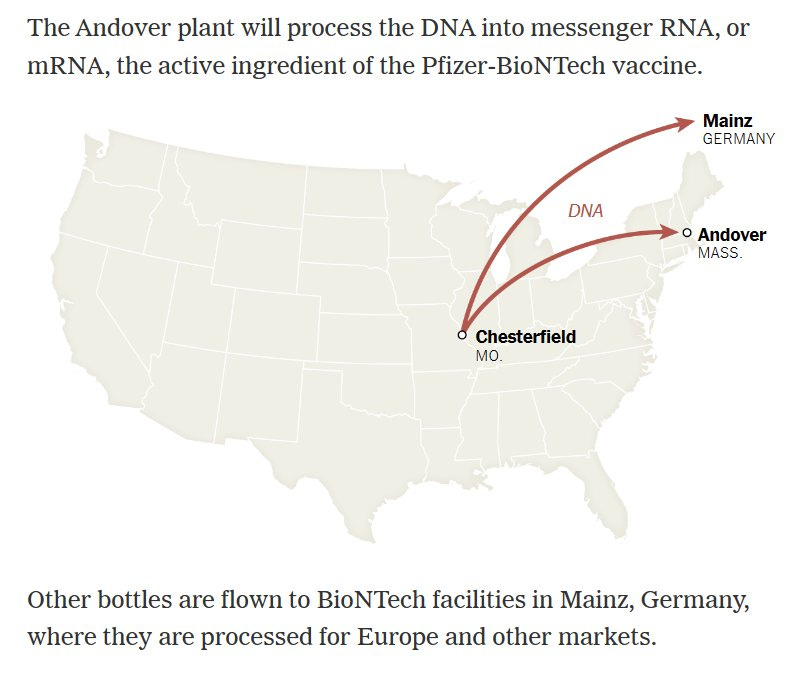
Bisher wurde angenommen, dass die Plasmide für die BioNDreck/Pfizer Plörre alle von Pfizer kommen. DAS zumindest behauptet die NYTimes[1], welche schreibt, dass die Plasmide aus einer Pfizer Fabrik in Chesterfield[2] kommen würden und von da aus nach Mainz und Andover (Massachusetts, USA), verschickt würden. Die NY Times schreibt, dass die Chesterfieldfabrik die einzige Quelle für Pfizers Plasmide für die Plörre wären. Gut, der Artikel behauptet auch, dass alle verbleibenden Plasmidrückstände rausgefiltert würden, was ja nachweislich falsch ist. Wer der NYTimes glaubt ist eigentlich selbst schuld, und dem ist auch nicht mehr zu helfen.
Zugegeben, ich kam auch nicht auf die Idee einfach "Biontech Herkunft DNA-Templates" zu googeln, zum einen, weil google mir normalerweise nicht mehr ausspuckt, was ich suche, sondern mich stattdessen mit Regierungspropaganda „beglückt“, zum anderen hätte man ja tatsächlich auf die Idee kommen müssen aktiv danach aktiv zu suchen, und nicht zu glauben, dass die Plasmide alle aus Chesterfield kommen. Vor allem, weil es in den Datenbanken zur Pfizerstudie und den Substacks auf denen ich mich herumtreibe, keinen Hinweis darauf gab, an Herkunft der Plasmide zu zweifeln. Man könnte sagen, ich war ein Schaf und habe der NYTimes geglaubt. Schande über mich.
J. hat mir nun den Namen einer anderen Firma zugespielt, die weder in Ugurs Buch „Project Lightspeed“ noch sonst irgendwo aufgetaucht ist: Biomay
Sucht man in den Pfizer Studiendaten nach dieser Firma mittels Dailyclout Abstractor Software[3] bekommt man keine Treffer. Nirgends ist diese Firma erwähnt, aber es gibt sie.
Biomay[4] ist, genau wie Polymum, eine österreichische, um genau zu sein Wiener Firma, zu deren Repertoire die Plasmidherstellung gehört.
Nun wird es komplexer.
Beginnen wir damit, was wir in Project Lightspeed zu diesem Thema finden:
Am 23. Dezember kam eine E-Mail, die die zusätzliche Bestellung bestätigte. Monate später würde die Produktionsstätte, für die BioNTech zunächst ohne finanzielle Unterstützung gekämpft hatte, der EU helfen, das Gesicht zu wahren. Das Bundesgesundheitsministerium in Berlin hatte mit lokalen Behörden in der Nähe von Marburg zusammengearbeitet, sodass bis Februar 2021 der Standort genehmigt und in Betrieb genommen werden konnte.“ (S. 308, Project Lightspeed)
Tatsächlich ging die Produktion bereits Anfang 2021 in Betrieb:
„MAINZ, DEUTSCHLAND, 10. Februar 2021 (GLOBE NEWSWIRE) - Wir haben den Herstellungsprozess in der Marburger Anlage mit der Ausführung des ersten Schritts begonnen: der Produktion von mRNA, dem pharmazeutischen Wirkstoff des Impfstoffs COVID-19 von Pfizer-BioNTech. Eine einzige mRNA-Charge in der derzeitigen Größenordnung reicht aus, um etwa acht Millionen Impfstoffdosen herzustellen.“[5]
Zu diesem Zeitpunkt arbeitete man also möglicherweise tatsächlich mit Plasmiden aus Chesterfield.
D.h. aber auch, dass die ersten Impfkampagnen in Deutschland möglicherweise noch mit Pfizer Produkten durchgeführt wurden und nicht mit BioNTech Plörre, da BioNTech selbst in seiner Pressemitteilung schreibt, dass die ersten in Marburg hergestellten Chargen ab Anfang April zur Verfügung stünden und davor wohl vermutlich bis Ende April aufgrund der Produktionskapazitäten nur Kleinserien von BioNTech produziert wurden.
Kleinserien, woran erinnert mich das? Da war doch dieses dänische Paper, das herausfand, dass vor allem die Chargen kleiner Größe besonders tödlich waren[6], aus welcher Produktionsstätte diese wohl kamen? Kleinserien in Bierfassgröße?
„Zunächst mussten in einem Labor DNA-Sequenzen produziert werden, ein komplizierter und unwägbarer Prozess. Dann übersetzte Kuhns Team mit Hilfe von Bioreaktoren von der Größe eines Party-Bierfasses die DNA in mRNA, reinigte das Material mit Hilfe von Puffern, verpackte es und fror den Wirkstoff bei minus 70 Grad Celsius ein. Die Plastiksäcke – die genügend Flüssigkeit für ein paar tausend Dosen enthielten – wurden in spezielle Styroporboxen gepackt, die etwa so groß wie ein Koffer sind, aber Trockeneis enthalten, und an einen eigens dafür vorgesehenen Fahrer übergeben.“ (S. 273, Project Lightspeed)
Ab Mai jedoch kommt ein neuer Plasmidlieferand, namens Biomay, hinzu. Am 11. Mai 2021 gab Biomay bekannt, dass sie eine der Firmen wären, die BioNTech mit dem DNA-Template, also der DNA-Vorlage = Plasmid, bzw. linearisierte DNA, beliefern würden[7]. Eine der Firmen… Wie viele weitere Firmen es gibt kann man aktuell nicht sagen. Es gibt zumindest schon mal 2 Plasmidlieferanten: Pfizer (Chesterfield) und Biomay (Wien).
Wurde nun mit Plasmiden verschiedener Zulieferer parallel gearbeitet?
Laut meiner Informantin liefert Biomay BioNTech bereits linearisierte Plasmid-DNA für die zellfreie Produktion der modRNA. Wenn es also in Sequenzierungen deutscher oder türkischer Chargen auch Plasmide gäbe (wozu aktuell keinerlei Daten vorliegen, die aber angeblich bereits im Hintergrund erzeugt werden), dann wäre wohl nicht Pfizer oder Biomay in der Haftung, sondern BioNTech, wurde mir gesagt.
„Was Verunreinigungen in Arzneimitteln angeht, so ist arzneimittelrechtlich nicht entscheidend wie sauber das Startermaterial ist, sondern ob das Endprodukt die festgelegten Qualitätsanforderungen erfüllt. Im Klartext heißt das: Wenn in einem späteren Schritt sowieso DNA herausgeholt werden soll, warum sollen vorgelagerte Schritte das auf Kosten der Ausbeute ebenfalls zum Ziel haben? Für die Qualität des Endprodukts haften diejenigen, die das Endprodukt freigegeben haben. Beispielsweise in Marburg. Da nach der modRNA-Produktion sowieso die DNA von der modRNA abgetrennt werden muss, ist es dieser Schritt, der ggf. für die Gerichte relevant ist, denn erst nach diesem muss das Produkt hinsichtlich Verunreinigungen den festgelegten Grenzwerten genügen. Wenn also mit Plasmiden kontaminierte DNA-Templates verwendet wurden, kann das zwar ein vertragsrechtliches Problem zwischen dem Lieferanten und BioNTech sein, die Haftungsfrage in Bezug auf Dritte betrifft aber nur BioNTech bzw. die Produktion in Marburg […] Schuld im juristischen Sinne sind ggf. ausschließlich die Personen, die für die Inverkehrbringung des fertigen Arzneimittels gesorgt haben.“
BioNTech arbeitet in einem zellfreien System[8]. Zellfreie Systeme[9] sind im Prinzip verflüssigte Bakterienleichen. Schätzungsweise wird mit verflüssigten, toten E.Coli gearbeitet (die man dann euphemistisch „Lysat“ nennt), was die teils wohl noch vorhandenen Endotoxine erklären könnte, über die sich Geoff Pain mittlerweile mehrere Wochen in vielen, vielen Artikeln auf seinem Substack aufregt[10]. In diesen flüssigen E.Coli Leichen lässt man dann die modRNA herstellen. Man lässt die armen Bakterien also selbst nach ihrem Tod noch für die Pharma arbeiten. Wer liefert eigentlich dieses zellfreie Expressionssystem. Das wird doch sicherlich auch zugekauft? Ist das System validiert und GMP? Diese zellenfreien Systeme waren zu meiner Zeit damals noch sehr unzuverlässig und tückisch.
Verwendet wird bereits linearisiert gelieferter Plasmid dsDNA (doppelsträngige DNA), was so einige Tücken mit sich bringt, aber anders bekommt man den Austausch von Uracil gegen Pseudouridyl nicht hin, weil E.Coli dieses Synthetische Nucleotid nicht erstellt, weil es eben künstlich ist und in die Synthese von Extern zugesetzt wird (wer liefert das Nucleotid eigentlich? Ich frag ja nur.)
Wir wissen nun von Anandamide[11], dass die Pfizer Versionen der Plörre mit Plasmiden verunreinigt sind. (Anandamide ist übrigens Kevin McKernen und die Ergebnisse gibt es auch als Preprint Paper[12] und nicht nur als Substack. Da aber die Substack-Artikel unter dem Netznamen Anandamide zitiert werden, bleibe ich bei Anandamide, wenn ich aus seinen Substack zitiere.)
BioNTech in Marburg arbeitet wohl seit Mai/Juni 2021 auch mit bereits linearisierten Plasmiden von Biomay und nicht nur oder nicht mehr mit Plasmiden von Pfizer aus Chesterfield.
Folglich müssen die Ergebnisse von Anandamide nicht zwangsläufig auf Deutschland und die Türkei zutreffen, denn diese beiden Länder werden laut Vertrag von BioNTech und nicht von Pfizer beliefert[13] was so auch von Ugurs „Project Lightspeed“ auf Seite 250 bestätigt wird:
„Ugur und Özlem wollten, dass BioNTech den Impfstoff nach Deutschland und in die Türkei selber verkaufen durfte.“
ALLE internationalen Daten, die für die Plörre erzeugt wurden, sind also für Deutschland und Türkei nicht unbedingt übertragbar und das gilt somit auch umgekehrt!
Natürlich kann man nun argumentieren, die EMA hätte auch DNA Verunreinigungen angemerkt und wenn schon in USA alles verunreinigt ist, dann kann man davon ausgehen, dass das auch in Deutschland der Fall ist. Jedoch gilt offiziell noch zum einen die Unschuldsvermutung bis zum Beweis der Schuld, zum anderen können theoretisch durchaus andere Plasmide enthalten sein als im Rest der Welt oder es könnte sich bei der DNA-Verunreinigung um Bruchstücke bakterieller chromosomaler DNA handeln. Ohne Labordaten kann man aktuell nicht davon ausgehen, dass die Ergebnisse zwangsweise deckungsgleich sein müssen. Sie können es sein aber sie müssen es nicht sein. Aktuell (7.5.2023) wissen wir das einfach nicht.
Nun hat mir meine Quelle aber noch weitere Schreibprompts geliefert, das geht aber in Richtung Gerüchteküche.
„Im September hat Biomay von BioNDreck die Anweisung bekommen, dass die Herstellungsprotokolle für die linearisierten Plasmide außer Kraft gesetzt und archiviert werden sollen. Dürfen diese somit nach Ablauf von einem Jahr vernichtet werden?“
Jürgen K., der im Gegensatz zu mir und J. Ahnung hat von der „Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher Herkunft (Arzneimittel- und Wirkstoffherstellungsverordnung – AMWHV)[14]“ sagt dazu:
„Die Aufbewahrungsfrist für die Dokumentation jeder Charge steht in § 20 AMWHV, diese beträgt ein Jahr nach Ablauf des Verfallsdatums, aber mindestens 5 Jahre.“
Das kann ich alles leider nur so als Zitat stehen lassen und weder überprüfen noch kommentieren. Ich habe keine Ahnung von diesen Gesetzen und freue mich über Zuschriften, die mir Infos zutragen, mit denen ich arbeiten kann.
Ich vertraue J. und Jürgen K. an dieser Stelle, aber ich kann J. Aussage nicht auf ihren Wahrheitsgehalt hin überprüfen. Das Gesetzt kann man sich aber immerhin anschauen.
J. hat noch eine Korrelation entdeckt, die zumindest nachdenklich machen sollte:
Es gibt da einen gewissen Christoph Huber. „Huber ist einer der Gründer und Mitglied des Aufsichtsrats von BioNTech.“[15]
Im Biomay Aufsichtsrat gibt es einen Hans Huber[16].
Gut, Huber ist jetzt kein seltener Name, in Österreich der zweithäufigste und in Deutschland an Position 40[17]. Is aber schon auffällig, dass Christoph Huber aus Wien stammt, wo Hans Huber bei Biomay arbeitet.
Das muss nichts heißen. Ich kann aktuell kein Verwandtschaftsverhältnis nachweisen. Wäre aber interessant, da mal nachzuhaken.
Jürgen K. hatte zum Schluss noch einen Tipp für mich, der mir persönlich neu war.
Jedes EMA-Dokument kann über ASK EMA
https://www.ema.europa.eu/en/about-us/contacts/send-question-european-medicines-agency
bestellt werden. Man muss halt wissen, was man haben möchte.
[1] Cott, E., deBruyn, E., & Corum, J. (2021, May 3). How Pfizer Makes Its Covid-19 Vaccine. The New York Times. https://web.archive.org/web/20230101053651/https://www.nytimes.com/interactive/2021/health/pfizer-coronavirus-vaccine.html
[2] Praveen. (2017, July 2). Pfizer R&D Facility, Chesterfield, Missouri. Pharmaceutical Technology. https://www.pharmaceutical-technology.com/projects/pfizer-rd-facility-chesterfield/
[3] Pfizer's Documents - Public Health and Medical Professionals for Transparency (shinyapps.io) https://vaccines.shinyapps.io/abstractor/
[4] Biomay AG. (2023, March 4). Biotech one-stop manufacturer of mRNA, pDNA and recombinant proteins. https://www.biomay.com/
[5] Update on vaccine production at BioNTech’s manufacturing site in Marburg | BioNTech. (n.d.). BioNTech. https://investors.biontech.de/news-releases/news-release-details/update-vaccine-production-biontechs-manufacturing-site-marburg
[6] Schmeling, M., Manniche, V., & Hansen, P. R. (2023). Batch‐dependent safety of the BNT162b2 mRNA COVID‐19 vaccine. European Journal of Clinical Investigation. https://doi.org/10.1111/eci.13998
[7] Biomay-Admin. (2022, May 11). Biomay Cooperates with BioNTech to Supply DNA Template for COVID-19 mRNA Vaccine. Biomay AG. https://www.biomay.com/biomay-cooperates-with-biontech-to-supply-dna-template-for-covid-19-mrna-vaccine/
[8]„Single-stranded, 5’-capped messenger RNA produced using a cell-free in vitro transcription from the corresponding DNA templates, encoding the viral spike (S) protein of SARS-CoV-2 “ Ema. (2023, April 3). Comirnaty - European Medicines Agency. European Medicines Agency. https://www.ema.europa.eu/en/medicines/human/EPAR/comirnaty
[9] Wikipedia-Autoren. (2006). Zellfreie Genexpression. de.wikipedia.org. https://de.wikipedia.org/wiki/Zellfreie_Genexpression
[10] GeoffPainPhD. (n.d.). Archive - Geoff Pain PhD. https://geoffpain.substack.com/archive?sort=new
[11] Anandamide. (2023, March 8). Pfizer and Moderna bivalent vaccines contain 20-35% expression vector and are transformation competent in E.coli. Susbtack. https://anandamide.substack.com/p/pfizer-and-moderna-bivalent-vaccines
[12] McKernan, K., Helbert, Y., Kane, L. T., & McLaughlin, S. (2023). Sequencing of bivalent Moderna and Pfizer mRNA vaccines reveals nanogram to microgram quantities of expression vector dsDNA per dose. OSF Preprint. https://doi.org/10.31219/osf.io/b9t7m
[13] Kogon, R. (2023b, May 3). BioNTech’s 30 Billion Reasons. Brownstone Institute. https://brownstone.org/articles/biontechs-30-billion-reasons/
[14] AMWHV - Verordnung über die Anwendung der Guten Herstellungspraxis bei der Herstellung von Arzneimitteln und Wirkstoffen und über die Anwendung der Guten fachlichen Praxis bei der Herstellung von Produkten menschlicher Herkunft. (n.d.). https://www.gesetze-im-internet.de/amwhv/BJNR252310006.html
[15] Wikipedia-Autoren. (2019). Christoph Huber. de.wikipedia.org. https://de.wikipedia.org/wiki/Christoph_Huber#Weblinks
[16] Biomay AG. (2022, February 4). Management Team - Biomay AG. https://www.biomay.com/company/management-team/
[17] https://forebears.io/surnames/huber




"...Schuld im juristischen Sinne sind ggf. ausschließlich die Personen, die für die Inverkehrbringung des fertigen Arzneimittels gesorgt haben.“"
Verkehrbringer ist der Bund. Der Bund ist Eigentümer bis die Injektion im Arm ist. Soweit ich weiß, gilt das ab Werk. Inwieweit dann dennoch die Überwachung (mittels GPS in den Boxen) erfolgte, weiß ich nicht. In Empfang genommen wurden sie bis 22. Februar 2022 von der Bundeswehr, die auch für die Verteilung und die Versendung ins Ausland einschließlich Rücknahmen. Das Bundesgesundheitsministerium gab an, daß "die Zahl der schweren Nebenwirkungen" seit Ende 2020 bekann war (also aus den Studien). Hier gibt es eine gute Zusammenfassung von Maria Gutschi: https://www.bitchute.com/video/muB0nrznCAC4/
Spahn hat das Arzneimittlerecht geändert und Lauterbach hat diese Änderung bis Ende 2023 verlängert. Sie wußten, was sie tun.
Es wäre evtl. gut mal nach den Betriebsgenehmigungsverfahren (In RLP und Hessen) und den lt. FdS antwort in Hessen und BaWü zu fragen. In Idar Oberstein ist ja auch noch ein Werk und in der Kupferbergstraße abgesehen von der Goldgrube.
Hier noch ein Artikel zum Etikettenschwindel: https://www.corodok.de/krank-nach-der-impfung/
Vielen Dank für Ihre Arbeit!
Ein weiterer pDNA Zulieferer für Biontech ist das Unternehmen "AGC Biologics" (AGC Asahi Glass):
"Heidelberger Anlage von AGC Biologics liefert weitere Plasmid-DNA für COVID-19-Impfstoff (7. Juni 2021)" -> weitere heißt wohl in diesem Fall, dass schon zuvor geliefert wurde! Siehe auch Gewinnsprung bereits im Jahr 2020: https://www.northdata.de/AGC+Biologics+GmbH,+Heidelberg/Amtsgericht+Mannheim+HRB+335606
https://www.agcbio.com/news/agc-biologics-heidelberg-facility-to-further-supply-plasmid-dna-for-covid-19-vaccine
"AGC Biologics unterstützt BioNTech Omicron-basierten Impfstoffkandidaten mit pDNA-Ausgangsmaterial (8. Februar 2022)"
https://www.agcbio.com/news/agc-biologics-supports-omicron-based-vaccine-candidate-manufacturing-with-starting-material
Ab jetzt wird wohl In-House von Biontech in Marburg ein Teil der Plasmid-DNA hergestellt.
Übrigens nennen alle CDMOs, welche Plasmid-DNA (pDNA) herstellen das "Kind" beim Name: Es handelt sich dabei um eine Gentherapie. Nur durch die Definitionsänderung, dass es sich um keine Gentherapie handelt, wenn es ein Impfstoff ist, konnte dies so von BigPharma "gespielt" werden.
Ich gehe von weiteren Zulieferern von pDNA aus, da es weltweit einen Mangel gab und wie wild überall zugekauft wurde...
"Die Plasmidherstellung ist der Flaschenhals der genetischen Medizinrevolution (16. Okt. 2020)"
-> "Leider ist die Aufstockung der Produktionskapazität für Plasmid-DNA nicht trivial, und die DNA-Produktion ist zu einem Engpass für die Industrie geworden. Vertragshersteller, die Plasmid-DNA in GMP-Qualität anbieten können, haben lange Wartelisten und erhebliche Rückstände aufgebaut."
...
"Das Verfahren ist von Natur aus langsam und teuer, hat eine begrenzte Kapazität und ist anfällig für Chargenfehler."
...
"Der Reinigungsprozess ist ähnlich teuer, langsam und schwierig zu skalieren."
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7564888/
-----
Nächste Plasmid-Stufe: Doggybone-DNA (dbDNA) von Touchlight Genetics, Pfizer hat schon zugegriffen. -> "Optimaler Vektor: dbDNA™ kann lange, komplexe, instabile Sequenzen codieren, bakterielle Sequenzen eliminieren und hat ein starkes Expressionsprofil." -> bakterielle Sequenzen eliminieren, AHA!
https://www.touchlight.com/platform-technology/overview/