Christies Twitter Lehrgang zum Zeta-Potential
Das Zeta Potential und seine biologischen Folgen
Es braucht noch einen anderen Twitter Thread von Christie, um den vollen Umfang der Verunreinigungen und Ladungen der Nanolipide (NLP) zu verstehen.
Ein weiteres Puzzlestück für das volle Verständnis des Problems ist das Zeta Potential, also die Nettoladung der Lipidnanopartikel:
Dieser „Lehrgang“ auf Twitter umfasst aktuell mehrere Teile:
Teil 1 https://twitter.com/_HeartofGrace_/status/1707566809648353770
Teil 2 https://twitter.com/_HeartofGrace_/status/1709304826893345026
Teil 3 https://twitter.com/_HeartofGrace_/status/1710332556837847301
Teil 4 https://twitter.com/_HeartofGrace_/status/1711414416946708497
Teil 5 https://twitter.com/_HeartofGrace_/status/1712100706906206488
Teil 6 https://twitter.com/_HeartofGrace_/status/1713183770734403666
Teil 7 https://twitter.com/_HeartofGrace_/status/1713604114175717823
Teil 8https://twitter.com/_HeartofGrace_/status/1713885468318630273
Teil 9 https://twitter.com/_HeartofGrace_/status/1713928455597740265
Teil 10 https://twitter.com/_HeartofGrace_/status/1713951401359945946
Teil 11 https://twitter.com/_HeartofGrace_/status/1714311685396148652
Teil 12 https://twitter.com/_HeartofGrace_/status/1714323978762719396
Teil 13 https://twitter.com/_HeartofGrace_/status/1715953903836049595
Es ist stilistisch offensichtlich, dass diese Texte für ein anderes Medium (Twitter bzw. X) geschrieben wurden.
D.h. die Texte sind meist kurze Sätze und Umgangssprachlich. Wortspiele, die auf Deutsch nicht funktionieren und Grüße an andere Twitternutzer, bzw. Seitenhiebe für Insider habe ich entfernt.
Zudem sollten Tweets auch einzeln funktionieren und Threads auch. Daraus folgen zwangsläufig sehr viele thematische Wiederholungen, da man im Normalfall seltenst alle Threads hintereinander an einem Stück gelesen hat, bzw. nicht immer alle Threads gefunden und verfolgt hat. Bei X/Twitter sind daher diese ständigen Wiederholungen durchaus sinnvoll.
Manchmal bin ich nicht Christies Meinung und merke das dann auch an, lasse aber ihren Originaltext stehen. Vielleicht liege ja ich falsch, daher greife ich nicht korrigierend ein. Sie ist die Expertin, ich der Schüler. Korrektur und Zusammenfassen traue ich mir bei meinem aktuellen Wissensstand nicht zu, da ich inhaltlich nichts verfälschen will.
Ich hatte im Anglistikstudium Übersetzungskurse. Ich weiß daher, dass ich nicht so arbeite, wie man sollte. Ich mache mir das Leben leicht mit KI Übersetzung und glätte nur sprachlich, wo es zu holperig wird. Ich passe den kulturellen Kontext nicht an die Leserschaft an. Ich lasse die Originallinks zu den englischen Quellen, die Christie genutzt hat, statt ein deutsches Äquivalent zu suchen, das gleiche gilt für die Bilder.
Das würde man in einer ordentlichen Übersetzung natürlich anders machen. Aber das ist nicht der Sinn dieses Substacks. Hier soll deutschen Lesern, die des Englischen nicht mächtig sind, der fachliche Inhalt möglichst originalgetreu vermittelt werden ohne Anspruch auf eine fachgerecht ausgeführte Übersetzung.
Man unterschätzt schnell, wieviel Inhalt über Twitter tatsächlich in dieser Form vermittelt werden kann. Das wird einem erst bewusst, wenn man diese Inhalte in ein anderes Medium, wie Substack oder eine Word-Datei, überträgt.
Der „Lehrgang“ läuft noch und wird in diesem Substack fortlaufend aktualisiert werden.
Für all jene, die keine Lust haben, alles durchzulesen, hier die Zusammenfassung (wird auch laufend ergänzt), was ich bisher gelernt habe:
1. Die Ladung der LNP bestimmt elektrostatisch, wo im Körper der Partikel endet. Nichts kann das verhindern, auch keine Aspiration.
Positive LNP gehen in die Lunge
Neutrale LNP (ca. -3mV) gehen in die Leber und andere Bereiche des Körpers verteilt
Negative LNP gehen in die Milz
Stark negative LNP gehen ins Gefäßsystem (HERZ, Vene, Arterie). Stark negative LNP verursachen ebenfalls Blutklumpen (Bindung an den Thrombozytenfaktor 4), Schaffung einer PROTEIN-KORONA (das LNP bindet sich an Albumin, andere Plasmaproteine), mögliche Verletzungen und Spikeexpression im Endothel der Gefäße.
2. Die Debye-Länge (die Dicke der elektrischen Doppelschicht um geladene Teilchen in einer Lösung) ändert sich, wenn sich die Ionenstärke, die Proteininteraktionen oder die pH-Bedingungen im Körper ändern. Schwankungen treten auf, wenn Liposomen mit verschiedenen Körperflüssigkeiten/Geweben interagieren, und sie können das Verhalten und die Stabilität liposomaler Arzneimittelabgabesysteme beeinflussen.
3. Kleinere LNPs (50 nm) weisen aufgrund seines höheren Oberflächen-Volumen-Verhältnisses einen stärkeren Oberflächenladungseffekt auf. Das bedeutet, dass der kleinere LNP, der einzelne LNP, mit einer nicht neutralen Ladung, entweder positiv oder negativ, MEHR an Dinge bindet, MEHR aggregiert, mehr Schaden anrichtet (wenn er Schaden anrichtet) und im Vergleich zu den größeren dazu insgesamt mehr Schaden anrichtet (es sei denn, Aggregation – Blockaden – Aneurysma, LNP aggregiert und verbindet sich mit anderen Dingen).
4. Der Gerinnungsprozess ist in Gegenwart negativ geladenen Liposomen, auch bekannt als LNP, tausendmal aktiver!
=== Teil 1 ===
Wie die Oberflächenladung (Zeta-Potential) des LNP bestimmt, wohin es im Körper gelangt (in die Leber und dann in die Milz oder direkt ins Herz oder in die Lungen), und warum dies mehrere Arten von Nebenwirkungen erklärt, einschließlich der jüngsten, fatalen Herzstudie, über die hier berichtet wird.
Ladungen: Schaut euch das Video an (zur Auffrischung für einige): Dieses Video (Mr. Anderson) erklärt, wie positive (+), negative (-) und neutrale (0) Elemente zusammenwirken. Wie sich sogar etwas mit einer +Ladung an etwas NEUTRALES ANLAGEN kann.
Er versucht, einfache Erklärungen für alle zu verwenden.
LNP: Meine alberne Zeichnung. Es werden NICHT ALLE Lipide besprochen. WIR FOKUSSIEREN uns auf die LADUNG.
Das ROTE rückwärts gerichtete S= negativ geladene mod RNA (-). Das GRÜNE Plus (+) ist ein POSITIV geladenes ionisierbares Lipid. Sie kleben aneinander (besseres Bild enthalten). Außerdem: Pfizer's Dokument: zeta= -3 mV.
Sehen Sie sich das Video NUR an, wenn Sie sich mit Wissenschaft auskennen. In dem Video/der Studie nahmen die Wissenschaftler LNP mit RNA (-) und pos. Lipiden (+) und injizierten sie in Mäuse - verschiedene Arten von LNPs - einige mit gleichem (-)/(+)=neutralem Potential, einige mehr (+), einige mehr (-), einige SEHR negativ (--), und verfolgten, WO im Mäusekörper die LNP/RNA hinging, entsprechend der Ladung. Das Zeta-Potential ist kompliziert. Es hat Faktoren: GRÖSSE der LNP, Menge der positiven (+) und negativen (-) Ladungen darin, Oberflächenladung (äußere Schicht) im Verhältnis zum pH-Wert und andere Dinge. Dies ist der Einfachheit halber verwässert.
Die Wissenschaftler der Firma NANO und ANDERE (keine Verschwörungstheorie, nicht meine Theorie) fanden heraus, dass, wenn sie das Verhältnis von positiven (+) zu negativen Ladungen (-) innerhalb der LIPID-NANOPARTIKEL anpassten, das LNP NICHT in die LEBER ging und sich dort verteilte, wie ursprünglich angenommen.
(*Anmerkung DrBine: Quelle zur NANO Studie hatte ich angefragt, mittlerweile hat Christie mich auf Twitter aber leider gesperrt*)
Die Wissenschaftler fanden heraus, dass, wenn das LNP eine Oberflächenladung hat, die mehr oder minder NEUTRAL ist, es in die Leber geht und sich auf andere Bereiche des Körpers verteilt, wie in ersten Studien und klinischen Versuchen gesehen (ohne die DNA-Plasmide, ja?) Dies war mit einem Zeta-Potential von ca. - 3 Millivolt.
ABER wenn das LNP eine höhere (+) POSITIVE LADUNG hat, geht es NICHT in die LEBER und verteilt sich - es geht in die LUNGEN. WENN es eine geringfügig negative (-) Ladung hat, geht es in die Milz. Wenn es MEHR NEGATIV (--) hat, kann es ins Gefäßsystem (HERZ, Vene, Arterie) entweichen und Schlimmes verursachen.
Kranz LM, Diken M, Haas H, Kreiter S, Loquai C, Reuter KC, Meng M, Fritz D, Vascotto F, Hefesha H, Grunwitz C, Vormehr M, Hüsemann Y, Selmi A, Kuhn AN, Buck J, Derhovanessian E, Rae R, Attig S, Diekmann J, Jabulowsky RA, Heesch S, Hassel J, Langguth P, Grabbe S, Huber C, Türeci Ö, Sahin U. Systemic RNA delivery to dendritic cells exploits antiviral defence for cancer immunotherapy. Nature. 2016 Jun 16;534(7607):396-401. doi: 10.1038/nature18300. Epub 2016 Jun 1. PMID: 27281205. https://pubmed.ncbi.nlm.nih.gov/27281205/
Cheng Q, Wei T, Farbiak L, Johnson LT, Dilliard SA, Siegwart DJ. Selective organ targeting (SORT) nanoparticles for tissue-specific mRNA delivery and CRISPR-Cas gene editing. Nat Nanotechnol. 2020 Apr;15(4):313-320. doi: 10.1038/s41565-020-0669-6. Epub 2020 Apr 6. PMID: 32251383; PMCID: PMC7735425. https://pubmed.ncbi.nlm.nih.gov/32251383/
(*Anmerkung Dr. Bine Kontext: Schaut man sich das vollständige Bild der BioNTech Publikation von 2016 an, sieht man in der Bildüberschrift, dass negativ geladene LNP über den ganzen Körper in dendritische Zellen verteilt werden. Durch die DNA-Verunreinigung sind die LNP höchstwahrscheinlich negativ geladen. Soviel zum Thema bleibt an der Einstichstelle.*)
Wenn die Ladung positiv (+) ist, gelangt das LNP direkt in die Lunge. Es spielt keine Rolle, ob Sie aspirieren! Dies geschieht durch eine Injektion in den MUSKEL, nicht nur durch eine IV. MUSKEL. Das LNP könnte eine Verletzung der Lunge verursachen. Wenn es ein wenig negativ ist, geht es in die Milz. Wenn es SEHR negativ ist, geht es zum HERZ.
Folgendes kann auch verursacht werden, wenn die Ladung sehr negativ ist: Blutklumpen (Bindung an den Thrombozytenfaktor 4 - nachgewiesen in der AstraZeneca-Studie), Schaffung einer PROTEIN-KORONA (das LNP bindet sich an Albumin und andere Plasmaproteine) - mögliche Verletzungen und Spikeexpression im Endothel der Gefäße.
(*Anmerkung DrBine: Hier hat Christie einen Gedankensprung, den sie nicht erklärt. Virenpartikel sind scheints auch negativ geladen und legen sich zum Schutz vor der Erkennung durch das Immunsystem eine Corona zu. DAHER hat der Vektorimpfstoff wohl einen ähnlichen Effekt wie ein LNP*)
Schauen wir uns nun den grundlegenden Aufbau der LNP in sehr einfachen Worten an, damit möglichst viele ihn verstehen. LNP besteht aus Cholesterin, DSPC, "unprotonierten" (noch nicht von H+ geladenen) ionisierbaren Lipiden, geladenen (+) Lipiden, PEG und modRNA (-) Ladung.
Wie oben zu sehen ist, baut sich das LNP selbst zusammen (dieser Begriff wird von einigen falsch verstanden - das LNP baut sich im Labor aufgrund von Ladungen und Inhalten zusammen). Die Unternehmen müssen jedoch die "Ladung" der LNP ohne DNA-Plasmide gemessen haben. Sie taten dies mit in vitro Test (IVT).
(*Anmerkung DrBine: Robert Malone hat dazu schöne Vorträge auf Englisch, wo er die spontanne Aggregation der Partikel sehr gut erklärt:
, https://t.me/DrBines_verbales_Vitriol/1331,
*)
Dies ist eine alte Zeichnung, bevor bekannt wurde, dass die DNA-Plasmide vollständig und in Stücken vorhanden sind. Der lila Kreis in der Zeichnung ist das DNA-Plasmid. Das rote rückwärtige S ist immer noch modRNA, und das grüne Plus (+) sind positiv geladene Lipide.
Zunächst wurde angenommen, dass das LNP nur modRNA enthält.
Anstelle von modRNA und Lipiden in der Mischung befinden sich jedoch DNA-Plasmide in der Mischung, wenn die LNP gebildet werden. Die Messung des Zetapotentials (-3 mV) wurde mit einem Verfahren zur Herstellung von LNP und modRNA mit IVT (ohne Plasmide) durchgeführt. Daher ist die gemessene Ladung möglicherweise nicht genau.
Zwei Dinge könnten geschehen sein. Sie könnten DNA-Plasmidstücke haben (entschuldigen Sie die Plasmidkreise, da sie das DNA-Plasmid darstellen), die (-) von Pos-Lipiden (+) umgeben sind und ein Lipoplex bilden - nicht Teil der RNA-LNP-Struktur. ODER, DNA/RNA-Lipopolyplex (modRNA UND DNA im Inneren).
(*Anmerkung DrBine: Wenn sich nur Plasmid DNA im LNP befindet, bewegen wir uns genetisch in Bereich Gentherapie mit Plamsiden, was etwas ganz andres ist als modRNA- Behandlung welcher Art auch immer*)
Der DNA-Polyplex selbst sollte eine eher positive Ladung haben (die zur Lunge geht!). Und laut der Studie von precision nano und anderen geht eine hochgradig negative Ladung in das Gefäßsystem, was den zuvor beschriebenen Effekt erklären würde. Diese neue Studie wurde gerade veröffentlicht.
Krauson AJ, Casimero FVC, Siddiquee Z, Stone JR. Duration of SARS-CoV-2 mRNA vaccine persistence and factors associated with cardiac involvement in recently vaccinated patients. NPJ Vaccines. 2023 Sep 27;8(1):141. doi: 10.1038/s41541-023-00742-7. PMID: 37758751; PMCID: PMC10533894. https://www.nature.com/articles/s41541-023-00742-7
(*Anmerkung DrBine: Precision Nano hat so einige Studien auf der Homepage: https://www.precisionnanosystems.com/resources-and-community/knowledge-center/publications, welche sie wohl meint?*)
In dieser Studie heißt es: "
EN: "…VACCINE WAS NOT DETECTED IN THE MEDIASTINAL LYMPH NODES, SPLEEN, OR LIVER. VACCINE WAS DETECTED IN THE MYOCARDIUM IN A SUBSET OF PATIENTS VACCINATED WITHIN 30 DAYS OF DEATH."
DE: “... IMPFSTOFF WURDE NICHT IN DEN MEDIASTINALEN LYMPH-KNOTEN, MILZ ODER IN DER LEBER nachgewiesen. BEI EINER UNTERGRUPPE VON PATIENTEN, DIE INNERHALB VON 30 TAGEN VOR DEM TOD GEIMPFT WURDEN, WURDE DER IMPFSTOFF IM HERZMUSKEL NACHGEWIESEN."
EN: "Serious adverse complications due to these vaccines are uncommon and may include anaphylactic reactions, myocarditis, pericarditis, myocardial infarction, cerebral sinus thrombosis, stroke, pulmonary embolism, neuropathies, and autoimmune hepatitis"
DE: "Schwerwiegende unerwünschte Komplikationen durch diese Impfstoffe sind selten und können anaphylaktische Reaktionen, Myokarditis, Perikarditis, Myokardinfarkt, zerebrale Sinusthrombose, Schlaganfall, Lungenembolie, Neuropathien und Autoimmunhepatitis umfassen.“
Wir wissen aus Studien
Wenn man das Verhältnis von (+) geladenen Lipiden zu negativ geladener (-) modRNA verändert, ändert sich der Ort, an den sie im Körper gelangen. Die Kontamination von DNA-Plasmiden MUSS das ZETA-Potenzial und die Gesamtladung der LNP verändern, so dass sie manchmal in die Gefäße/Lunge gelangen.
Zusätzlich zu den DNA-Plasmiden, die das Zetapotenzial (die Ladung) verändern, könnte eine weitere Ursache darin bestehen, dass das LNP während des Gefrier-/Auftauvorgangs zerfällt und Teile austreten können, wodurch sich die Gesamtladung ebenfalls verändert. De et al haben dies nachgewiesen.
De A, Ko YT. Why mRNA-ionizable LNPs formulations are so short-lived: causes and way-out. Expert Opin Drug Deliv. 2023 Feb;20(2):175-187. doi: 10.1080/17425247.2023.2162876. Epub 2023 Jan 1. PMID: 36588456. https://www.tandfonline.com/doi/abs/10.1080/17425247.2023.2162876
Negative Ladungen verursachen auch Klumpen (negativ geladene Liposomen), wie oben gezeigt.
Die Einführung der negativ geladenen DNA-Plasmide mit einer Rate von Milliarden pro Dosis bei 100 bp (Basenpaar-Durchschnitt) muss eine Verschiebung von Zeta bewirken. Die Ladung verteilt sich wahrscheinlich UNGLEICHMÄSSIG, was die Heterogenität (Unterschiede) zwischen den Chargen und Fläschchen erklärt. Da die Ladung ungleichmäßig verteilt ist, gäbe es Abweichungen zwischen Chargen und Fläschchen. Die FDA muss sofort eine Untersuchung einleiten und den Vertrieb sofort stoppen.
Die DNA-Plasmide geben Anlass zu erheblicher Besorgnis.
=== Teil 2 ===
Debye-Länge und Zetapotenzial.
Es gibt zwei Hauptgleichungen, die bei kolloidalen Systemen zur Schätzung des Zetapotenzials verwendet werden.
Die Debye-Länge ist Teil dieser Gleichungen, und sie kann sich ändern!
Dies ist einer der Gründe, warum sich das Zetapotenzial ändern kann!
Als ich in der Vergangenheit das Zeta-Potenzial berechnet habe, habe ich absichtlich falsche Zahlen verwendet, um zu sehen, wer wirklich aufpasst, aber auch, um zu zeigen warum jede Art von Messung nur für diesen einen Moment in der Zeit gilt und die Umgebung, in der sich das LNP zu diesem Zeitpunkt befindet. Die Wechselwirkung kann sich ändern.
Hier ist die zuvor diskutierte Smoluchowski-Gleichung (ich werde jede einzelne auseinanderziehen, jede Maßeinheit erklären und warum sie wichtig ist, so gut ich kann.
ζ=2⋅η⋅Eμ⋅ε
Das ist die Smoluchowski-Gleichung
ζ ist das Zetapotenzial.
μ ist die elektrophoretische Mobilität des Partikels.
ε ist die Dielektrizitätskonstante des Mediums.
η ist die Viskosität des Mediums.
E ist das angelegte elektrische Feld.
(dies wird sehr umfangreich, daher wird es in viele verschiedene Themen aufgeteilt)
Hier ist die im letzten Thread besprochene Henry-Gleichung:
ζ=3⋅η⋅rH2⋅μ⋅ε
Wobei:
ζ =Zetapotential.
μ = elektrophoretische Mobilität des Teilchens.
ε = Dielektrizitätskonstante des Mediums.
η = Viskosität des Mediums.
rH= ist der hydrodynamische Radius des Teilchens.
Es sieht nach viel aus, aber das meiste ist Plug-and-Play-Algebra. Es sieht einfach so aus, als würde es dein Gehirn schmelzen, aber wenn du die Dinge langsam auseinandernimmst und einfach nur Zahlen einträgst, wird es schon klappen. Oder auch nicht.
Die Debye-Länge, benannt nach dem niederländischen Chemiker Peter Debye, ist ein Parameter in der Elektrochemie und Kolloidwissenschaft. Sie wird auch als Debye-Hückel-Screeninglänge bezeichnet. Die Debye-Länge (λ_D) ist die Dicke der elektrischen Doppelschicht um geladene Teilchen in einer Lösung.
Einfacher ausgedrückt: Wenn Teilchen in einer Flüssigkeit eine elektrische Ladung auf ihrer Oberfläche haben, bilden sie eine "Wolke" aus Ladung um sich herum. Die Debye-Länge gibt an, wie dick oder dünn diese Wolke ist. Ist die Debye-Länge kurz, befindet sich die Wolke in der Nähe des Teilchens, ist sie lang, erstreckt sich die Wolke weiter weg.
Der kleine Pfeil in der hellgrauen Region oben ist die Debye-Länge. Die Debye-Länge gibt an, wie weit die Auswirkungen dieser Ladungen reichen und wie die Ladungen Dinge wie die Teilchenbewegung und die Wechselwirkungen mit anderen geladenen Teilchen beeinflussen - wie ein LNP im Körper interagieren würde.
Die Debye-Länge ist bei der Berechnung des Zetapotenzials mit der Henry-Gleichung von größerer Bedeutung, da die Teilchen nicht ganz kugelförmig sind, und bei der Smoluchowski-Gleichung ist sie eher indirekt von Bedeutung, aber sie ist dennoch wichtig. Die Sache ist die, dass sich die Debye-Länge ändern kann!
Die Debye-Länge (λ_D) kann sich je nach der Ionenstärke der Lösung und den Eigenschaften der vorhandenen Elektrolyte ändern. Die Ionenstärke bezieht sich auf die Konzentration der geladenen Ionen (wie Natrium und Chlorid) in der Lösung.
Die Debye-Länge kann sich im Zusammenhang mit Liposomen, die im menschlichen Körper mit einem Arzneimittel interagieren, auf folgende Weise ändern:
Wenn ein Arzneimittel auf Liposomenbasis in den Blutkreislauf injiziert wird, kann die Ionenstärke der Umgebung variieren. Das Blut enthält verschiedene Ionen, deren Konzentrationen aufgrund von Faktoren wie Flüssigkeitszufuhr, Ernährung und medizinischen Bedingungen schwanken können.
Auswirkung auf λ_D: Eine Zunahme der Ionenstärke (höhere Ionenkonzentration) verkürzt tendenziell die Debye-Länge, während eine Abnahme der Ionenstärke (niedrigere Ionenkonzentration) sie verlängert. Die Debye-Länge um Liposomen in der Blutbahn kann sich also ändern, wenn sich die Ionenbedingungen im Körper ändern.
Im Blutkreislauf können Liposomen auf Proteine wie Albumin treffen, die an ihrer Oberfläche adsorbieren und eine "Proteinkorona" bilden können. Diese Proteinkorona verändert die Oberflächenchemie der Liposomen.
Die Adsorption von Proteinen kann die Zusammensetzung der Ionen in der Umgebung der Liposomen verändern, was sich wiederum auf die Debye-Länge auswirkt. Je nach Art und Umfang der Proteinbindung kann die Debye-Länge zunehmen oder abnehmen. Das PEGylierte Lipid soll Proteine im Blut und in anderen Bereichen des Körpers daran hindern, am LNP zu haften. Das PEG bildet eine sterische Barriere um das LNP, die verhindert, dass es mit anderen Dingen zusammenstößt, was aber nicht bedeutet, dass es nicht interagiert oder dass sich die Ladung nicht ändern kann.
Liposomen/LNP können so konzipiert werden, dass sie ihre Nutzlast in bestimmten Körperkompartimenten mit unterschiedlichen pH-Werten freisetzen. Einige Liposomen setzen beispielsweise Arzneimittel in der leicht sauren Umgebung von Tumorgewebe frei.
Änderungen des pH-Wertes können die Ionisierung der Moleküle in der Lösung beeinflussen. Änderungen der Ionisierung können sich wiederum auf die Debye-Länge auswirken. In Regionen mit unterschiedlichen pH-Werten kann die Debye-Länge um Liposomen entsprechend variieren.
Zusammenfassend lässt sich sagen, dass sich die Debye-Länge ändern kann, wenn sich die Ionenstärke, die Proteininteraktionen oder die pH-Bedingungen im Körper ändern. Schwankungen treten auf, wenn Liposomen mit verschiedenen Körperflüssigkeiten/Geweben interagieren, und sie können das Verhalten und die Stabilität liposomaler Arzneimittelabgabesysteme beeinflussen.
Selbst bei diesem einen Aspekt, der die Ladung auf der Oberfläche eines LNP betrifft, können sich die Dinge also ändern. Nichts existiert in einem Vakuum.
Als Pfizer diese Messung vornahm, fand sie in einem Labor statt, nicht in einem menschlichen Körper und auch nach dem Eintritt des LNP in den Körper kann sich alles ändern. Und damit meine ich wirklich ALLES!
=== Teil 3 ===
Die Oberflächenladung (Zeta) eines LNP bestimmt nicht nur, WO es im Körper hingeht, sondern auch WIE es mit verschiedenen Dingen interagiert. Viele Variablen beeinflussen die Zeta-Ladung.
Heute: Smoluchowski-Gleichung (Zeta):
η = Viskosität des Mediums.
Viskosität ist der Widerstand gegen das Fließen.
Die Viskosität sagt uns, wie dick oder "klebrig" eine Flüssigkeit ist. Einfacher ausgedrückt, bestimmt die Viskosität, wie leicht eine Flüssigkeit oder ein Gas fließt. Die Viskosität kann sich auf das Öl in Ihrem Auto beziehen. Meine Autos werden nur mit synthetischem Öl befüllt, weil synthetisches Öl einen höheren Geschwindigkeitsindex hat. Das bedeutet, dass sich die Viskosität weniger verändert und stabiler ist, wenn sich die Temperatur beim Anlassen des Motors und unter normalen Betriebsbedingungen ändert.
Dies hat mehrere Komponenten. Eine davon ist der Geschwindigkeitsindex, wenn es um Öl geht. Die meisten Öle werden dünner und weniger viskos, wenn sie erhitzt werden.
Die meisten Öle sind temperaturabhängig. Sie dicken ein, wenn sie abgekühlt sind, und verflüssigen sich, wenn sie erhitzt werden - aber nicht alle. Denken Sie zum Beispiel an Margarine (igitt).
Bei höheren Temperaturen ist sie flüssig. Bei Zimmertemperaturen und kühleren Temperaturen sind sie dickflüssiger. Bei Wärmezufuhr wird sie weniger zähflüssig. Der Geschwindigkeitsindex gibt an, wie stark sich die Viskosität eines Öls bei Temperaturänderungen ändert. Für den Viskositätsindex (VI) gibt es bestimmte Werte und bestimmte Werte werden für verschiedene Anwendungen bevorzugt. Für diejenigen unter uns, die 4 Jahreszeiten haben, verwenden wir im Sommer andere VI-Öle als im Winter.
Die Viskosität ist bei der Anwendung von LNP und Oberflächenladung (Zeta) SEHR wichtig, weil wir im menschlichen Körper unterschiedliche Viskositäten haben - ganz unterschiedliche. Zum Beispiel ist die Viskosität unseres Blutes ganz anders als die der Rückenmarksflüssigkeit (cerebrospinal fluid = CSF).
Im menschlichen Körper umfasst die Viskosität oder der Widerstand für die Blutzirkulation die Reibung zwischen den Blutbestandteilen sowie zwischen dem Gefäßlumen und dem Blut.
Nehmen wir als Beispiel MICH. Ich bin 1,80 Meter groß und 48 Jahre alt. Ich laufe viel. Ich trinke und rauche nicht. Ich nehme Blutverdünner. Ich habe eine niedrige Ruheherzfrequenz von 40, da ich über 40 Jahre lang Distanzläufer bin, und laut ärztlicher Aussage bin ich in hervorragender Cardio-Form. Mein Blutdruck liegt an den meisten Tagen bei 90/60. Ich habe einige gesundheitliche Bedenken, die jedoch keinen Einfluss auf diese Messung haben. Die Viskosität meines Blutes bei 37 °C (98,6 °F): Ungefähr 3,0 bis 4,5 Centipoise (cP).
Plasmaviskosität bei 37 °C: ca. 1,2 bis 1,4 Centipoise (cP).
Das ist ganz anders als meine Gehirn-Rückenmarks-Flüssigkeit.
CSF-Viskosität bei 37 °C: ca. 0,6 bis 1,0 Centipoise (cP).
DAS ist ein Unterschied! Das sind nur drei Parameter!
Jede Zahl in dieser Zeta-Berechnung ist entscheidend dafür, wie hoch die Oberflächenladung (Zeta) auf dem LNP ist, denn sie steht im Verhältnis zu dem, worin sich das LNP befindet!
Zeta ist NICHT immer statisch!
Centipoise (cP) entspricht einem Hundertstel (1/100) Poise
Wasser bei 20 °C (68 °F) hat eine dynamische Viskosität von etwa 1,002 Centipoise (cP). Dynamisch bedeutet Veränderung. Statisch bedeutet, dass sich das gleiche ZETA stabilisieren kann, aber statisch sein kann. Die pegylierten Lipide an der Außenseite des LNP wurden aus mehreren Gründen dort platziert. Aber sie sind keine Garantie (für irgendetwas).
Die Viskosität selbst ist KEINE Eigenschaft des Gehirngewebes. Knochen, Muskeln, Herz, Bindegewebe, Organe und andere Bereiche haben keine messbare Viskosität, es handelt sich eher um mechanische und elektrische Messungen.
Die AUGEN haben unterschiedliche Viskositäten.
Die Hornhaut hat eine niedrige Viskosität, da sie zur Befeuchtung Tränen produzieren muss.
Der wässrige Humor hat eine niedrige Viskosität, um den Druck im Auge und die Ernährung aufrechtzuerhalten. Die Linse besteht hauptsächlich aus Proteinfasern mit niedriger oder gar keiner Viskosität. Glaskörper: Höhere Viskosität, um die Form beizubehalten (Probleme bei Glaskörperablösung, Floatern, kommt irgendjemandem bekannt vor?) Netzhaut: Hier gibt es keine flüssigkeitsähnliche Viskosität. Andere Teile haben nicht viel Viskosität, außer dem Tränenfilm.
Der Wert für die Viskosität KANN also das Zeta-Potenzial, die Bioverteilung, wohin das LNP im Körper gelangt, und wie es interagiert, beeinflussen.
Gemäß der verwendeten Gleichung Höhere Viskosität (η): Wenn die Viskosität des Mediums, in dem sich das Teilchen bewegt, zunimmt, wird der Nenner in der Gleichung (η) größer. Dadurch würde das berechnete Zetapotential (ζ) sinken.
Eine höhere Viskosität verringert die elektrophoretische Mobilität und damit das Zetapotential. Eine höhere Viskosität senkt Zeta.
Wenn umgekehrt die Viskosität des Mediums abnimmt, wird der Nenner in der Gleichung (η) kleiner. Dies würde zu einer Erhöhung des berechneten Zetapotentials führen. Eine niedrigere Viskosität erhöht die elektrophoretische Mobilität und das Zetapotential.
Dies bedeutet, dass es indirekt proportional zum endgültig berechneten Zetapotential ist.
Kommen wir zurück zum BLUT und der RÜCKENMARLSFLÜSSIGKEIT.
Blut hat im Vergleich zu Liquor eine höhere Viskosität. Die höhere Viskosität von Blut kann im Vergleich zu Liquor zu einem geringeren Zetapotential führen.
Es gibt jedoch auch einen pH-Wert im Blut im Vergleich zu CSF sowie IONEN im Blut, in Proteinen, im Endothel und in anderen Molekülen, mit denen man zu kämpfen hat.
Das Zeta-Potenzial von Nanopartikeln kann auch durch die lokale Umgebung in verschiedenen Teilen des Körpers und durch Zellen, die Blutgefäße auskleiden, beeinflusst werden. Im Gegensatz dazu können Nanopartikel im Liquor unterschiedliche Wechselwirkungen innerhalb des Zentralnervensystems erfahren.
Als nächstes: pH-Wert und Ionen, die die potenzielle Bioverteilung von ZETA beeinflussen, und Wechselwirkungen im menschlichen Körper in verschiedenen Organen und Kompartimenten.
Interessant wird es, wenn Ionen und Proteine im Körper hinzukommen. ;)
=== Teil 4 ===
Das Zetapotential ist die Oberflächenladung auf LNP (und anderen Dingen!). Das Zeta-Potenzial bestimmt nicht nur, wohin der LNP im Körper gelangt, sondern auch, WAS der LNP bewirkt (Wechselwirkungen).
Das Zetapotential existiert nicht im luftleeren Raum. Es kann sich aufgrund vieler Faktoren ändern.
Heute: IONEN!
IONEN existieren im menschlichen Körper. Sie liegen nicht nur in Form von Metallen vor. In unserem Körper schweben Metalle herum. Natrium (Na+) ist ein Metall. Es hat eine positive Ladung von +1 genau wie Kalium (K). Natriumchlorid, was Sie essen, hat zwei miteinander verbundene Ionen, Cl- und Na+!
(IONENVERBINDUNG!)
Die Bindungen im Salz (Cl- UND Na+) werden als ionisch bezeichnet, da beide eine elektrische Ladung haben – das Chlorid-Ion (Cl-) ist negativ geladen und das Natrium-Ion (Na+) ist positiv geladen.
Diese Dinge können eine sogenannte „Stärke“ haben. Dies nennt man IONENSTÄRKE. UND diese variiert!
Die Ionenstärke misst die Menge an Ionen (geladenen Teilchen) in einer Lösung, ausgedrückt als Molarität (Mol Ionen pro Liter Lösung). Lösungen mit höherer Ionenstärke enthalten mehr Ionen, während Lösungen mit niedrigerer Ionenstärke weniger Ionen enthalten. Die Ionenstärke ist ein wichtiger Faktor bei der Berechnung des Zetapotentials, da sie die elektrischen Eigenschaften (Wohin das LNP geht und womit es interagiert) der Lösung (IHR KÖRPER, IHR GEWEBE, IHR BLUT) und die STABILITÄT geladener Teilchen (IN DIESEM FALL, DER LNP).
In einem früheren Thread habe ich die Debye-Länge erklärt, die für die Berechnung des Zetapotentials von entscheidender Bedeutung ist. Es ist die „Wolke“, über die wir gesprochen haben. Es definiert, wie weit der elektrische Einfluss eines geladenen Teilchens in die umgebende Lösung reicht und welche elektrostatischen Wechselwirkungen es mit anderen Dingen haben kann.
Die Debye-Länge (λ_D) kann berechnet werden:
λ_D = (ε * k * T) / (2 * N * e^2 * I)^0,5
λ_D ist die Debye-Länge.
ε: Permittivität des Lösungsmittels
k: Boltzmanns Konstante.
T: absolute Temperatur.
N: Avogadros Nummer.
e: Elementarladung.
I: Ionenstärke der Lösung
Ist es offensichtlich, dass bei ZETA und der geladenen Oberfläche des LNP viele Faktoren eine Rolle spielen, die bestimmen, wohin es im Körper gelangt und was es tut?
Die Debye-Länge ist umgekehrt proportional zur Quadratwurzel der Ionenstärke (I). Mit zunehmender Ionenstärke nimmt die Debye-Länge ab, und mit abnehmender Ionenstärke nimmt die Debye-Länge zu.
In Lösungen mit höherer Ionenstärke (MEHR IONEN) ist die Debye-Länge kürzer und elektrostatische Wechselwirkungen zwischen geladenen Teilchen sind stärker lokalisiert.
Lokalisierter: Dies bedeutet, dass die Art und Weise, wie geladene Teilchen aufeinander „einwirken“, auf eine kürzere Entfernung innerhalb der Lösung beschränkt ist. WAS das für LNP und Zeta bedeutet: Wenn Sie ein LNP in einer Lösung mit HÖHEREN Ionen (wie Blut) haben, ist die Debye-Länge in der Lösung relativ kurz. Dies bedeutet, dass elektrostatische Wechselwirkungen zwischen LNPs mit einer Ladung (- oder +) und anderen geladenen Teilchen wie Ionen oder Proteinen nur über eine kurze Reichweite wirken. Nur auf diejenigen Teilchen in ihrer unmittelbaren Nähe. ABER! (Sehen Sie, warum das in gewisser Weise tatsächlich SCHLECHTER ist?) WENN diese Debye-Länge in den Blutgefäßen oder Venen (oder im Herzen? Hallo!) LÄNGER ist, kann sich der elektrische Einfluss geladener LNPs über eine größere Entfernung innerhalb der Lösung (Blut/GEWEBE). Eine Änderung der Debye-Länge kann besorgniserregende Auswirkungen auf das Verhalten und die Wechselwirkungen geladener Teilchen (LNP) haben.
Dies kann jedoch je nach Situation gut oder schlecht sein. Wenn es bei dieser Ladung eine höhere Debye-Länge gibt, und sagen wir, sie ist negativ, dann besteht eine höhere Chance, dass sie andere negativ geladene Dinge abstößt (einige Proteine tun das) oder Dinge mit entgegengesetzter Ladung anzieht (PF4)!
Der Thrombozytenfaktor 4 (PF4) ist ein 70 Aminosäuren langes Protein, das in Alpha-Granula von Blutplättchen gespeichert und bei der Blutplättchenaktivierung freigesetzt wird.
PF4 ist kationisch oder positiv geladen und bildet bei physiologischem pH-Wert und physiologischer Ionenstärke Tetramere (dies wird später erklärt).
Scully M, Singh D, Lown R, Poles A, Solomon T, Levi M, Goldblatt D, Kotoucek P, Thomas W, Lester W. Pathologic Antibodies to Platelet Factor 4 after ChAdOx1 nCoV-19 Vaccination. N Engl J Med. 2021 Jun 10;384(23):2202-2211. doi: 10.1056/NEJMoa2105385. Epub 2021 Apr 16. PMID: 33861525; PMCID: PMC8112532. https://pubmed.ncbi.nlm.nih.gov/33861525/
EN: "VITT occurs when antibodies attack a blood protein called platelet factor 4 (PF4). This activates platelets in the blood, causing them to clump together and form clots, the study authors explained."
DE: „VITT tritt auf, wenn Antikörper ein Blutprotein namens Thrombozytenfaktor 4 (PF4) angreifen. Dadurch werden Blutplättchen im Blut aktiviert, was dazu führt, dass sie zusammenklumpen und Gerinnsel bilden, erklärten die Autoren der Studie.“
Viele Blutproteine wie Albumin, Globuline und einige Enzyme tragen eine POSITIVE Ladung. Die Ladung von Proteinen wird durch das Gleichgewicht der positiv und negativ geladenen Aminosäurereste innerhalb ihrer Struktur bestimmt.
Hämoglobin: POSITIVE LADUNG.
Verschiedene Partikel und Metaboliten im Blut, wie Aminosäuren, Peptide und einige Hormone, haben eine positive Nettoladung! Es wäre schrecklich, wenn ein LNP aufgrund einer NEGATIV GELADENEN DNA-Plasmidkontamination eine höhere negative Ladung erhalten würde.
Oberfläche im Verhältnis zu ihrem Volumen im Vergleich zu größeren Partikeln. Die Oberflächenladung verteilt sich über die gesamte Oberfläche des LNP. Mit abnehmender Größe des LNP nimmt die Oberflächenladungsdichte zu. Was könnte also schlimmer sein: KLEINES LNP oder GROSS?
Kleinere LNP erfahren aufgrund der höheren Oberflächenladungsdichte STÄRKERE elektrostatische Wechselwirkungen mit Ionen IM KÖRPER. Dies führt zu erheblichen Abstoßungs- oder Anziehungskräften zwischen Partikeln, abhängig von ihrer Oberflächenladung und der Ladung umgebender Ionen.
LNP unterschiedlicher Größe können unterschiedliche Neigungen zur Aggregation (Verklumpung) oder zur Wechselwirkung mit Partikeln im Körper haben. Aggregation kann das effektive Zeta-Potenzial der Partikelcluster verändern und ZETA VERÄNDERN!
(*Anmerkung DrBine: Zu diesem Bild fehlt leider die Quelle im Tweet. Ich habe nachgefragt und bin daher nun gesperrt? Bilder ohne Quelle und Kontext finde ich schwierig.*)
Die LNPs variieren in der Größe, bevor es zu einer Aggregation oder Absorption eines Lipids (Ostwald-Effekt), einer Ausflockung oder einer Ionenverbrückung kommt (siehe anderen Thread).
Das Zetapotential kann bei der Messung für Partikel unterschiedlicher Größe im Bereich von 50 nm bis 200 nm aufgrund größenabhängiger Faktoren und Wechselwirkungen mit dem umgebenden Medium (Blut, Gewebe, Lösung, Gehirn, Organe usw.) unterschiedlich sein.
Der kleinere LNP (50 nm) weist aufgrund seines höheren Oberflächen-Volumen-Verhältnisses einen stärkeren Oberflächenladungseffekt auf. Das bedeutet, dass der kleinere LNP, der einzelne LNP, mit einer nicht neutralen Ladung, entweder positiv oder negativ, MEHR an Dinge bindet, MEHR aggregiert, mehr Schaden anrichtet (wenn er Schaden anrichtet) und im Vergleich zu den größeren dazu insgesamt mehr Schaden anrichtet (es sei denn, Aggregation – Blockaden – Aneurysma, LNP aggregiert und verbindet sich mit anderen Dingen).
NÄCHSTES: Was passiert, wenn das LNP mit anderen Dingen BINDET, und wie diese nun mit ZELLREZEPTOREN interagieren können.
=== Teil 5 ===
Das PEG, ZETA-POTENZIAL UND DIE BILDUNG EINER NEUEN BIOLOGISCHEN IDENTITÄT:
Wie LNP zu einer „PROTEIN CORONA“ werden kann (*eine Protein Corona ausbilden kann?*), mit dem Immunsystem, anderen Körperteilen und Zellrezeptoren interagieren kann und auch (CHARGENABHÄNGIG!) zu UNERWÜNSCHTEN EREIGNISSEN UND VERLETZUNGEN führen kann.
Das PEG ist eine „sterische Barriere“, wie ein Regenschirm, um es davon abzuhalten, mit anderen Molekülen, wie geladenen Teilchen, zu interagieren. Proteine können Ladung haben! Das PEG hält das LNP auch länger im Umlauf, da es vor dem Immunsystem verborgen ist, wie eine Tarnvorrichtung auf einem Raumschiff.
Das LNP kann jedoch immer noch mit anderen Dingen im Körper interagieren. Wir wissen, dass sich LNPs nicht gleichmäßig bildet und es Kristallisationsprobleme gibt, aber auch Variationen beim PEG außerhalb des LNP! Dies hat viele Konsequenzen für das LNP und den menschlichen Körper.
Diese Studie fand extreme Unterschiede in der Menge an PEG auf der Außenseite der LNP, und auch wenn es WENIGER PEG-Moleküle (PEG hat immer noch bedenkliche Eigenschaften) auf der Außenseite der LNP sind, korrelieren die kürzeren PEGs mit Chargen mit höheren unerwünschten Ereignissen und Verletzungen von Menschen.
NEUE BIOLOGISCHE IDENTITÄT UND VERSCHIEBENDES ZETA-POTENZIAL, DAS ZU UNERWÜNSCHTEN EVETS/VERLETZUNGEN FÜHRT
(KOMBINIERT MIT DNA-Plasmid-Kontamination):
Der LNP besteht wie gesagt aus vielen Teilen, aber die hier gezeigten Fotos sind bei weitem nicht repräsentativ für ALLE LNPs. Sie werden variieren!
(Bitte entschuldigen Sie meine schlechten Zeichnungen):
Das rote S nach hinten ist die modRNA (-) und das grüne (+) sind positiv geladene, ionisierbare kationische Lipide, die aneinander gebunden sind [denken Sie auch daran, dass Verunreinigungen in (+) Lipiden Mutationen verursachen (Packer et al., 2021).
(* Ich schätze, sie meint dieses Paper mit Pater et al., 2021)
Packer M, Gyawali D, Yerabolu R, Schariter J, White P. A novel mechanism for the loss of mRNA activity in lipid nanoparticle delivery systems. Nat Commun. 2021 Nov 22;12(1):6777. doi: 10.1038/s41467-021-26926-0. PMID: 34811367; PMCID: PMC8608879. https://pubmed.ncbi.nlm.nih.gov/34811367/
Lila Linien sind jetzt lineare DNA
Allerdings können „Dinge“ durch Anziehung (Ladungen – Gegensätze ziehen sich an), über Van-der-Waals-Kräfte, Absorptionskinetik (größere Mengen an Proteinen um LNP herum lagern sich SCHNELLER an LNP an), erhöhte Temperaturen, hydrophile/ hydrophobe Wechselwirkungen, zur Bildung einer neuen Entität führen.
In der Studie wurde festgestellt, dass das PEG im LNP nicht in der Menge vorhanden war, in der es vorhanden sein sollte. Und mit der DNA im Inneren wird die Oberflächenladung (möglicherweise) bereits NOCH negativer werden. Das bedeutet, dass das LNP an Proteine im Blut, wie zum Beispiel Albumin, haften könnte. (*oder das Albumin an das LNP?*)
(Albumin in Rot)
Albumin ist ein Protein im Blut. Es hat eine negative Ladung. Es gibt viele Dinge im Blut (und im Körper), die an ein LNP binden können. Wenn Proteine an einem LNP haften, spricht man von Opsonisierung. Wenn Albumin am LNP haftet, kann es eine noch HÖHERE negative Ladung haben und MEHR unerwünschte Ereignisse wie Gerinnung, Immunreaktionen, Thrombose und Hyperkoagulabilität, endotheliale Dysfunktion (erneute Gerinnselbildung), Anti-Phospholipid-Syndrom (APS) usw. verursachen Bindung an bestimmte Zellrezeptoren!
(*Anmerkung DrBine: Moderna hat in seinem Börsenbericht 2018 von Opsonierung als Problem berichtet. Das könnte sich auf die schlechten Erfahrungen von Moderna mit der ALC-Plattform und der damit einhergehenden Opsonierung beziehen: https://www.sec.gov/Archives/edgar/data/1682852/000119312518323562/d577473ds1.htm S. 33*)
Insbesondere Albumin macht 60 % des Plasmas aus.
(*Anmerkung DrBine: Jessica Rose tippt auf ApoE, wie bei Onpattro*)
Albumin hält den osmotischen Druck (onkotischer Druck) im Blutkreislauf aufrecht. Dieser Druckgradient ist wichtig für die Aufrechterhaltung des Flüssigkeitsgleichgewichts zwischen Blutgefäßen und Geweben, des pH-Werts und des Natriumspiegels! Es fungiert als Puffer für den pH-Wert im Blut und kann auch als Ligand fungieren.
Wenn das LNP noch negativer wird, kann es bei der Injektion in den Muskel in das gesamte Gefäß gelangen (Aspiration spielt keine Rolle) und sich an den Thrombozytenfaktor 4 (PF4) BINDEN, was zur Bildung von Blutgerinnseln führt.
Außerdem hat uns Dr. Geoff Pain vor der Kontamination mit Endotoxinen gewarnt, die durch die Verwendung nicht gefilterter Plasmide entsteht, die in E. coli „gezüchtet“ werden, von dem bekannt ist, dass es Bakterien namens Endotoxin enthält.
(*Anmerkung DrBine: Korrektur: Es enthält keine Bakterien namens Endotoxine, sondern Endotoxine sind Bestandteil der Membran gram-negativer Bakterien, zu denen E.Coli gehört*)
Dieses Bakterium (*Korrektur: Das Endotoxin https://drbine.substack.com/p/sind-die-kationischen-nlp-nun-inflammatorisch *) HAT AUCH EINE NEGATIVE LADUNG und kann an der Außenseite des LNP haften, was auch dazu führt, dass das ZETA-POTENZIAL NEGATIVER ALS ZUVOR WIRD UND eine noch seltsamere biologische Identität annimmt, die nun in der Lage ist, noch mehr Blutgerinnsel, Infektionen und hohe Konzentrationen zu verursachen Sie können eine Immunantwort hervorrufen, die Eigenschaften anderer Dinge in ihrer Umgebung verändern, unerwünschte Ereignisse und Immunreaktionen hervorrufen und verschiedene molekulare Reaktionen im Körper auslösen, die Schaden anrichten.
Und weil es jetzt zu einer Verschiebung des Zeta-Potentials, der Oberflächenladung, kommt, wird das LNP sich in verschiedene Bereiche im Körper bewegen – die Ladung treibt die Bioverteilung UND die Interaktionen mit den Zellen im Körper an, und JETZT haften zusätzlich Proteine daran. Der Haken und Bakterien Endotoxine – schlechte Nachrichten.
(Anmerkung DrBine: Der endgültige Laborbeweis für Endotoxinbelastung durch Massenspektrometrie steht aktuell noch aus. Solange ist das eine unbewiesene Hypothese, die zu verifizieren oder falsifizieren wäre. Mir bekannte LAL-Test Ergebnisse waren negativ. Geoff Pain hat da aber wohl was am köcheln:
https://twitter.com/FluoridePoison/status/1719159498605257175
Ohne die volle Wirkung des PEG an der Außenseite des LNP kann es auch an ENDOTHELZELLEN binden. Dies kann zu Entzündungen, Immunreaktionen, Vasokonstriktion oder Vasodilatation führen (wodurch sich Gefäße verengen oder zusammenziehen) und auch zur Expression des Spike-Proteins im Endothel, denn ohne das PEG in voller Kraft an der Außenseite des LNP kann es auch an ENDOTHELZELLEN binden (https://pesquisa.bvsalud.org/global-literature-on-novel-coronavirus-2019-ncov/resource/pt/covidwho-1632901). Dies kann zu Entzündungen, Immunreaktionen, Vasokonstriktion oder Vasodilatation führen (wodurch sich Gefäße verengen oder zusammenziehen) und das Spike-Protein im Endothel exprimieren UND Auswirkungen auf die Blutgefäße und das Herz haben. Dies sollte der primäre Mechanismus für eine endotheliale Dysfunktion sein, denn der anfängliche Kontakt mit dem Endothel würde auch das Elektrolytgleichgewicht im Körper stören, die Angiogenese und die Reaktion auf Entzündungen negativ beeinflussen.
Da die LNPs an mehrere Dinge binden, können sie nun höhergeordnete Strukturen bilden, die als Komplexe bezeichnet werden.
Stellen Sie sich vor, der LNP hat jetzt eine negative Ladung, aber dann können positive und negative Dinge wie eine Kette daran haften bleiben und beginnen, sich zu verklumpen.
Das LNP kann auch eine Proteinkorona bilden, indem es sich mit Immunglobulinen, roten Blutkörperchen (Erythrozyten) (was zu Kapillarverstopfungen führt), weißen Blutkörperchen und Blutplättchen (Thrombozyten) verbindet – was zu MEHR Blutgerinnseln führt und weitere Blutgerinnsel und Bindeereignisse verursachen.
Kürzlich, am Wochenende, sprachen McKernan, Speicher und Rose über ihre jüngsten Erkenntnisse, dass die DNA-Plasmid-Kontamination in VAERS mit höheren unerwünschten Ereignissen korreliert.
Da das PEG außerhalb des LNP in seiner Größe oder Menge nicht einheitlich ist, führt dies dazu, dass sich die Oberflächenladung des LNP verschiebt und entweder ins Positive (+) oder Negative (+) geht, was die Bioverteilung verändert, Wechselwirkungen und unerwünschte Ereignisse in mehreren Systemen im Körpers verursacht, an Proteine im Körper bindet, mit dem Immunsystem interagiert, Blutgerinnsel verursacht, mit Albumin interagiert und mit dem Endothel interagiert und dort das Spike exprimiert, wodurch das Endothel beschädigt wird, während Endotoxin alles noch weiter negativ macht, soweit es vorhanden ist und die DNA-Kontamination ist in VAERS-Chargen höher.
ALLES beweist, dass das Zeta-Potenzial ein Hauptauslöser der akuten unerwünschten Ereignisse ist (zusätzlich zum Spike, dem Mutagenen Potential der DNA-Kontaminationen, mutagene Verunreinigung im Lipid…).
=== Teil 6 ===
GRUNDLEGENDE LADUNGEN: Die Vorgeschichte
Fast ALLE biochemischen Reaktionen im Körper beinhalten auf irgendeine Weise die Bewegung geladener Teilchen oder die Beteiligung geladener Moleküle.
Dies ist ein großes Thema, das ignoriert wird und der Auslöser für fast alle unerwünschten Ereignisse ist.
Es gibt positive (+) Ladungen und negative (-) Ladungen. Eine positive Ladung entsteht durch einen Überschuss an positiv (+) geladenen Teilchen – Protonen (+) innerhalb eines Objekts. Eine negative (-) Ladung entsteht durch einen Überschuss an negativ (-) geladenen Teilchen – Elektronen – innerhalb eines Objekts.
Positiv geladene Teilchen werden „Kationen“ genannt. Sie enthalten mehr positive als negative Ladungen. Negativ geladene Teilchen werden „Anionen“ genannt. Ladungen können aufgrund von Interaktionen mit anderen Objekten (z. B. einem Ballon!) geändert werden.
Die Berechnung der Ladung eines Objekts mag entmutigend bedrohlich wirken, ist aber einfache Mathematik.
Sie könnten sich Videos zu formaler Ladung, Valenzschalen und der Formel ansehen, aber der Einfachheit halber verwenden wir nur grundlegende Mathematik.
Zur Berechnung der Nettoladung addieren wir die Gesamtzahl der Kationen und Anionen. Nehmen wir als Beispiel Speisesalz. Salz besteht zu gleichen Teilen aus Natrium und Chlorid (Verhältnis 1:1). Natrium (Na) hat eine Ladung von +1. Chlorid hat eine Ladung von -1. Wenn Sie 1 + (-) addieren, erhalten Sie NULL (0). Das bedeutet, Salz, Speisesalz, ist neutral. es gibt keine Nettoladung. 0 ist neutral.
Das Folgende dient nur zur Verwendung in der Mathematik, ist in Bezug auf Zahlen nicht genau und dient lediglich dem Unterricht. Stellen Sie sich einen LNP vor, in dem sich positive und negative Ladungen befinden. Nehmen wir an, wir haben fünf positiv geladene Lipide (das sind die geladenen ionisierbaren Lipide) in einem LNP, jedes mit einer Ladung von +1, und EIN Stück aufgebrochener modRNA, das eine negative Ladung von -5 hatte (rein willkürliche Zahlen zu Lehrzwecken). Wir würden die fünf geladenen Lipide plus -5 addieren, um eine Gesamtsumme von Null zu erhalten. Dies bedeutet, dass LNP eine neutrale Nettoladung hätte.
Dies ist kein Zetapotential. Das Zetapotential sagt uns, wie hoch die Ladung auf der Oberfläche des LNP ist, im Verhältnis zu den Ionen, von denen es umgeben ist, zum pH-Wert, zur Viskosität usw.
Nettoladung:
Der pH-Wert ist ein Maß dafür, wie sauer oder basisch eine Lösung ist. Je mehr Protonen (H+) in einer Lösung positiv geladen sind, desto saurer ist sie. Der Magen ist sehr sauer. Waschmittel ist eine schwache Base. Säuren haben pH-Werte unter 7 und Basen haben pH-Werte über 7.
Der pH-Wert ist entscheidend für chemische Reaktionen, Enzymaktivität und biologische Prozesse. Biologische Systeme wie Blut und Zellumgebungen halten für eine optimale Funktion einen bestimmten pH-Bereich aufrecht. Enzyme, die für unser Funktionieren unerlässlich sind.
Wenn es um Vorgänge im Körper geht, sind fast ALLE Vorgänge ladungsabhängig. Es macht keinen Sinn, dass Zeta-Potenzial und Ladungen in Gesprächen ignoriert werden.
Arten geladener Reaktionen:
Coulomb-Gesetz:
Positive Ladungen (z. B. Protonen) ziehen negative Ladungen an.
Ion zu Ion: Ionen mit entgegengesetzter Ladung ziehen sich gegenseitig an und bilden Ionenbindungen. Beispielsweise werden in einem Salzkristall (Natriumchlorid, NaCl) positiv geladene Natriumionen (Na+) von negativ geladenen Chloridionen (Cl-) angezogen.
Ionen-Dipol-Wechselwirkungen:
Geladene Ionen können mit polaren Molekülen interagieren und so Ion-Dipol-Wechselwirkungen erzeugen. Beispielsweise interagieren in Wasser die positiv geladenen Wasserstoffionen (H+) mit dem negativ geladenen Sauerstoffatom (O) im Wassermolekül. (https://www.chemistrylearner.com/chemical-bonds/ion-dipole-forces)
Dipol-Dipol-Wechselwirkungen:
Polare Moleküle mit teilweise positiven und negativen Enden können durch Dipol-Dipol-Wechselwirkungen interagieren. Das positive Ende eines Moleküls wird vom negativen Ende eines anderen Moleküls angezogen.
Polare Moleküle: Ladungsverteilung ist ungleichmäßig:
Wasserstoffbrückenbindungen entstehen zwischen einem Wasserstoffatom, das an ein stark elektronegatives Atom (wie Sauerstoff oder Stickstoff) gebunden ist, und einem anderen elektronegativen Atom in einem anderen Molekül (DNA).
Van-der-Waals-Kräfte:
Elektrostatische Abschirmung: IONEN können in Gegenwart anderer Ladungen die Wechselwirkung zwischen zwei Ladungen teilweise abschirmen. Dies bedeutet, dass „Screening“ die Interaktion durch Abschirmung oder Induktion VERÄNDERN kann.
Weitere Informationen finden Sie unter: Elektronegativitätsunterschied, Dipolmomente, intermolekulare Wechselwirkungen, unpolare Momente und andere elektrostatische und bindende Wechselwirkungen zwischen Ionen.
Im menschlichen Körper gibt es einige wichtige spannungsgeladene Wechselwirkungen: Nervensignale: Aktion
Potentiale in Nervenzellen beruhen auf der Bewegung geladener Ionen (Natrium, Kalium, Kalzium, Chlorid) durch Zellmembranen.
Muskeln: Das Gleiten von Proteinfilamenten in Muskelzellen hängt von der Bewegung von Ionen (z. B. Kalzium) und ATP ab, das Ladungen trägt.
Mitochondrien:
Dabei erzeugen geladene Ionen (Protonen) einen elektrochemischen Gradienten zur Produktion von ATP.
Immunzellen nutzen geladene Moleküle und Ionen für Signal- und Erkennungsprozesse.
Der Körper reguliert geladene Ionen wie (Na+), (K+), (Ca2+) und (Cl-), um die Homöostase aufrechtzuerhalten.
Verschiedene Zellsignalwege beinhalten die Aktivierung von Proteinen durch Phosphorylierung und Dephosphorylierung, wobei es sich um ladungsbasierte Prozesse unter Verwendung von Phosphatgruppen (PO4³-) und Proteinkinasen handelt.
Immunsystem: Die Interaktion zwischen Immunzellrezeptoren (z. B. T-Zell-Rezeptoren und B-Zell-Rezeptoren) und Antigenen ist ladungsbasiert und beinhaltet elektrostatische Anziehung und Abstoßung.
PHAGOZYTE: Die negativ geladene Zellmembran der Phagozyte interagiert mit positiv geladenen Komponenten auf der Oberfläche des Krankheitserregers und erleichtert so die Adhäsion des Krankheitserregers an die Immunzelle.
(*Anmerkung DrBine: Quellenangaben wären nett gewesen*)
Änderungen der Ionenkonzentrationen können die Aktivierung und Reaktion von Immunzellen auslösen. Ein Anstieg der intrazellulären Kalziumionen signalisiert häufig die Aktivierung von Immunzellen.
(*Anmerkung DrBine: Quellenangaben wären nett gewesen*)
Mastzellen, eine Art Immunzellen, setzen Histamin als Reaktion auf Allergene oder Krankheitserreger frei. Histamin ist ein positiv geladenes Molekül, das mit spezifischen Histaminrezeptoren auf benachbarten Zellen interagiert und verschiedene Immunreaktionen, einschließlich Entzündungen, auslöst.
Die Ladungen auf der Oberfläche des LNP und im Inneren können mit einer unglaublichen Anzahl biologischer Prozesse interagieren, die Zellsignalwege verändern, Blutgerinnsel, die Bildung von Proteinkoronen, Reaktionen des Immunsystems, akute Hyponatriämie, neurologische Probleme und mehr verursachen
=== Teil 7 ===
LNP: Wie sich Zeta im menschlichen Körper verändert (für Laien) und warum Pharmaunternehmen falsch liegen, wenn sie sagen, dass ihre Berechnung des Zeta-Potentials (Oberflächenladung) korrekt ist, geschweige denn, dass sie keinen Schaden anrichtet.
Zeta ist der Ausgangspunkt für die meisten unerwünschten Ereignisse.
https://factreview.gr/wp-content/uploads/2023/07/Rolling-Review-Report-Quality-COVID-19-mRNA-Vaccine-BioNTech.pdf
(Lesen Sie die vorherigen Threads für vollständige Erklärungen zu LNP/Kolloiden/Lipiden/Zeta)
Zeta wird mit physikalischen Mitteln und auch mit Gleichungen (Smoluchowski/Henry) berechnet, wie zuvor in diesen Threads ausführlich erläutert. Zeta ist der Ausgangspunkt für unerwünschte Ereignisse. Es ist die Zündung.
Fakt ist: Das gemessene Zeta, von dem Pharmaunternehmen sagten, dass es sich nicht binden würde, -3,13 mV, wurde in einem großen Lösungsmittel gemessen und hatte NICHTS mit dem menschlichen Körper zu tun. DNA-Plasmid-Kontamination, Veränderungen im PEG, beide korrelieren mit bestimmten Chargen bei unerwünschten Ereignissen.
SIE LIEGEN FALSCH. Die zur Berechnung der Oberflächenladung verwendeten Dateneingaben ÄNDERN sich je nachdem, wo sich das NLP im Körper befindet, womit es interagiert, und wiederum verändert sich Zeta mit der DNA-Plasmid-Kontamination sofort negativer. Das ist keine Hypothese. Das ist eine Tatsache.
Schlüsselfaktoren, die die Oberflächenladung von LNP (Zeta) verändern und beeinflussen und bestimmen, wohin es im Körper gelangt (Bioverteilung) und WAS es bewirkt (der Ausgangspunkt hinter der Spike-Expression, wo Mutationen auftreten würden (falls vorhanden) und vieles mehr.
Die Debye-Länge ist in der Smoluchowski-Gleichung KRITISCH. DEBYE wird durch die Ionenstärke beeinflusst. In Flüssigkeiten wie Blut oder interstitieller Flüssigkeit ist die Ionenstärke im Vergleich zu hochionischen Lösungen geringer, was in biologischen Flüssigkeiten zu einer größeren Debye-Länge führt. Dies verändert Zeta.
Änderungen der Ionenstärke biologischer Flüssigkeiten verändern die Debye-Länge und Zeta. Eine Erhöhung der Ionenstärke führt zu einer kürzeren Debye-Phase, wodurch sich Zeta ändert – die Stärke (und möglicherweise auch die Richtung) der Oberflächenladung ändert sich, wohin das LNP geht und was es tun wird.
Änderungen des pH-Werts verändern die Oberflächenladung des LNP. Viele biologische Flüssigkeiten haben spezifische pH-Werte, die das Zetapotential beeinflussen können. Schwankungen im pH-Wert des Gewebes verändern die Oberflächenladung des LNP in bestimmten Körperkompartimenten und verändern so, was es tut und wohin es geht.
Biologische Flüssigkeiten enthalten Proteine wie Albumin und Immunglobuline, die an der Oberfläche des LNP adsorbieren können. Die Adsorption von Proteinen kann die Oberflächenladung (Zeta) des LNP verändern. Dieses Phänomen ist als Proteinkoronabildung bekannt und kann unerwünschte Ereignisse verursachen.
(*Anmerkung DrBine: Auch hier wäre eine Quellenangabe nett gewesen*)
LNPs interagieren mit Zellen und Geweben im Körper, was die lokale Umgebung und die Ionenstärke verändern kann. Zelluläre Reaktionen, wie die Freisetzung von Zytokinen, können zu Veränderungen des pH-Werts oder der Ionenstärke führe, somit das Zeta-Potenzial beeinflussen und eine IMUNSYSTEM-KASKADE (Zytokinsturm) verursachen.
Verschiedene Gewebe und Körperkompartimente weisen unterschiedliche Ionenstärken, pH-Werte und Proteinzusammensetzungen auf. Die Ionenstärke im Blut unterscheidet sich von der der interstitiellen Flüssigkeit oder dem Liquor. Diese Unterschiede wirken sich auf Zeta aus, wenn die LNPs verschiedene Körperkompartimente durchqueren.
BLUT: Die Ionenstärke ist relativ konstant und wird streng reguliert, um die Bedingungen aufrechtzuerhalten. Die Elektrolytzusammensetzung im Blutplasma (Natrium-, Kalium-, Kalzium- und Chloridionen) ist gut kontrolliert, was zu einer stabilen Ionenstärke führt. Das Vorhandensein von Plasmaproteinen und zellulären Komponenten kann jedoch aufgrund der Proteinkoronabildung zu Veränderungen des Zetapotentials führen Wechselwirkungen mit Blutzellen führen zu einer Kaskade möglicher Wirkungen.
Interstitielle Flüssigkeit ist die Flüssigkeit, die Zellen in Geweben umgibt. Es enthält eine ähnliche Elektrolytzusammensetzung wie Blutplasma, die Ionenstärke hängt jedoch vom Gewebetyp ab. Die Ionenstärke in der interstitiellen Flüssigkeit um das Muskelgewebe kann sich von der in der interstitiellen Flüssigkeit um das Fettgewebe unterscheiden. Diese Variationen verändern die Zeta von LNPs, wenn sie sich zwischen Geweben bewegen.
Innerhalb von Zellen unterscheiden sich die Ionenzusammensetzung und -stärke SEHR von extrazellulären Flüssigkeiten. Die intrazelluläre Umgebung weist hohe Konzentrationen an Kaliumionen (K+) und niedrige Konzentrationen an Natriumionen (Na+) auf. LNPs, die in Zellen eindringen, verändern ihre Ionenstärke und somit Zeta. Jedes Mal.
Schleimhäute: Magen-Darm-Trakt oder Atmungssystem, die Ionenstärke ändert sich durch die Sekretion von Schleim, der spezifische Elektrolyte enthält. Die Wechselwirkung von LNPs mit Schleimhäuten VERÄNDERT DAS LNP-ZETA und die Wirkungsweise der LNPs. Die Cerebrospinalflüssigkeit (CSF), die Gehirn und Rückenmark umgibt, hat eine andere Ionenzusammensetzung als Blutplasma. Die Ionenstärke im CSF ist geringer, was zu einer längeren Debye-Länge führt. Dieser Unterschied verändert die Oberflächenladung von LNPs, wenn sie in das ZENTRALE NERVENSYSTEM, EINSCHLIESSLICH DES GEHIRNS, gelangen.
(*Anmerkung DrBine: Eine Quellenangabe wäre nett gewesen, bzw. das Mitkopieren der Bildunterschrift*)
Der Blutkreislauf ist nicht der einzige Ort, an dem ein LNP mit Proteinen in Kontakt kommen und Proteinkoronen bilden kann. Die Bildung einer Proteinkorona kann auch in extrazellulären Flüssigkeiten auftreten, beispielsweise in der interstitiellen Flüssigkeit oder der Flüssigkeit, die Zellen in Geweben umgibt. Wenn LNPs in diese Umgebungen eingeführt werden, können sie Proteine aus dem lokalen Milieu adsorbieren, wodurch sich die Oberflächenladung und das Verhalten ändern – was dazu führt, dass sie sich an bestimmte Gewebe binden, Blutgerinnsel verursachen, innere Entzündungen verursachen, an Endothel binden, mit Antikörpern reagieren und in Bereiche wie die Hypophyse eindringen.
Schleimhaut: Ein LNP kann mit Proteinen in Schleimsekreten interagieren. Diese Wechselwirkung kann zur Bildung einer Proteinkorona führen und die LNP-Wechselwirkungen mit Schleimhäuten und Zellen beeinflussen, was zu unerwünschten Ereignissen führt. Gehirn-Rückenmarks-Flüssigkeit – das LNP kann auch hier Koronen bilden.
Vorhandener KREBS und TUMOREN: Auch die Umgebung in Tumoren ist unterschiedlich, und das Zeta-Potenzial kann sich ändern, wenn ein LNP mit (wachsenden) Tumoren in Kontakt kommt. Dabei spielt es keine Rolle, ob sie gutartig oder bösartig sind.
Innerhalb von Zellen, insbesondere Immunzellen wie Makrophagen und dendritischen Zellen, können Nanopartikel während der Endozytose und zellulären Aufnahme auf einen anderen Satz von Proteinen treffen. Dies kann das intrazelluläre Schicksal der Partikel beeinflussen.
Zurück zu den Ionen: MUSKELN haben eine unterschiedliche Ionenstärke, und dies kann Zeta und die Wechselwirkungen verändern.
Fettgewebe (Fett) hat eine ausgeprägte Mikroumgebung. Es enthält eine Vielzahl von Adipokinen und Fettsäuren, die mit LNPs interagieren und ZETA verändern können. Ja, dein FETT!
Der Liquor, der Gehirn und Rückenmark umgibt, hat eine geringere Ionenstärke als Blutplasma. Dies führt zu einer längeren Debye-Länge, was eine bessere räumliche Verteilung der LNPs ermöglicht und sich auf deren Verhalten an Grenzflächen auswirken kann, wodurch sie für bestimmte Bereiche des ZNS besser zugänglich werden.
Der nächste Thread fügt alles zusammen. In früheren Threads gibt es Zitate, die alles aufschlüsseln.
=== Teil 8 ===
Erklären Sie es mir, als wäre ich 12-Version:
Das ist eine komplexe Sache – wenn Sie kein Wissenschaftler sind und diese Themen verstehen, haben Sie die Nase vorn, denn ich spreche mit Ärzten und Wissenschaftlern, die es nicht verstehen.
Stellen Sie sich ein LNP als ein Schnellboot vor, das auf einem Fluss fährt. Das Schnellboot stellt das Lipid-Nanopartikel dar und der Fluss symbolisiert den Blutkreislauf oder einen anderen Ort im Körper, an dem sich das LNP bewegt. Es handelt sich um Schnellbot mit Tarnung, da das PEG das LNP vor dem Immunsystem verbirgt.
Das Boot ist von einer magnetischen Kraft umgeben, wie eine unsichtbare magnetische Blase. Diese magnetische Kraft ähnelt dem Zetapotential des LNP.
Die Magnetkraft des Bootes kann stark oder schwach sein, ebenso wie das Zetapotential stark negativ oder weniger negativ (oder sogar positiv) sein kann.
Der Bootsrumpf ist mit speziellen Stoßfängern beschichtet, ähnlich den pegylierten Lipiden auf der Oberfläche des LNP. Diese Stoßstangen bilden eine Schutzbarriere rund um das Boot.
Die Puffer (pegylierte Lipide) verhindern, dass das Boot mit anderen Booten und Hindernissen im Fluss zusammenstößt. Dies wäre so, als würde man es daran hindern, sich mit Dingen im Blutkreislauf zu verbinden, etwa mit Plasmaproteinen, die dazu führen würden, dass es eine Proteinkorona bildet, etwa Immunglobuline oder Albumin. Es würde auch die Bindung an den Thrombozytenfaktor 4 hemmen (Gerinnungszeit!)
(*Anmerkung DrBine: Erneut fehlt beim Bild die Bildunterschrift und Quelle*)
Während das Boot durch den Fluss fährt, interagiert seine magnetische Kraft (Zeta-Potenzial) mit der Umgebung. Wenn die Kraft stark (stark negativ) ist, kann sie andere Objekte mit der gleichen Ladung abstoßen und auf Distanz halten. Dies wird jedoch nicht vollständig gestoppt.
Die Stoßfänger des Bootes (pegylierte Lipide) sorgen dafür, dass es sanft an Hindernissen vorbeigleitet und nicht am Flussufer oder an anderen Booten kleben bleibt.
Dies wird immer noch passieren, wenn sich rund um das Boot weniger pegylierte Lipide (Stoßstangen) befinden – es kann immer noch mit anderen Dingen wie dem Endothel, Molekülen usw. interagieren.
Wissenschaftler können die magnetische Kraft (Zeta-Potenzial) des Bootes an die spezifische Route anpassen, die sie im Fluss nehmen möchten (z. B. auf ein bestimmtes Gewebe oder einen bestimmten Zelltyp abzielen). Dies ist keine Hypothese. Es ist Tatsache.
Die Kraft der Ladung außerhalb des LNP bestimmt, wohin sie geht und womit sie interagiert. Es ist der Hauptmechanismus, der die meisten unerwünschten Ereignisse auslöst. Wenn das Spike-Protein im Endothel oder im Herzen exprimiert wird, besteht eine hohe Wahrscheinlichkeit, dass das Zeta-Potenzial des LNP weit in den negativen Bereich gedrückt wurde und so in das Gefäß gelangt.
Die Flussbedingungen können sich unterwegs verändern, ebenso wie die Umgebung des Körpers. Beispielsweise können die Breite des Flusses, die Geschwindigkeit und andere Boote variieren.
Die Magnetkraft des Bootes (Zeta-Potenzial) und seine Puffer (pegylierte Lipide) können sich während der Fahrt verändern und unerwünschte Auswirkungen haben.
Nachteilige Auswirkung: Wenn das Boot zu stark aufgeladen ist, fällt es ihm manchmal schwer, sich anderen Booten zu nähern, mit denen es interagieren muss, was dazu führt, dass es bestimmte Zellen oder Gewebe meidet. Es könnte auch sehr aufgeladen sein, und wenn es positiv ist, gelangt es in die Lunge. Wenn es negativ ist, bindet es auch.
Der Fluss kann enge Passagen oder verengte Bereiche aufweisen, die Bereiche innerhalb des Körpers entsprechen, in denen das Boot vorsichtig navigieren muss.
Die Stoßfänger des Bootes (pegylierte Lipide) helfen ihm, Kollisionen mit dem Flussufer und anderen Booten zu vermeiden, indem sie eine Schutzbarriere bilden.
Nachteilige Auswirkung: Wenn das Boot in sehr engen Passagen zu breit ist oder seine Stoßstangen nicht wirksam sind, kann es dennoch auf Hindernisse stoßen, was möglicherweise zu Schäden oder Störungen der Umgebung führen kann. Genau wie bei Blutgefäßen, wenn Zeta negativ ist, kann das LNP an die Wände des Endothels binden und verursacht Entzündungen, die Expression des Spike-Proteins, eine Immunantwort und stößt die Gerinnung an (Virchow-Trias).
(*Anmerkung DrBine: Virchow-Trias:*)
https://flexikon.doccheck.com/de/Virchow-Trias
Der Fluss hat unterschiedliche Fließgeschwindigkeiten, die unterschiedlichen Fließgeschwindigkeiten in verschiedenen Körperteilen entsprechen.
Das Boot muss seine Geschwindigkeit und magnetische Kraft (Zeta-Potenzial) anpassen, um sich mit oder gegen die Strömung zu bewegen, um sein Ziel zu erreichen.
Nachteilige Auswirkung: Wenn das Boot seine Geschwindigkeit oder Magnetkraft nicht entsprechend anpasst, kann es Schwierigkeiten beim Vorwärtskommen haben oder von der Strömung mitgerissen werden, was zu unbeabsichtigten Folgen führen kann.
Das Boot verwendet Sensoren, um Hindernisse und andere Boote zu erkennen, genauso wie Wissenschaftler und Forscher LNPs mit Oberflächeneigenschaften entwerfen, um bestimmte zelluläre Ziele zu erkennen und mit ihnen zu interagieren.
Nachteilige Auswirkung: Wenn die Sensoren des Bootes nicht genau abgestimmt sind oder Signale falsch interpretieren, kann das Boot Hindernissen möglicherweise nicht ausweichen, was zu Kollisionen und möglichen Schäden am Boot und den Hindernissen führen kann.
=== Teil 9 ===
Erklären Sie es mir, als wäre ich 12 Jahre alt – Zeit für naturwissenschaftliche Mathematik!
VIELE von euch können das lernen!
Die Zeta-Verschiebung ist der Auslöser vieler unerwünschter Ereignisse / Nebenwirkungen. Die Gleichungen sehen kompliziert aus, aber wenn man jeden Abschnitt aufschlüsselt, handelt es sich um „Plug-and-Play“-Algebra.
Hier ist ein grundlegendes LNP. Diese Zahlen und Symbole sind nur zu Lehrzwecken und somit willkürlich. Wir lassen PEG, Cholesterin und DSPC weg und konzentrieren uns nur auf die Ladungen. Sie werden in Zahlen ungenau sein – dies dient nur dazu, die Art und Weise zu lernen, wie Sie sie addieren – eine visuelle Darstellung.
Ein Bestandteil dieser Berechnung ist die Bestimmung der NET-Ladung. Das Zetapotential ist die Oberflächenladung im Verhältnis zu allen anderen Dingen rund um den LNP. Sie haben Ionen in Ihrem Körper, des Weiteren nehmen die „Dicke“ des Gewebes oder Bluts (Viskosität), diverse Moleküle, der pH-Wert und einige andere Dinge Einfluss auf das LNP.
Schau dir das an. Es gibt 3 (+) und 3 (-) .
Die Art und Weise, wie Sie diese addieren, ist: 3 + (-) 3= 0. Drei plus minus drei oder drei minus drei ist Null. Die Nettoladung ist neutral.
Dies ist eine übermäßige Vereinfachung der größeren Gleichung, aber jeder Teil der Gleichung – jedes „Symbol“ enthält so einfache Mathematik, das ist alles. Allerdings ändert sich die Mathematik je nachdem, wo sich das LNP im Körper befindet, und verändert somit das Zeta, und somit wohin das LNP geht und was es tut.
Schauen Sie sich als nächstes noch einmal die Ladungen an – sowohl die positiven als auch die negativen. Dieses LNP hat VIER positiv geladene Teilchen (das grüne +) und DREI negativ geladene Teilchen.
Wir nehmen 4 + (-) 3, was vier minus drei ist, gleich eins. Das ist positiv. Daher ist die Nettoladung = +1.
Dieses hier hat etwas mehr zu bieten. Dieses LNP hat drei positiv geladene Teilchen und sechs negativ geladene Teilchen. Wir berechnen die Nettoladung auf die gleiche Art und Weise und nehmen 3 + (-) 6, was drei minus sechs ist, was 3-7= -3 ist. Das bedeutet, dass die Nettoladung -3 beträgt.
Ergibt das Sinn?
Wenden wir es nun auf den LNP an, und dies ist wiederum nur einer der kleinen Teile dieser großen Gleichung, aber jede Berechnung, jedes Symbol hat eine Berechnung wie diese. Dies ist eine der Textaufgaben, die viele von Ihnen im Algebra- oder Chemieunterricht gelöst haben. Das ist es! Nicht beängstigend!
Hier ist der LNP.
Die Ladungen sind nicht korrekt, dies ist nur eine Darstellung zu Lehrzwecken. ModmRNA weist negative Ladungen auf und die Ladungen variieren. Wir verwenden im Moment nur vereinfachte Zahlen, um das Rechnen zu lernen. Wissenschaftler machen die Dinge manchmal zu schwierig. Nicht heute!
Natürlich hat die Mod-RNA mehr als nur eine negative Ladung pro Stück, aber wir machen das nur, um zu lernen, WIE man heute EINEN Teil der Mathematik durchführt.
Hier gibt es drei positiv geladene Lipide und drei negativ geladene RNA. (+)3 + (-) 3= Null.
Neutrales LNP.
JETZT existieren diese Ladungen in einem Vakuum. Es gibt kein umgebendes Lösungsmittel, keinen pH-Wert, mit dem man zu kämpfen hat, keine Ionen, keine Viskosität, keine Debye-Länge – all die Dinge, über die wir in anderen Threads gesprochen haben. Darum bleibt es nicht beim Alten!
(Dies hat eine Nettoladung von minus drei).
Der Rest wird komplexer. Quantifizieren Sie die Ladungsdichte dieser Komponenten, indem Sie die Anzahl geladener Gruppen oder Ladungen pro Flächeneinheit (z. B. Ladungen pro Quadratnanometer) sowohl für die positiv geladenen Lipide als auch für die negativ geladene RNA bestimmen. Ja, mehr Mathematik!
Dann berechnen Sie das Gleichgewicht der positiven und negativen Ladungen auf der LNP-Oberfläche. Das Zetapotential stellt die Nettoladung dar. Subtrahieren Sie also die negativen Ladungen von den positiven Ladungen, um die Gesamtoberflächenladung zu erhalten. Dies geschieht im Vakuum, ohne andere Ionen usw.
Nun berücksichtigen Sie die Ionenstärke der Lösung, in der sich das LNP befindet. Die Debye-Länge (λ_ D) gibt uns die Dicke der elektrischen Doppelschicht um die geladenen Teilchen an und hängt von der Ionenstärke ab. Dieser Parameter kann das Zetapotential beeinflussen und das tut es auch!
Dann können Sie einfach die Smoluchowski-Gleichung oder die Henry-Gleichung (oder eine Hybridgleichung) anwenden, die das Zeta-Potenzial mit der elektrophoretischen Mobilität von LNP in Beziehung setzt. Diese Gleichungen berücksichtigen das Kräftegleichgewicht, einschließlich elektrostatischer Kräfte aufgrund von Oberflächenladungen.
Im physikalischen Umfeld wird das Zetapotential experimentell mithilfe von Techniken wie elektrophoretischer Lichtstreuung (ELS) oder Laser-Doppler-Anemometrie bestimmt. Diese Methoden messen die Geschwindigkeit von Teilchen in einem angelegten elektrischen Feld, um das Zetapotential zu berechnen.
Jetzt sollten Sie anhand der Ladungen eine gute Vorstellung davon haben, wie eine Komponente des Zeta-Potentials berechnet wird. Die DNA-Plasmid-Kontamination würde die negativen Ladungen verstärken, da es sich um hochelektronegative Teilchen handelt, die das von Pfizer berechnete Zeta-Potenzial ungültig machen.
Weitere Daten belegen, dass die PEGylierten Lipide an der Außenseite des LNP die als Schutzbarriere, als sterische Barriere, fungieren sollten, das LNP destabilisieren und es dazu bringen, mit noch mehr Molekülen zu interagieren, wodurch sich Zeta verändern kann.
Nächster Thread, Zeta Teil zehn: Alle Beweise zusammenfassen, um das Zeta-Potenzial zu beweisen, welches die Ladung des LNP steuert und somit wohin das LNP im Körper gelangt und damit wie die Kontamination und die extreme Variation im Zeta-Potential viele unerwünschten Ereignisse verursachen.
=== Teil 10 ===
Dank der jüngsten Entdeckung der DNA-Kontamination durch Dr. Phillip Buckhaults, Kevin Mckernan und andere, Dr. David Speicher, Dr. Rose (finden von DNA vs. Charge vs. unerwünschtes Ereignis) DrBine/Expertcouncil.one (PEG) und andere – das beweist so vieles, einschließlich der Änderung von Zeta.
Diese Serie bietet Hintergrundinformationen zu Lipiden, ihren Aktivitäten, Ladungen, Kolloiden, dem menschlichen Körper, wie man die Ladung eines Lipid-Nanopartikels bestimmt, was sie beeinflusst, wohin es im Körper gelangt und wie es die Kaskade für unerwünschte Ereignisse auslöst.
Ohne die sehr harte Arbeit der oben aufgeführten Personen und so vieler Menschen hinter den Kulissen, wären die Menschen nicht in der Lage, die Arbeit anderer zu ihren eigenen Erkenntnissen zu kombinieren. Viele Menschen mussten mit harten Konsequenzen rechnen, weil sie diese Arbeit unter großem persönlichen Risiko verrichteten. Das ist für euch.
Das Zeta-Potenzial ist kein neues Konzept – keine Hypothese. Das ist schon seit Jahren bekannt – lange bevor die Idee des LNP jemals zum Funkeln in den Augen eines Wissenschaftlers irgendwo in einem Labor wurde. Es ist die Ladung eines Teilchens, die bestimmt, was es tut.
Dies ist alles eine Zusammenfassung und eine Wiederholung dessen, was in anderen Threads gesagt wurde. Pfizer et al. ermittelten, dass das Zeta-Potenzial in einem Massenlösungsmittel (das nicht den menschlichen Körper in seiner Gesamtheit darstellt) ein Zeta-Potenzial von etwa -3 mV aufweist.
„Um unspezifische Ereignisse zu vermeiden“
Wir haben behandelt, was ein Bindungsereignis bedeutet: Bindung mit anderen Molekülen, Ionen, Proteinen, anderen Lipiden, dem Endothel, Plättchenfaktor 4 – es gibt viele Dinge, an die sich das LNP binden kann, wenn die Ladung zwischen positiv oder negativ schwankt. Aber es kann binden auch aufgrund von „Hydro“-Wechselwirkungen.
Dies kann zu Blutgerinnseln, einer Immunkaskade, einem Zytokinsturm, einer Bindung mit dem Endothel zur Expression des Proteins in den Kapillarwänden und Mikrogerinnseln führen und die schnelle Hyperkoagulationskaskade auslösen, die nachweislich aus negativ geladenen Liposomen resultiert, die mit dem Blut interagieren.
Die dicken Blutgerinnsel, von denen die Leute sagen, dass sie nicht existieren, wurden in einer Studie von Fazullin et al. Anfang 2020 nachgewiesen. Es beweist, dass stark negativ geladene Liposomen die Gerinnselbildung um das Tausendfache über das normale Maß hinaus vorantreiben.
Faizullin D, Valiullina Y, Salnikov V, Zuev Y. Direct interaction of fibrinogen with lipid microparticles modulates clotting kinetics and clot structure. Nanomedicine. 2020 Jan;23:102098. doi: 10.1016/j.nano.2019.102098. Epub 2019 Oct 23. PMID: 31655206. https://pubmed.ncbi.nlm.nih.gov/31655206/
Wenn das Zeta-Potenzial gemessen wurde, wurde es unter Verwendung eines Massenlösungsmittels gemessen, wobei bei Prozess EINS die modRNA unter Verwendung von IVT-Enzymen, die keine E. coli verwenden und ohne Plasmide hergestellt wurde. Von DNA zu RNA zu Protein – IVT-Enzyme, von RNA zu Protein. Das Zeta wurde von Pfizer durch Messung des LNP gemessen, nachdem es hergestellt wurde, unter Verwendung von Verfahren EINS – ohne die Anwesenheit von Plasmiden oder E. coli (*Anmerkung DrBine: erneut der Endotoxin-Fehler*) Endotoxinen. Für die klinischen Studien handelte es sich um einen völlig separaten Herstellungsprozess. Prozess ZWEI, das Zeug, das jedem in die Arme gespritzt wurde, verwendete DNA-Plasmide, um RNA herzustellen.
Pfizer gibt in seinem eigenen Dokument sehr deutlich an, dass sie das LNP-Zeta-Potenzial eher neutral gemessen haben, um „unspezifische Bindungsereignisse im Blutkompartiment zu vermeiden“. SIE WUSSTEN. Sie wussten, dass es schlecht wäre, wenn sich die Situation positiv oder negativ entwickeln würde.
Mehrere Studien haben bewiesen, dass sich, wenn das LNP nicht neutral ist, das Verhältnis der Ladungen innerhalb des LNP ändert, sodass es positiver oder negativer wird. Dadurch ändert sich, wohin das NLP geht und was es tut. Wenn es neutral ist, gelangt es in die Leber. Wenn positiv, geht es in die Lunge.
Leicht negativ, geht auf die Milz über. Und SEHR negativ geladenes LNP gelangt direkt in das Gefäß. Dabei spielt es keine Rolle, ob Sie in einen Muskel oder eine Vene injizieren. Es spielt keine Rolle, ob Sie aspirieren. Dieses Gerede muss sofort aufhören.
Daher wurde das ursprüngliche Zetapotential in einem Lösungsmittel gemessen. Aber als es gemessen wurde, gab es keine E-coli-Kontamination oder Endotoxin Kontamination durch Zellfreie Kultur und keine DANN Kontamination durch die Verwendung von Plasmiden, daher ist das gemessene Zeta FALSCH. Pfizer hat es falsch verstanden.
Die DNA-Plasmide haben eine hohe negative Ladung, sie sind sehr elektronegativ. Das bedeutet, dass jede Einführung, JEDE, dazu führen würde, dass sich das Zeta-Potenzial noch negativer wird, was dazu führen würde, dass das LNP an Dinge bindet, sich an das Endothel bindet und in das Gefäß austreten möchte.
Speicher und McKernan (das ist für euch!) stellten kürzlich fest, dass bestimmte Chargen/Chargen von Pfizer eine höhere Kontamination aufwiesen als andere, und sie verknüpften diese mit bestimmten Chargen, und siehe da: Je höher der DNA-Gehalt, desto mehr unerwünschte Ereignisse! (Myokarditis!)
Wenn Sie sich die Chargennummern in dieser Tabelle ansehen, gilt: Je mehr DNA in der Charge enthalten ist, desto höher ist die Zahl der verletzten Personen. Und wenn Sie sich fragen, wie schlecht meine Charge ist, gehen Sie zu Howbadismybatch und geben Sie diese Chargennummern ein, Sie werden viele Myokarditis-Ereignisse sehen. https://knollfrank.github.io/HowBadIsMyBatch/HowBadIsMyBatch.html
Dies beweist, dass sich das Zeta-Potenzial ins Negative verschiebt und die Kaskade unerwünschter Ereignisse in Gang setzt.
Die Veränderung des PEG, das eine Schutzbarriere an der Außenseite des LNP bildet, ist nicht einheitlich und es wurde auch festgestellt, dass bei der Betrachtung bestimmter Chargen die Chargen mit WENIGER PEG mehr unerwünschte Ereignisse aufwiesen! Dies beweist auch, dass Zeta eine wichtige Rolle spielt.
(*Anmerkung DrBine: Korrektur - Die AG Impfstoffe des Expertcouncil.one hat gesehen, dass kurze PEG- Schwänze mehr Nebenwirkungen aufweisen, nicht weniger PEG.*)
Die Arbeit anderer in Deutschland sowie von Dr. Geoff Pain, bei der Endotoxin in Chargen gefunden wurde, das ebenfalls eine negative Ladung hat und von E. coli stammt, aus denen die Plasmide „gezüchtet“ werden, verschiebt die Zeta ebenfalls noch weiter ins Negative , was den Beginn der unerwünschten Ereignisse verursacht.
(*Anmerkung DrBine: Korrektur – Es wurde zum aktuellen Zeitpunkt 1.11.2023 noch KEIN Endotoxin jenseits des Grenzwertes nachgewiesen. Des Weiteren stammt das Endotoxin aus der zellfreien Kultur, die aus verlüssigten E. Coli besteht, also im Prinzip aus verflüssigten E. Coli Leichen. Darin ist das Endotoxin mit enthalten, das Bestandteil der E. Coli Zellwand ist*.)
Kinder sind gestorben. Sie haben Kinder getötet. Natürlich, aber der Sohn und die Tochter von jemandem sind jetzt deformiert oder tot. Jeder Teil dieser Plattform hat ein Problem. Es ist nicht für den Masseneinsatz geeignet. Diese Plattform wurde zuvor nur für leidende Menschen genutzt. Das war ihr Plan A.
Plan B war RNA mit LNP, aber er wurde sicherlich nie mit E. Coli und Junk-Materialien hergestellt. Das Verfahren birgt immer noch Risiken. Aus diesem Grund wurde es in klinischen Studien nur für kleine Kohorten von vielleicht 50 Personen verwendet, die aufgrund genetischer Krankheiten nicht mehr lange zu leben haben.
Das Vorhandensein der DNA-Plasmide bestätigt jedoch, dass sich das Zeta-Potential ins Negative verschiebt, und die Arbeit von Speicher, McKernan und Rose beweist dies durch ihre Erkenntnisse, dass die Chargen mit höherer DNA-Plasmid-Kontamination häufiger unerwünschte Ereignisse aufweisen.
Das ist keine Hypothese, es ist keine Theorie, und ehrlich gesagt steht es auch nicht zur Debatte. Wer etwas anderes sagt, versucht Ihnen etwas zu verkaufen.
=== Teil 11 ===
Warum ein positiv geladenes (ZETA) LNP direkt in die Lunge gelangt und eine Hyperkoaggulation auslöst.
Es gibt mehrere Faktoren, die zusammenwirken und dazu führen, dass das LNP mit einer hohen Netto-positiven Oberflächenladung/einem hohen positiven Zeta-Potenzial direkt in die Lunge gelangt.
Wir müssen jeden Grund auseinandernehmen, der dieses Amalgam dafür bildet, warum der LNP dies tut. Einiges wurde behandelt.
PEG: Die pegylierten Lipide auf dem LNP (zur Auffrischung in diesem Thread/Kapiel abgedeckt) – bieten eine sterische Barriere (verhindern die Bindung an Plasmaproteine), Stabilität und machen so das LNP das Immunsystem unsichtbar, sodass es länger zirkulieren und in Gewebe eindringen kann (klingonischer Bird of Prey).
Auf die Größe kommt es an: Es wurde gemessen, dass der LNP zwischen 50 nm und 100 nm groß ist, obwohl einige Messungen besagen, dass er eine Größe von 200 nm erreicht (Aggregation, Ostwald-Effekt, Flockung würde dies ebenfalls bewirken). Größere Nanopartikel haben längere Zirkulationszeiten und reichern sich aufgrund des EPR-Effekts (Enhanced Permeability and Retention) in Geweben mit undichten Gefäßen wie Tumoren an. EPR: Eine erhöhte Permeabilität ist auf „Fensterungen“ in Kapillaren/Gefäßen usw. zurückzuführen.
(*Anmerkung DrBine Kontext - Die LNP haben eine Größe von 40 - 180 nm*)
Es gibt viele Bereiche im Körper, in denen dies auftritt (Tumoren sind einer davon), darunter:
Der Nierenglomerulus, der die Filtration von Blutplasma und die Bildung von Urin ermöglicht. Diese Kapillaren haben kleine Poren in ihren Wänden, die den Durchgang von Wasser, Elektrolyten und kleinen Molekülen ermöglichen, während größere Proteine und Blutzellen zurückgehalten werden. "Undicht".
Der Dünndarm ist mit Zotten ausgekleidet. Diese Strukturen verfügen über gefensterte Kapillaren, die die Aufnahme von Nährstoffen aus dem Verdauungstrakt in den Blutkreislauf erleichtern. Das Vorhandensein von Fenstern ermöglicht einen effizienten Nährstoffaustausch. (Tangente der Lunge). Außerdem haben einige endokrine Drüsen, wie die Nebennierenrinde und der Hypophysenvorderlappen, gefensterte Kapillaren. Dies ermöglicht den schnellen Austausch der von diesen Drüsen produzierten Hormone in den Blutkreislauf. Aus diesem Grund sehen Sie ungewöhnliche Blutungsstörungen (Hypophyse).
In der Plazenta, die das heranwachsende Baby mit Nährstoffen und Sauerstoff versorgt, unterstützen gefensterte Kapillaren den Austausch von mütterlichem und fetalem Blut und ermöglichen so die Übertragung von Sauerstoff, Nährstoffen und Abfallprodukten. So kommt der LNP da rein.
In entzündeten Bereichen können die Blutgefäße für Immunzellen und Proteine durchlässiger werden. Diese erhöhte Permeabilität ermöglicht es Immunzellen, zum Ort der Infektion oder Verletzung zu wandern. Bist du Raucher? Haben Sie eine Lungenentzündung?
Zurück zur Lunge. In der Lunge gibt es Fenster (Poren) in den Kapillaren, die den Durchgang des LNP ermöglichen und es ihm so ermöglichen, an bestimmte Stellen zu diffundieren.
SCHLEIMWECHSELWIRKUNGEN: Dies ist einer der Hauptgründe, warum das positiv geladene LNP mit hohem positivem Zeta-Potenzial in die Lunge gelangt. Die Schleimschicht der Atemwege ist negativ geladen. Der Schleim in den Atemwegen besteht hauptsächlich aus GLYKOPROTEINEN, den sogenannten MUCINS, die zahlreiche negativ geladene Gruppen enthalten. Diese negative Ladung wird benötigt, damit das Atmungssystem „funktionieren“ kann.
„Muzine sind die wichtigsten gelbildenden Bausteine des Schleims und bestehen aus fadenförmigen Kernproteinen, die eine große Anzahl O-verknüpfter Oligosaccharidketten enthalten, die nach außen ragen. Oligosaccharidketten verleihen Muzinen über Carboxyl- und Sulfatgruppen eine negative Ladung.“
Li LD, Crouzier T, Sarkar A, Dunphy L, Han J, Ribbeck K. Spatial configuration and composition of charge modulates transport into a mucin hydrogel barrier. Biophys J. 2013 Sep 17;105(6):1357-65. doi: 10.1016/j.bpj.2013.07.050. PMID: 24047986; PMCID: PMC3785869. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3785869/
Die negative Ladung des Schleims hilft dabei, Fremdpartikel wie Staub, Schadstoffe und Mikroorganismen, die beim Atmen in die Atemwege gelangen, einzufangen und zu entfernen. Diese Fremdpartikel tragen eine positive Ladung und die elektrostatische Wechselwirkung zwischen dem negativ geladenen Schleim und den positiv geladenen Partikeln trägt dazu bei, sie zu immobilisieren und aus den Atemwegen zu entfernen. Dieser Mechanismus ist Teil des natürlichen Abwehrsystems der Lunge und für die Aufrechterhaltung einer gesunden Atemfunktion von entscheidender Bedeutung. Die positiv geladenen Partikel werden vom negativ geladenen Schleim in der Lunge angezogen. Das Gleiche gilt für das LNP, hier gibt es eine große Menge an konzentrierten negativ geladenen Mucinen, und weil Gegensätze sich anziehen, und wenn das LNP zirkuliert, bleibt es an den Mucinen in der Lunge hängen, was zu einer Kaskade führt. Neben Schleim weisen die Zellmembranen verschiedener Lungenzellen auch elektrische Ladungen auf, die mit der Verteilung von Ionen und Kanälen verbunden sind. Diese Ladungen spielen eine Rolle bei der Aufrechterhaltung des elektrischen Gleichgewichts und der Funktionalität der Lungenzellen.
Diese tragen auch zu den negativ geladenen Kompartimenten der Lunge bei. Da sich Gegensätze anziehen, wie in diesem Thread schon oft erwähnt, wird ein positiv geladener LNP nach seiner Zirkulation in diesem Bereich bleiben und hierher gehen und reagieren wollen.
Wenn positiv geladene LNPs in den Blutkreislauf gelangen ODER in die Lunge eingeatmet werden, interagieren sie mit dem negativ geladenen Schleim in den Atemwegen. Diese elektrostatische Wechselwirkung führt dazu, dass das positiv geladene LNP an den Mucinen „klebt“.
Omo-Lamai S, Zamora ME, Patel MN, Wu J, Nong J, Wang Z, Peshkova A, Chase LS, Essien EO, Muzykantov V, Marcos-Contreras O, Myerson JW, Brenner JS. Physicochemical Targeting of Lipid Nanoparticles to the Lungs Induces Clotting: Mechanisms and Solutions. bioRxiv [Preprint]. 2023 Jul 25:2023.07.21.550080. doi: 10.1101/2023.07.21.550080. PMID: 37546837; PMCID: PMC10401951. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10401951/
EN: "Here we found that lung-tropic LNPs employing cationic lipids induce massive thrombosis. We demonstrate that thrombosis is induced in the lungs and other organs, and greatly exacerbated by pre-existing inflammation."
DE: „Hier haben wir herausgefunden, dass lungentrope LNPs, die kationische Lipide verwenden, eine massive Thrombose auslösen. Wir zeigen, dass Thrombosen in der Lunge und anderen Organen induziert werden und durch bereits bestehende Entzündungen stark verschlimmert werden.“
Aber sie haben nicht gesagt, WARUM es in die Lunge gelangt.
EN: "This clotting is induced by a variety of formulations with cationic lipids, including LNPs and non-LNP nanoparticles. The mechanism depends on the LNPs binding to fibrinogen and inducing platelet and thrombin activation.”
DE: „Diese Gerinnung wird durch eine Vielzahl von Formulierungen mit kationischen Lipiden induziert, darunter LNPs und Nicht-LNP-Nanopartikel. Der Mechanismus hängt davon ab, dass die LNPs an Fibrinogen binden und die Aktivierung von Blutplättchen und Thrombin induzieren.“
Und wir wissen, dass negativ geladenes, stark negativ geladenes LNP nicht in die Milz gelangt, sondern nur leicht negativ geladen ist. Wenn es um das positiv geladene LNP geht, klebt es an den Muzinen, was in dieser Studie niemand sagt.
EN: “These mucins have a high negative surface charge and a large hydration capacity. Mucins act as the main structural component of the mucus layer, giving rise to its polymeric, viscoelastic and protective properties."
DE: „Diese Mucine haben eine hohe negative Oberflächenladung und eine große Hydratationskapazität. Muzine fungieren als Hauptstrukturbestandteil der Schleimschicht und verleihen ihr polymere, viskoelastische und schützende Eigenschaften.“
Dharmani P, Srivastava V, Kissoon-Singh V, Chadee K. Role of intestinal mucins in innate host defense mechanisms against pathogens. J Innate Immun. 2009;1(2):123-35. doi: 10.1159/000163037. Epub 2008 Oct 8. PMID: 20375571; PMCID: PMC7312850. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7312850/
Schauen wir uns nun einige Bedenken im Zusammenhang mit Mucinen und ihrer stark negativen Ladung an und wo sonst im Körper werden Sie diese Dinge in kleineren Mengen sehen:
Magen-Darm-Trakt, Fortpflanzungssystem, Speicheldrüse, Augenoberfläche, Harntrakt und Becherzellen, sie befinden sich jedoch ALLE in der Lunge – nur gefüllt.
LNPs mit einer positiven Ladung bleiben auch an diesen Dingen hängen, aber die Lungen werden leichter und schneller zugänglich sein:
Und das ist NOCH nicht alles. „Der Mechanismus hängt davon ab, dass die LNPs an Fibrinogen binden und die Aktivierung von Blutplättchen und Thrombin induzieren.“
Die Studienautoren haben diese Studie nicht gesehen:
BOOM! :
„Positiv geladene Oberfläche löst Gerinnungsaktivierung durch Faktor-VII-aktivierende Protease (FSAP) aus“
Die positiv geladene Oberfläche des LNP bindet sich an Mucin in der Lunge und verursacht Gerinnsel (Lungenembolie – es gibt auch noch ein paar andere Mechanismen, das ist nicht der einzige, das Spike ist nicht der einzige, seufz, oder die Aktivierung des Immunsystems) interagiert auch nicht nur in der Lunge, sondern auch in andere Bereiche des Körpers, und dies ist der Beginn dieses Mechanismus (denken Sie daran, dass negative Ladung auch Blutgerinnsel verursacht – die dicken, spindelförmigen!).
EN: "Contact between biomedical materials and blood often initiates undesirable pro-coagulant and pro-inflammatory processes. On negatively charged materials blood coagulation is known to be triggered through auto-activation of Factor XII, while activation on cationic surfaces follows a distinct and so far enigmatic mechanism."
DE: „Der Kontakt zwischen biomedizinischen Materialien und Blut löst häufig unerwünschte gerinnungsfördernde und entzündungsfördernde Prozesse aus. Bei negativ geladenen Materialien wird die Blutgerinnung bekanntermaßen durch die Autoaktivierung von Faktor Mechanismus."
Sperling C, Maitz MF, Grasso S, Werner C, Kanse SM. A Positively Charged Surface Triggers Coagulation Activation Through Factor VII Activating Protease (FSAP). ACS Appl Mater Interfaces. 2017 Nov 22;9(46):40107-40116. doi: 10.1021/acsami.7b14281. Epub 2017 Nov 9. PMID: 29091393. https://pubmed.ncbi.nlm.nih.gov/29091393/
EN: "Factor VII activating protease (FSAP), is known to be activated on positively and on negatively charged macromolecules in plasma"
DE: „Faktor VII aktivierende Protease (FSAP) wird bekanntermaßen auf positiv und negativ geladenen Makromolekülen im Plasma aktiviert.“
Miyata S. New aspects in fenestrated capillary and tissue dynamics in the sensory circumventricular organs of adult brains. Front Neurosci. 2015 Oct 27;9:390. doi: 10.3389/fnins.2015.00390. PMID: 26578857; PMCID: PMC4621430. https://pubmed.ncbi.nlm.nih.gov/26578857/
Wie kann also ein LNP positiv geladen sein, wenn die meisten Kapitel/Threads von negativ geladenen Verunreinigungen handeln, wie z. B. einer DNA-Plasmid-Kontamination (hohe negative Ladung?), die in der jüngsten Präsentation von Speicher/McKernan/Rose von der Korrelation zwischen höherer DNA-Plasmid-Kontamination sprach in Chargen mit hohen Daten zu unerwünschten Ereignissen wie Myokarditis?
Einfach. DNA-Lipoplex-Solobildung (DNA-Plasmide in der Mitte des Liposoms haben es nie in LNP geschafft, oder die RNA/DNA ist beim Einfrieren und Auftauen ausgetreten, wodurch sich das Verhältnis zwischen den positiv geladenen Lipiden und der modRNA in einen positiver geladenen Zustand verändert hat.
Wir wissen, dass mehrere Studien, darunter Dr. Ko und Dr. De (2023), Carusso et al. und einige andere, zeigen, dass das LNP während des Gefrier-Auftau-Prozesses abgebaut wird und die Nukleinsäuren (RNA/DNA) herausrutschen. Dr. McCairn in Japan führte sogar einige Tests einschließlich Mikroskopie an einigen Fläschchen durch und zeigte, dass keine Nukleinsäure (kein Phosphor) vorhanden war.
(*Anmerkung DrBine: Den Versuch von Kevin kenne ich nicht. Ich kenne aber einen ähnlichen von einem Kanadier und er hat das falsche Elektronenmikroskop genommen, eines von Geologen, die können organische Materialien nicht detektieren. Irgendwas mit Fenster oder nicht Fenster.*)
Die Leute sagen immer wieder: „Ich habe die Kontrolle, ich habe die Placebos.“ Nein, nein, wenn Sie nur eine direkte Injektion von LNP und Lipiden ohne RNA oder DNA erhalten, dann erhalten Sie positiv geladene Lipide mit einem hochpositiven Zeta-Potenzial. Und das kann zu einem Gerinnsel führen. ODER, weil die DNA-Kontamination möglicherweise einen eigenen Lipoplex gebildet hat und nicht Teil des LNP ist, der aufgrund des Verhältnisses von DNA zu positiven Lipidladungen (abhängig von den Basenpaaren in der DNA) eine hohe positive Ladung aufweisen könnte.
Wenn man das Verhältnis von positiven zu negativen Ladungen ändert, verändert sich auch die Oberflächenladung (Zeta) und verändert, wohin sie geht und woran sie bindet.
Brader ML, Williams SJ, Banks JM, Hui WH, Zhou ZH, Jin L. Encapsulation state of messenger RNA inside lipid nanoparticles. Biophys J. 2021 Jul 20;120(14):2766-2770. doi: 10.1016/j.bpj.2021.03.012. Epub 2021 Mar 25. PMID: 33773963; PMCID: PMC8390897. https://pubmed.ncbi.nlm.nih.gov/33773963/
=== Teil 12 ===
Hoch negativ geladene Stoffe (hoher Netto-negativer Zeta-Wert) gelangen in die Gefäße und können zu Megagerinnseln führen (leicht negativer Kopf-Milz-Wert).
Reden wir über negative Ladungen!
Carrasco MJ, Alishetty S, Alameh MG, Said H, Wright L, Paige M, Soliman O, Weissman D, Cleveland TE 4th, Grishaev A, Buschmann MD. Ionization and structural properties of mRNA lipid nanoparticles influence expression in intramuscular and intravascular administration. Commun Biol. 2021 Aug 11;4(1):956. doi: 10.1038/s42003-021-02441-2. PMID: 34381159; PMCID: PMC8358000. https://pubmed.ncbi.nlm.nih.gov/34381159/
Wir wissen aus anderen Threads (siehe meinen Beitragsverlauf), dass positive und negative Ladungen Blutgerinnsel verursachen. Vor ungefähr einem Jahr habe ich einen großen Substack geschrieben und über negativ geladene Teilchen gepostet (er ging viral), der jetzt noch einmal gelesen werden muss, und wir haben darüber gesprochen!
Diese Einbalsamierer und andere sehen diese dicken, spindelförmigen Klumpen, die andere Eigenschaften haben, als sie normalerweise im postmortalen „Hühnerfett“ sehen würden (ja, ich kenne die „eckligen“ Begriffe, die ihr Pathologen verwendet, mein Pathologenfreund klärt mich auf. Die Pathologen verwenden die ecklige Anatomie)
So viele Leute sagten, dass dies nicht passieren würde und dass sich diese „Super“-Blutgerinnsel auf keinen Fall bilden könnten (so wie uns gesagt wurde, dass es Turbokrebs auf keinen Fall gibt), aber diese Studie (und es gibt noch andere) wurde 2019 abgeschlossen und 2020 veröffentlicht von einem Forscherteam, das die tatsächliche physikalische Dynamik von negativ geladenen Liposomen und der Gerinnung untersuchte, und was sie herausfanden, ist verblüffend:
Faizullin D, Valiullina Y, Salnikov V, Zuev Y. Direct interaction of fibrinogen with lipid microparticles modulates clotting kinetics and clot structure. Nanomedicine. 2020 Jan;23:102098. doi: 10.1016/j.nano.2019.102098. Epub 2019 Oct 23. PMID: 31655206. https://www.sciencedirect.com/science/article/abs/pii/S1549963419301820
EN: “Extensive studies revealed the role of blood lipid microparticles (liposomes, microvesicles) in activation of coagulation cascade. The direct interaction of fibrinogen/fibrin with lipid surfaces and its consequence for hemostasis received much less attention. We observed pronounced changes in both clot morphology and kinetics of fibrin clotting in the presence of artificial liposomes.”
DE: „Umfangreiche Studien zeigten die Rolle von Blutfett-Mikropartikeln (Liposomen, Mikrovesikeln) bei der Aktivierung der Gerinnungskaskade. Die direkte Interaktion von Fibrinogen/Fibrin mit Lipidoberflächen und deren Folgen für die Hämostase erhielten weitaus weniger Aufmerksamkeit. Wir beobachteten deutliche Veränderungen sowohl in der Gerinnselmorphologie als auch in der Kinetik der Fibringerinnung in Gegenwart künstlicher Liposomen.“
UND!
EN: “The main population of circulating lipid microparticles in blood is formed by the platelet MVs, released into the bloodstream under the platelets activation. It has beenestablished that MVs in blood can influence fibrin formation, clot structure and resistance to lysis due to their participation in the generation of active thrombin and plasmin.”
DE: „Die Hauptpopulation der zirkulierenden Lipidmikropartikel im Blut wird von den MVs der Thrombozyten gebildet, die durch die Aktivierung der Thrombozyten in den Blutkreislauf freigesetzt werden. Es ist erwiesen, dass die MVs im Blut die Fibrinbildung, die Gerinnungsstruktur und die Lysebeständigkeit beeinflussen können, da sie an der Bildung von aktivem Thrombin und Plasmin beteiligt sind.“
Und:
„Mit der Dosenelektronenmikroskopie (REM) wurde die Struktur von Gerinnseln untersucht, die in Gegenwart oder Abwesenheit von MLV-Partikeln gebildet wurden. Gerinnsel wurden durch Zugabe von Tb zu Fg-Lösung oder Lipid-MLV in Puffer 1 erzeugt. Die Endkonzentrationen waren: Fg 1 mg/ml, Lipid 1 mg/ml, Tb 0,26 NIH. Alle Einzelheiten des Verfahrens sind im Zusatzmaterial beschrieben.“
Zetapotential gemessen!: „Um die Wechselwirkung von Fg mit Lipidpartikeln zu untersuchen, haben wir das Zetapotential und die hydrodynamische Größe des SUV beim Titrieren mit Fg-Lösung gemessen. Lipidsuspensionen und Fg-Lösungen wurden in Puffer 2 hergestellt, 10 Minuten bei 10.000 × g zentrifugiert und auf einem Zetasaizer gemessen Nano-Spektrometer (Malvern Panalytical Ltd.) bei 37 °C.“
Hier ist die Verfolgung der Fibrinogenbildung und der Lipidkomponenten grafisch dargestellt. Als nächstes kommt Zeta und Fibrinogen (CLOT).
Schauen Sie sich diese Tabelle an. Wow. Dies ist der Zusammenhang zwischen der Ladung auf der Oberfläche und der Fibrinogenbildung.
DAS ist wichtig:
EN: "These data illustrate that the effective charge of the bilayer formed by neutral zwitterionic lipids is generally non-zero due to surface adsorption of counterions and depends on the ratio of saturated and unsaturated fatty acid tails and conformation of head groups. Upon the adsorption of any ligand the counterions will be displaced out of the surface that is accompanied by zeta potential variations"
DE: „Diese Daten veranschaulichen, dass die effektive Ladung der durch neutrale zwitterionische Lipide gebildeten Doppelschicht aufgrund der Oberflächenadsorption von Gegenionen im Allgemeinen ungleich Null ist und vom Verhältnis der gesättigten und ungesättigten Fettsäureschwänze und der Konformation der Kopfgruppen abhängt.“
Durch die Adsorption eines Liganden werden die Gegenionen aus der Oberfläche verdrängt, was mit Schwankungen des Zetapotentials einhergeht.
Darauf werden wir später noch eingehen.
Zurück zu den Gerinnseln.
EN: "The dimensions of lipid particles represent another factor having noticeable impact on the fibrin clot structure. Influence of size of non-adsorbing EPC particles on clotting kinetics differs in case of large particles in crude suspension and after homogenization by ultrasound down to small sized MLVs (Figure 2, B). Small-sized EPC MLVs do not influence kinetics at all. Largesized particles in crude suspension modify kinetics simply posing spatial barriers to diffusion and fibril propagation."
DE: „Die Abmessungen der Lipidpartikel stellen einen weiteren Faktor dar, der einen spürbaren Einfluss auf die Fibringerinnselstruktur hat. Der Einfluss der Größe nicht adsorbierender EPC-Partikel auf die Gerinnungskinetik unterscheidet sich bei großen Partikeln in der Rohsuspension und nach der Homogenisierung durch Ultraschall bis hin zu kleinen MLVs ( Abbildung 2, B). Kleine EPC-MLVs beeinflussen die Kinetik überhaupt nicht. Große Partikel in der Rohsuspension verändern die Kinetik und stellen lediglich räumliche Barrieren für die Diffusion und Fibrillenausbreitung dar.“
Dies wurde in den früheren Threads, die ich über die Größe von LNP und Zeta erstellt habe, besprochen.
EN: "Being bound to the membrane surface, coagulation proteases become thousands of times more active due to the formation of spatially arranged multi-enzyme complexes facilitating the surface-directed transfer of the activated coagulation factors between the various complexes."
DE: „Durch die Bindung an die Membranoberfläche werden Gerinnungsproteasen durch die Bildung räumlich angeordneter Multienzymkomplexe um ein Vielfaches aktiver und ermöglichen so den oberflächengerichteten Transfer der aktivierten Gerinnungsfaktoren zwischen den verschiedenen Komplexen.“
Der Gerinnungsprozess ist in Gegenwart dieser negativ geladenen Liposomen, auch bekannt als LNP, tausendmal aktiver!
=== Teil 13 ===
DAS HERZ HAT ZETA-POTENZIAL!
Das Herz-Zeta-Potential ist bei Menschen mit Bluthochdruck anders!
Raten Sie mal, was das bedeutet, wenn es um die Interaktion mit einem LNP geht, insbesondere mit einem LNP, auf dem sich eine hohe Ladung befindet?
Die Studie (um die es in diesem Kapitel geht):
S. Gaikwad, Swati, Jasmine G. Avari, and Mansi Liladhar Patil. 2020. ‘Zeta Potential as a Diagnostic Tool to Determine the Angina Risk’. Apolipoproteins, Triglycerides and Cholesterol. IntechOpen. doi:10.5772/intechopen.92373. https://www.intechopen.com/chapters/72171
Cliff-Anmerkungen: Die Studie beobachtete Variationen im Erythrozyten-Zeta-Potenzial im Herzen und morphologische Veränderungen bei Patienten mit Bluthochdruck und Myokardinfarkt. Was ist mit den LNP?
(*Anmerkung DrBine: Cliff-Anmerkung bezieht sich auf CliffsNotes, einen bekannten englischsprachige Reihe von Lektüreschlüsseln https://en.wikipedia.org/wiki/CliffsNotes, entspricht im Deutschen etwa der Serie „Für Dummies“, nur für Schullektüren*)
Die vorherigen Threads geben Aufschluss darüber, wie sich das Zeta-Potenzial in verschiedenen Körperteilen je nach pH-Wert, Ladung, Viskosität usw. ändern kann (wir haben noch nicht einmal alles behandelt! Bald!)
Was aber, wenn ein aufgeladener LNP in das Herz von jemandem eindringt, der eine anderes Zetapotential hat?
Erythrozyten (rote Blutkörperchen/Erythrozyten) sind eine Art von Blutzellen. Ihre Hauptfunktion besteht darin, Sauerstoff von der Lunge zu allen Geweben und Organen des Körpers zu transportieren und Kohlendioxid von den Geweben zurück zur Lunge zu befördern, wo es ausgeatmet werden kann.
Die Studie ergab, dass Patienten mit Bluthochdruck im Vergleich zu gesunden Probanden eine signifikante Verringerung des Zeta-Potenzials (ZP) aufwiesen. Die Oberflächenladung von Erythrozyten ist bei Bluthochdruckpatienten geringer als bei gesunden Personen (Oberflächenladung = Zeta).
Bemerkenswerterweise war die Reduzierung des ZP (Zeta-Potenzial) bei Patienten, die sowohl an Bluthochdruck als auch an einem Myokardinfarkt (MI) litten, noch signifikanter. Die ZP-Werte in dieser Gruppe waren im Vergleich zu gesunden Personen und solchen mit alleiniger Hypertonie deutlich niedriger.
In der Studie wird festgestellt, dass eine Verringerung des ZP mit einer Verformung der Erythrozyten (Anisozytose) und einer erhöhten Fragilität der Erythrozyten einhergeht, die beide bei Patienten mit Bluthochdruck und MI beobachtet wurden. Diese Veränderungen der Erythrozyteneigenschaften stehen im Zusammenhang mit oxidativem Stress, der durch reaktive Sauerstoffspezies (ROS) verursacht wird. Patienten mit MI, die sich einer Bypassoperation der Koronararterien (coronary artery bypass grafting, CABG) und einer Angioplastie unterzogen und Medikamente erhielten, wiesen im Vergleich zu unbehandelten MI-Patienten höhere ZP-Werte auf.
Was bedeutet es, wenn ein LNP mit neutraler Ladung oder weitgehend neutralem Zetapotenzial in das Herz einer gesunden Person eindringt und nicht in das einer Person mit Bluthochdruck? Was bedeutet es, wenn ein LNP mit stark negativem Zeta-Potenzial in das Herz eines Gesunden eindringt und ein LNP mit unterschiedlichem Zeta-Potenzial? Positives Zeta? (positives Zeta hat einen Tropismus für die Lunge, denken Sie daran, und Hyperkoagulation. Aber das gilt auch für negative. Fazullin et al. 2020 zeigt das).
Das bedeutet, dass es einen Unterschied zwischen den Ionen oder dem pH-Wert oder beidem in den Herzen gesunder Menschen und solchen mit Bluthochdruck geben muss.
Das Zetapotenzial hängt von vielen Faktoren ab (wie bereits erwähnt), und Ionen und pH sind zwei davon. Herz-Kreislauf-Erkrankungen können das Säure-Basen-Gleichgewicht des Körpers beeinträchtigen, was zu Veränderungen des pH-Werts im Blut führen kann. Bei Bluthochdruck sind auch die Ionen im Herzen anders.
Oxidativer Stress kann zu Veränderungen in der Zusammensetzung der Erythrozytenmembran und dem Vorhandensein geladener Gruppen auf der Zelloberfläche führen, was das Zetapotenzial beeinflussen kann. Blut enthält verschiedene Ionen, darunter Natrium, Kalium, Chlorid und Bikarbonat, die zu seiner ionischen Zusammensetzung beitragen und das Zetapotenzial von Zellen und Partikeln im Blutstrom verändern. Bluthochdruck verändert die Blutviskosität, wodurch das Blut dicker und fließfähiger wird. Veränderungen der Blutviskosität können sich auf das Zetapotenzial auswirken, da es durch den Abstand zwischen Partikeln oder Zellen in der Flüssigkeit beeinflusst wird. Bluthochdruck kann zu endothelialer Dysfunktion, oxidativem Stress und Entzündungen führen, die wiederum die Oberflächeneigenschaften von Zellen und Partikeln im Blut beeinflussen können. Diese Veränderungen wirken sich auf das Zetapotenzial aus. Außerdem kann sich bei hartem Training, wie bei Sportlern (FUSSBALL!), Milchsäure im Herzen ansammeln. Diese geht zwar wieder weg, aber währenddessen kann sie sich bei manchen Menschen ansammeln, und wenn das der Fall ist, raten Sie mal, was dann beeinträchtigt wird: Zeta!
WENN sich das Herz nun nicht in einem gesunden Zustand befindet und eine Entzündung oder andere Probleme aufgrund von Bluthochdruck, verändertem Zeta usw. aufgetreten sind, besteht die Gefahr, dass die folgenden Probleme auftreten (sie treten auch bei gesunden Herzen auf, mit der Plasmid-DNA, negativem Zeta usw., aber dieser Zustand verschlimmert die Situation): Stark negativ geladene LNPs können im Zusammenhang mit einem geschädigten oder entzündeten Herzen bestimmte Verhaltensweisen zeigen:
Entzündliche Zustände können das Immunsystem stimulieren. Stark negativ geladene LNP sind möglicherweise anfälliger für die Erkennung durch das Immunsystem.
*** - Entzündetes Gewebe setzt häufig entzündungsfördernde Zytokine frei.
Stark negativ geladene LNP könnten mit Zytokinen oder zellulären Faktoren interagieren, die als Reaktion auf eine Entzündung freigesetzt werden, und so möglicherweise eine Immunreaktion auslösen, die zu unerwünschten Ereignissen beiträgt.
Wenn das Immunsystem die LNPs aufgrund ihrer negativen Ladung als Fremdkörper oder potenzielle Bedrohung erkennt, kann es Immunzellen wie T- oder B-Zellen aktivieren, was zu Immunreaktionen führt.
Neutrale LNPs können mit Immunzellen im geschädigten Herzen interagieren, die sie als fremde Substanzen erkennen und das Immunsystem aktivieren können.
Neutrale LNPs können mit Zytokinen und Chemokinen interagieren, die aus dem geschädigten Herzgewebe freigesetzt werden. Diese Wechselwirkungen können zur Rekrutierung und Aktivierung von Immunzellen führen und so zu Entzündungen oder unerwünschten Ereignissen beitragen.
Die Interaktion mit Immunzellen oder das Vorhandensein von LNPs im geschädigten Herzgewebe könnte zu einer lokalen Entzündung beitragen und bestehende Entzündungen und Gewebeschäden verschlimmern.
🚨🚨🚨Die Erkennung von LNPs durch das Immunsystem kann Immunreaktionen auslösen, einschließlich der Freisetzung von entzündungsfördernden Zytokinen, der Aktivierung von Immunzellen sowie allergischer oder Überempfindlichkeitsreaktionen. 🚨🚨🚨🚨🚨🚨
Die vorzeitige Freisetzung der LNP-Nutzlast, wie z. B. RNA oder Arzneimittel, aufgrund von Wechselwirkungen mit entzündetem Gewebe könnte zu lokaler Toxizität oder unbeabsichtigten pharmakologischen Wirkungen führen.












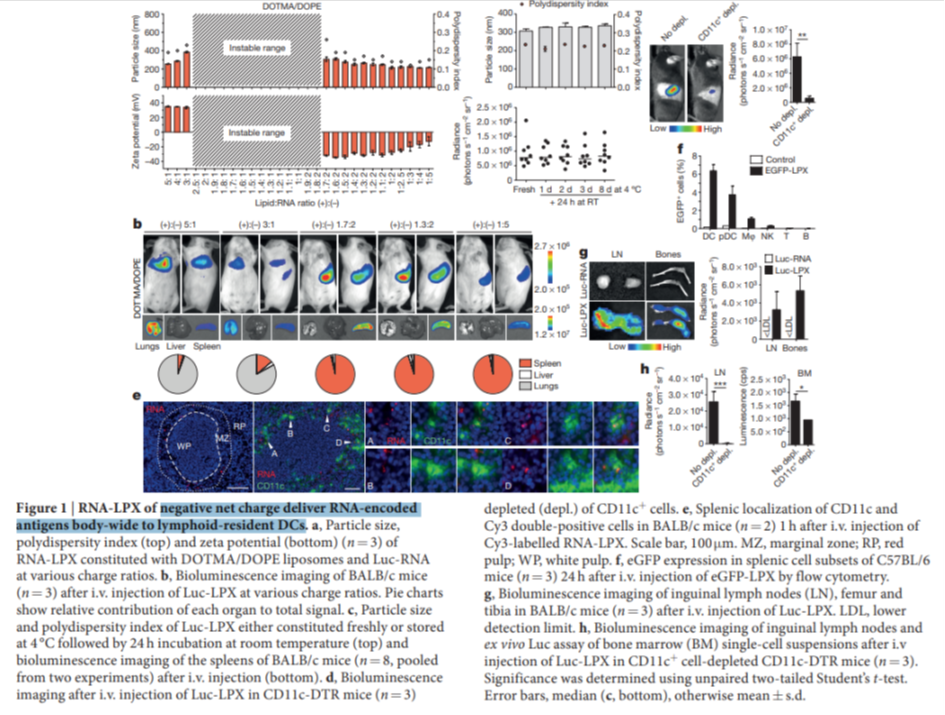






























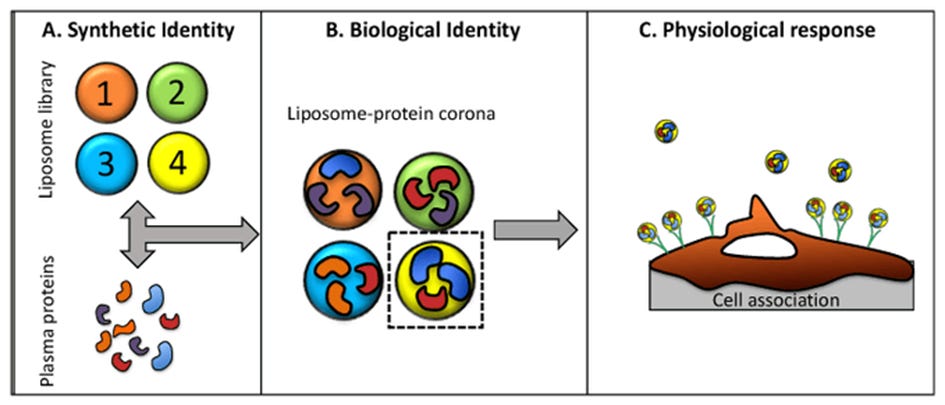






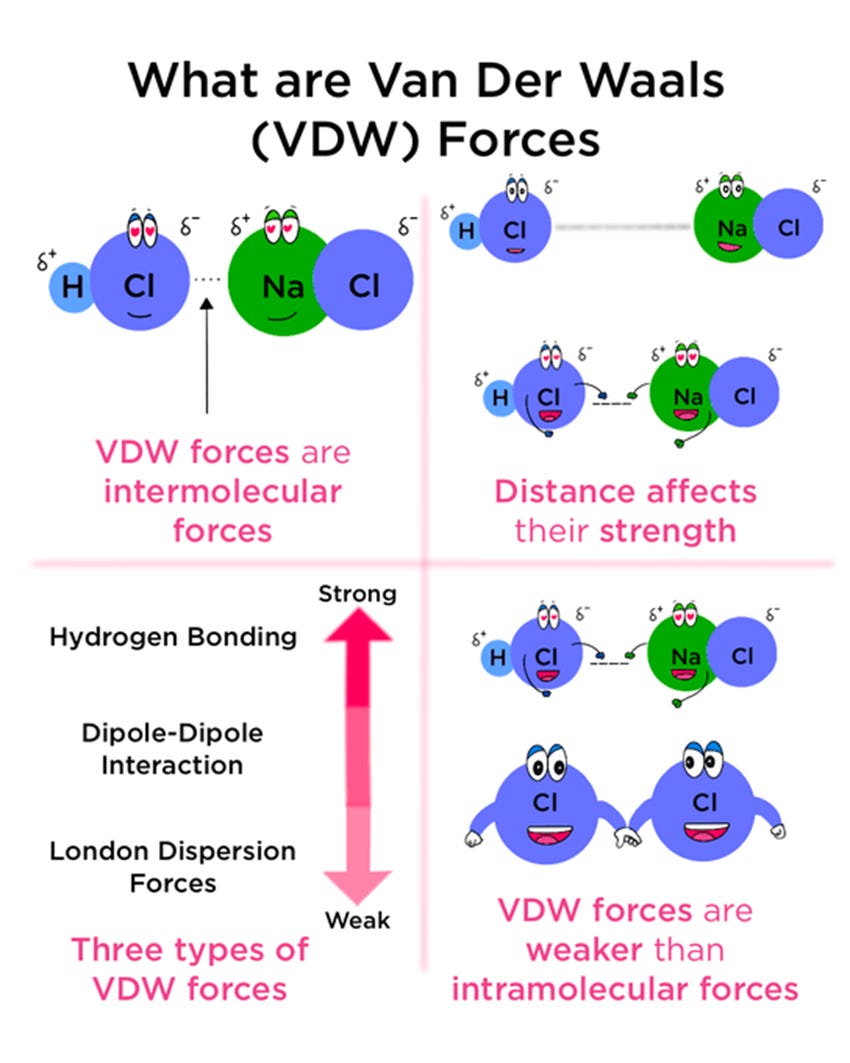



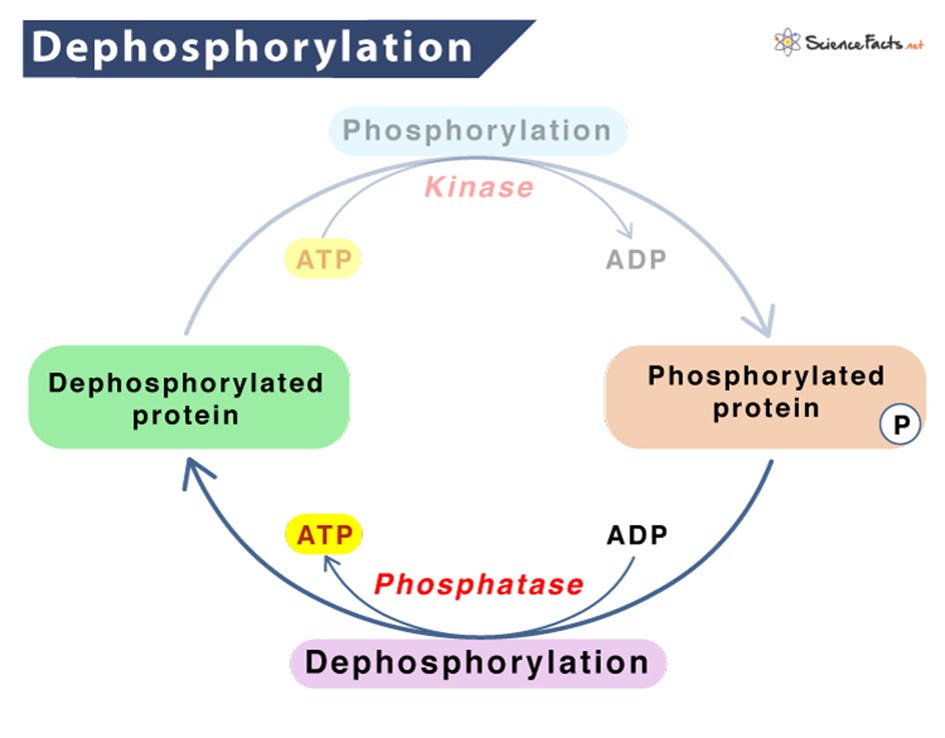
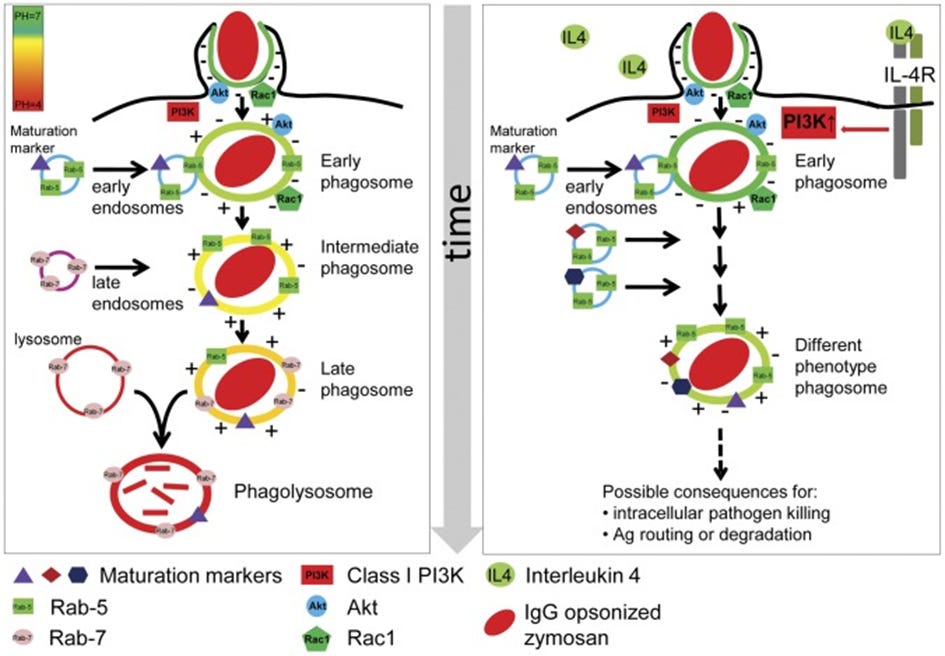



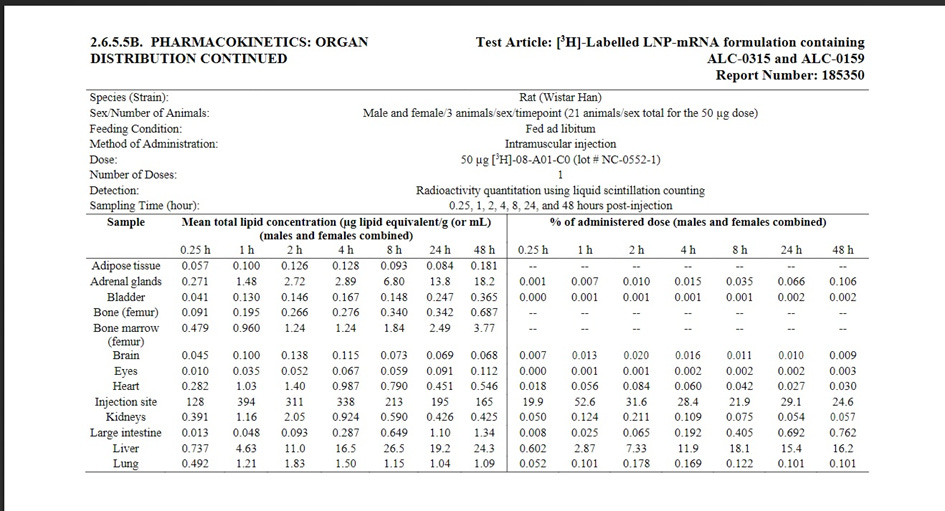








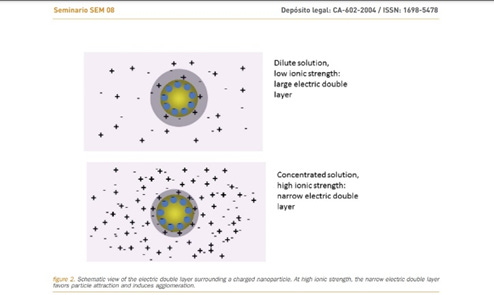















While cryptic for now, do necropsies turn up amyloid clots in darted mammals? Mysterious sequence in SV40. What if a veterinarian were to supply them with a vial of Pzp to compare?
And/or ... Characterization of Classical Vaccines by Charge Detection Mass Spectrometry https://pubmed.ncbi.nlm.nih.gov/34435777/
The strange link between the sterilization of wild horses and mRNA vaccines https://archive.ph/pt8mu
Too much to convey here but IMV irt SpayVac mammal immunocontraceptive vaccine. March 2020. SEC filings prior courting human vaccine companies like Pfizer to be the supplier of their lipid nanoparticles. DPX-COVID-19 ... capacity to bind on target to the spike protein. Couple SEC filings: https://archive.ph/fGy0F https://archive.ph/LTUMJ
A blur. We're talking reduction of baby count in overabundant invasive species mammals and also human covid vaccines out of the other side of the mouth.
Well, I mean, ok, put yourself in their shoes, if you control trillions and it's your job to save the planet from what those around you are warning is certain disaster ahead from skyrocketing population growth, would you want to avert more brutal war or even the nuclear option to cull the herd? With an apparently more compassionate route a la the series Utopia via a fake pandemic to get everybody injected with fertility reduction?
A competent elite class would just offer gift cards for voluntary vasectomies problem solved instead of all these shenanigans but I guess deception is too much fun for them to resist. I imagine they have to fear each other, peer fear, and so daring to suggest the idea might be risky at a dinner party on the yacht. Imagine: You're sitting there with the guys who engineered the whole scam and say: "Gentlemen, it's possible Bill's "next pandemic" might turn into an even uglier crash and burn than this one, what say we instead get honest, publish all the scary statistics that are making us all lose sleep and just offer gift cards for voluntary vasectomies?
Bob, you feeling ok? Where's the fun in being honest with them?
In der Elektrotechnik ist Potentialausgleich, in Form einer gute Erdung, das Fundament für ein stabiles und sicheres Funktionieren. Zeta-Potential hinterlässt in mir den tiefen Eindruck, wie sehr wir auch elektrische Wesen sind. Könnte eine gute Erdung, sprich Potentialausgleich mit Mutter Erde, doch eine Bedeutung für unser Wohlbefinden und Gesundheit haben? In unsere modernen Gesellschaft wandeln wir sehr isoliert von Mutter Erde durch das Leben, dank "schützender" Schuhe mit Sohlen aus Kunststoff.